文献解读|Signal Transduct Target Ther(52.7):单细胞转录解析揭示胰腺导管腺癌转移过程中免疫抑制微环境的演变
✦ +
+
论文ID
原名:Single-cell transcriptional dissection illuminates an evolution of immunosuppressive microenvironment during pancreatic ductal adenocarcinoma metastasis
译名:单细胞转录解析揭示胰腺导管腺癌转移过程中免疫抑制微环境的演变
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2025.06.09
DOI号:10.1038/s41392-025-02265-0
背 景
胰腺癌仍然是肿瘤学中最艰巨的挑战之一,约占所有癌症相关死亡人数的 8.5%。胰腺导管腺癌 (PDAC) 是胰腺最常见的恶性肿瘤,约占所有病例的 80%,5 年生存率低于 12%。PDAC的治疗前景复杂,因为绝大多数患者(超过 80%)就诊时患有不可切除的疾病,并且以区域或远处转移为特征。虽然手术切除后进行辅助治疗是局部早期疾病患者的标准治疗方式,但化疗对大多数不可切除的患者无效,凸显了对新治疗策略的迫切需求。除了常规疗法的晚期检测和疗效有限的挑战之外,PDAC 还对免疫检查点阻断等免疫疗法具有抗药性,而免疫疗法已在治疗其他各种恶性肿瘤方面取得成功。但是,在PDAC从正常细胞向恶性肿瘤演变的过程中,宿主免疫系统如何丧失其监视功能仍是未知的。
实验设计
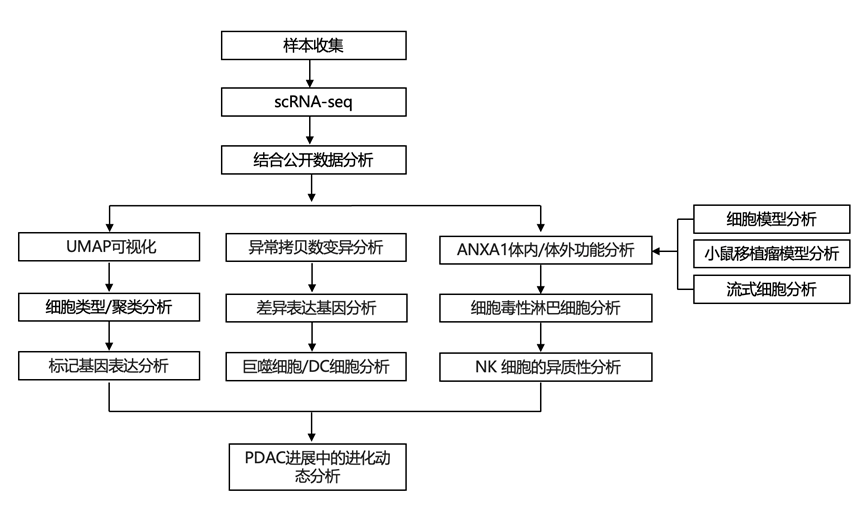
结 果
01
PDAC转移过程中细胞生态系统的转录分析
为了探究PDAC转移过程中肿瘤微环境的演变,研究团队利用10×Genomics平台对6例肝转移患者匹配的原发性和转移性病灶、2例健康供体胰腺组织(HD)和2例原发性非转移性胰腺肿瘤(primary_NM)进行了单细胞转录组分析(scRNA-seq)。同时,他们整合了来自两个公共数据集(CRA001160和GSE205049)的scRNA-seq数据,其中包括20例HD病灶和15例原发性NM病灶(图1a),共获得132115个单细胞转录组数据,其中包括来自22个HD组织的26786个细胞,来自17个原发性NM组织的43928个细胞,来自6个伴有肝转移的原发性肿瘤(原发性HM)的26281个细胞,以及来自6个肝转移(HM)病变的35120个细胞(图1b)。细胞类型由典型标记定义和呈现,这些标记基于细胞类型、组织来源(图1c-d)和患者来源通过均匀流形近似和投影(UMAP)图进行可视化。PTPRC阴性(CD45-)细胞进一步定义为上皮细胞(EPCAM+、KRT8+、KRT18+、KRT19+)、内皮细胞(VWF+、CDH5 +、ENG +、PECAM1 +)、成纤维细胞(FAP+、COL1A1 +、DCN +),而PTPRC阳性(CD45 +)细胞进一步定义为 B 细胞(CD79A+、CD79B +、MS4A1 +)、T 细胞(CD3D+、CD3E +、CD3G +)、NK细胞(KLRF1+、KLRD1 +、GNLY +)、单核细胞(CD14 +、S100A12 +)、巨噬细胞(FCGR3A +、CD68 +、CD86 +)、中性粒细胞(FCGR3B+、 FPR1 +)、树突状细胞(HLA-DRA +、 FCER1A +) 和肥大细胞(MS4A2 +、TPSAB1+、 KIT+)(图1e-f)。
整合分析利用了三个数据集的互补优势:CRA001160 队列(主要包含来自 HD 和 Primary_NM 样本的非免疫细胞)、GSE205049 数据集(包含来自 HD 和 Primary_NM 样本的免疫细胞)以及本研究的 scRNA-seq 数据(涵盖 HD、Primary_NM、Primary_HM 和 HM 样本的免疫和非免疫细胞)。虽然实验设计各异,但系统的批次校正(RPCA、CCA 和 Harmony)实现了跨平台细胞区室的稳健整合,低维 UMAP 投影中免疫细胞的无缝对齐证明了这一点。相反,非免疫上皮细胞显示出反映其生物起源的聚类模式。本研究数据集(P7 和 P8,共 21230 个细胞)和 CRA001160 数据集中来自 HD 和 Primary_NM 样本的上皮细胞共聚类。然而,来自 Primary_HM 和 HM 病变的上皮细胞形成了不同的距离,表明在 PDAC 演化过程中上皮细胞存在疾病特异性异质性。这些结果证实了跨数据集数据整合的可靠性,同时揭示了上皮细胞的疾病特异性异质性。
分数柱状图(图1g)和 UMAP 图(图1c-d)显示了每种细胞类型的百分比和分布。本研究的综合分析证明了在从健康胰腺到转移性病变的疾病进展阶段中系统地识别所有主要的免疫和基质成分。这些发现强调了本研究数据在捕捉不同疾病阶段的 PDAC 微环境异质性方面的稳健性。此外,来自不同患者甚至器官的内皮细胞在图上聚集在一起(图1c-d)。这表明这些非恶性细胞具有相似的表达特征。此外,他们观察到来自 HM 和原发性胰腺病变的免疫和基质群体合并成转录连贯的群体,而不是按组织来源分离(图1c-d)。这种空间趋同表明胰腺癌细胞可能通过显性功能程序重编程宿主微环境,从而有效地覆盖肝脏微环境信号,从而重现类似胰腺的生态系统。至关重要的是,即使排除微环境细胞,转录重叠仍然存在,这表明原发性上皮细胞和转移性上皮细胞区室之间存在固有的生物学连续性。这些发现共同证实了HM是一个连续的疾病阶段,其中转移性播散代表了胰腺癌进展的一个进化但基本连续的阶段。
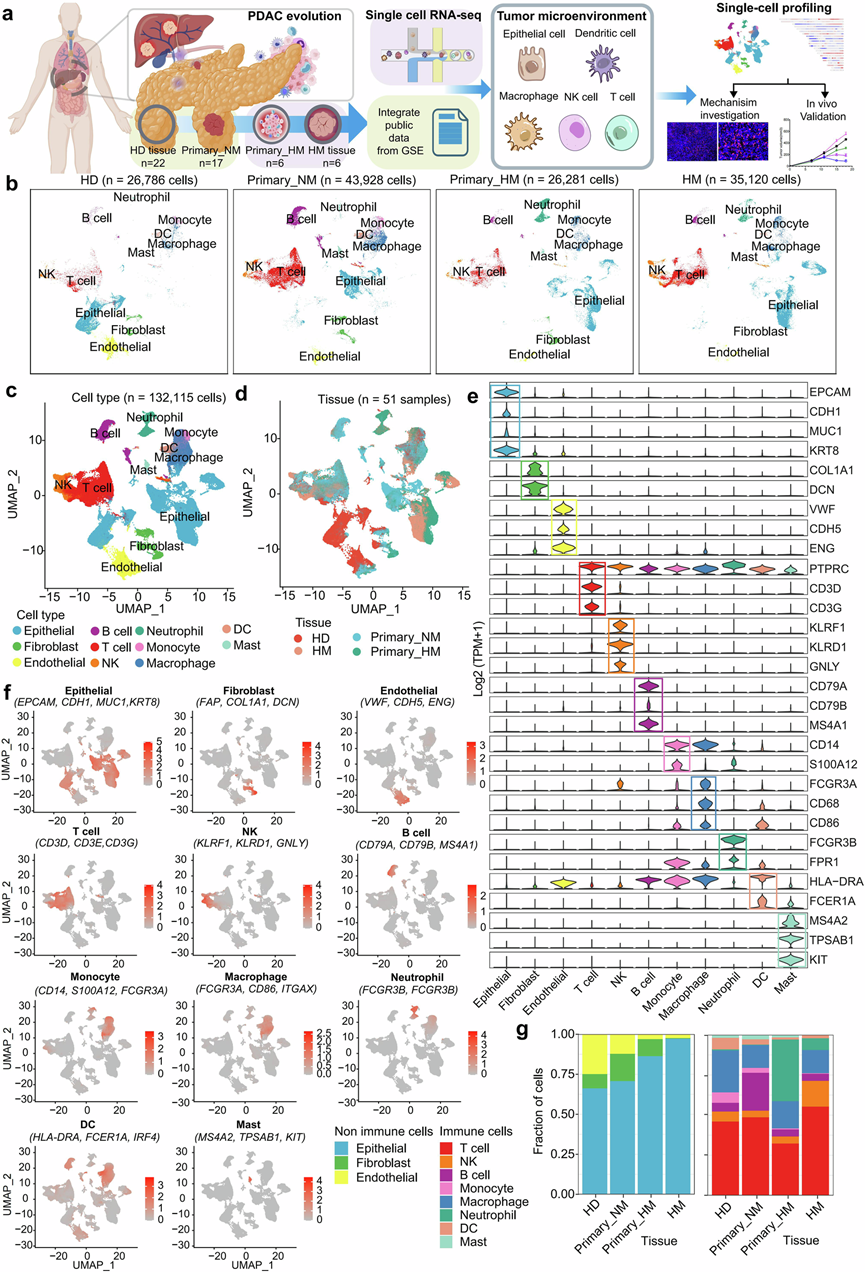
图1. PDAC 转移中肿瘤微环境的特征。
(a) 旨在解剖 PDAC 转移中肿瘤微环境的实验设计示意图。(b) UMAP图显示了从健康供体(HD)、无转移的原发肿瘤(Primary_NM)、有转移的原发肿瘤(Primary_HM)和转移性肿瘤(HM)的活检中鉴定出的不同细胞类型。(c-d) UMAP 图说明了按细胞类型和组织来源分类的所有测序细胞的分布,并指示了相应的颜色代码。(e) 小提琴图显示了标记基因在不同细胞类型中的表达谱。(f) UMAP 图叠加了指定细胞亚型的标记基因平均表达水平,从灰色到红色。(g)条形图显示了HD、Primary_NM、Primary_HM和HM队列中每种细胞类型的比例。
02
PDAC转移过程中上皮细胞改变的特征
每种细胞类型的百分比结果中一个有趣的现象是,从健康组织到转移性病变,上皮细胞的比例逐渐增加(图1g)。为了阐明其潜在机制,他们首先关注上皮细胞群。使用 CopyKT 算法通过恶性指数异常拷贝数变异 (CNV)区分正常上皮细胞(NEC)和肿瘤恶性上皮细胞(TEC)。使用 UMAP 根据恶性强度、组织来源和 CNV 评分绘制上皮细胞的转录组(图2a-d)。有趣的是,虽然正常上皮细胞和恶性肿瘤细胞在基因拷贝数改变方面表现出明显的差异,但无转移的原发性肿瘤细胞、有转移的原发性肿瘤细胞和转移性肿瘤细胞之间的 CNV 评分是可比的(图2b-d)。然后,他们从上述活检样本中解剖恶性肿瘤细胞中每个染色体的CNV。异常CNV在某些染色体上观察到,这些染色体是判断恶性肿瘤的标准,例如3、7、8、9和20号染色体(图2e)。值得注意的是,在肿瘤演变过程中表征恶性程度方面,7号和20号染色体的CNV似乎更可靠、更一致,这表明诊断目标可能具有功能。
随后,他们尝试在基因水平上表征每个阶段之间的变化(图2f)。差异表达基因(DEG)分析表明,与胰腺生理功能相关的基因,如INS、ALB、CTRB2和PLA2G1B,在健康组织的上皮细胞中高表达。在未发生和发生转移的原发性肿瘤中,与胰腺癌发生(如CECAM5、MUC1和MUC5AC)和转移(如EMP1、AQP5和VIM)相关的基因分别得到富集。在来自转移性病灶的肿瘤细胞中发现了可能促进转移的基因,包括S100A8、SMCG 和 CXCL14。他们通过基因集富集分析(GSVA)总结了这些差异表达基因的生物学功能,并富集为八类特征(图2g)。与脂质代谢、细胞间连接和免疫监视相关的信号在正常胰腺上皮细胞中富集,并从良性器官到恶性组织逐渐减少。癌基因通路、细胞周期、抗凋亡、糖酵解、上皮-间质转化和生物大分子合成的信号随着肿瘤恶性演变而增加。值得注意的是,与淋巴细胞和髓系细胞相关的免疫信号的减少凸显了肿瘤演变过程中免疫监视系统的功能障碍。此外,转移性肿瘤细胞表现出与原发性肿瘤细胞相似的免疫调控特征,表明转移部位的免疫微环境是由来自原发性肿瘤的肿瘤细胞塑造的(图2g)。

图2. 分析 PDAC 转移过程中上皮细胞的变化。
(a-b) UMAP 图显示上皮细胞的细胞类型和组织来源。(c) UMAP 图突出显示了从 Primary_NM、Primary_HM 和 HM 组织中分离的上皮细胞的组织来源。(d) UMAP图表示来自 Primary_NM、Primary_HM 和 HM 组织的上皮细胞的异常拷贝数变异 (CNV)分数。(e) 染色体图显示了 HD、Primary_NM、Primary_HM 和HM样本中上皮细胞在不同染色体上的 CNV 分数分布。(f) 热图列举了每种组织来源的上皮细胞的前 20 个 DEG。(g) 热图显示不同组织的上皮细胞之间差异富集的基因集。
03
PDAC转移过程中巨噬细胞的变化
共鉴定出19661个髓系细胞,并用UMAP图呈现。巨噬细胞(9970个细胞)、树突状细胞(1812个细胞)、中性粒细胞(5622个细胞)、肥大细胞(1074个细胞)和单核细胞(1383个细胞)由上述典型标记物定义。在来自各个组织来源的三个数据集中均大量观察到巨噬细胞和树突状细胞。单核细胞主要见于亨廷顿氏病和无转移的原发性肿瘤的活检中,肥大细胞几乎未见。
基于无监督聚类,巨噬细胞进一步分为三个群体(图3a)。C0 显示非转移性原发性病变优先模式(图3b-c)。脂质代谢相关基因,如APOE和APOC1,在 C0 中上调(图3d-f)。GSVA 特征分析证实了这一特征(图3g)。因此,他们将该群体定义为早期肿瘤相关巨噬细胞 (esTAM)。MDSC 标记基因(S100A8、S100A9和S100A12)是 C1 的代表性差异表达基因(图3d-f)。趋化性和细胞因子产生的特征在该群体中富集(图3g)。 MDSC 标记评分在该群体中始终突出,可将其定义为 MDSC 样巨噬细胞(图3h-i)。值得注意的是,C1 群体显示出转移性原发病灶优先模式(图3c),暗示其具有促转移功能。在 C2 群体中观察到补体相关基因(C1QA、C1QB和C1QC)(图3d-f),这也明确了典型的 TAM (cTAM) 标记(图3h-i)。
此外,他们分析了PDAC进化过程中中性粒细胞的特征。分离并聚类了不同组织来源的中性粒细胞,以便进行后续的DEG和功能富集分析。综合分析揭示了胰腺癌进展过程中中性粒细胞的动态功能进化。在HD组织中,中性粒细胞维持以细胞外基质组织和消化酶调节为特征的稳态维持功能。在转变为Primary_NM肿瘤后,这些细胞获得了促增殖能力以及适应性免疫调节能力。值得注意的是,Primary_HM肿瘤内的中性粒细胞表现出增强的炎症活化和凋亡启动表型。引人注目的是,HM中性粒细胞通过IL-10信号激活和趋化优势机制经历了深度免疫抑制重编程。这些阶段特异性的适应性突显了中性粒细胞在塑造肿瘤耐受性方面的功能可塑性,提示微环境驱动的重编程是转移能力的关键驱动因素。
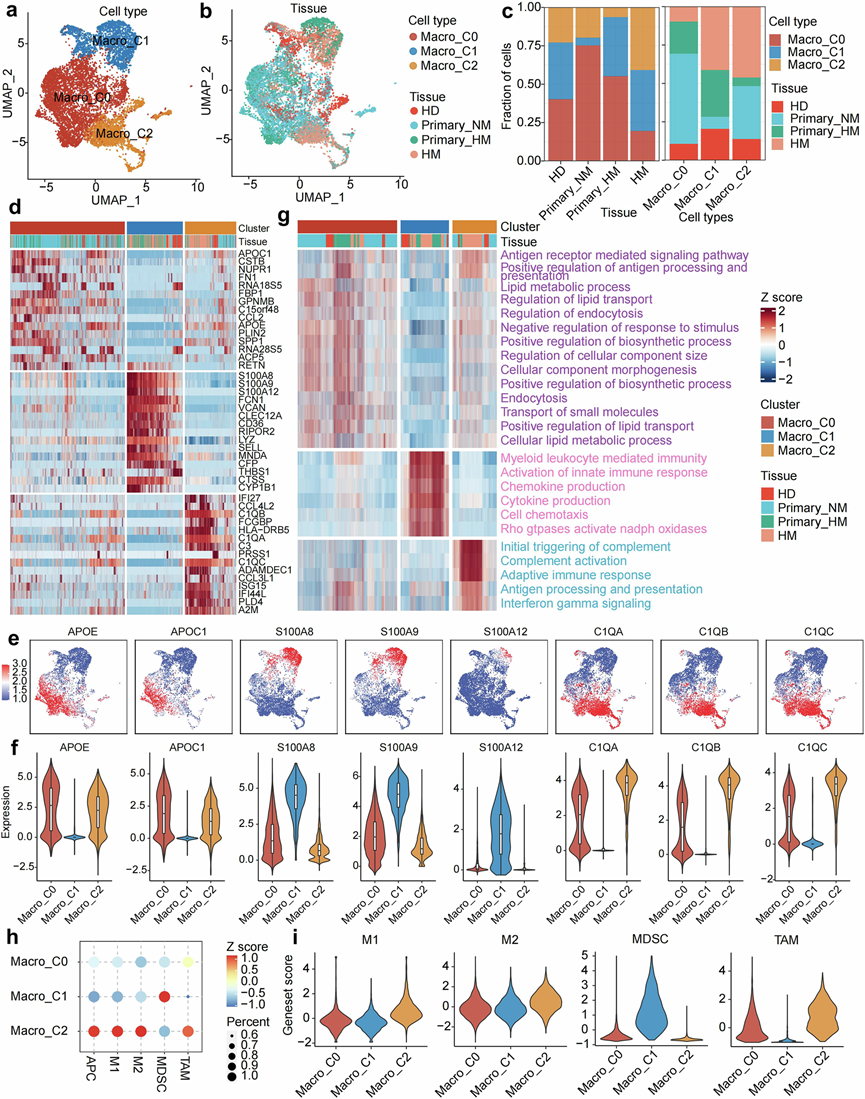
图3. PDAC 转移演变过程中巨噬细胞的改变。
(a) UMAP投影显示了来自所有活检的亚聚类巨噬细胞,细胞根据其细胞类型用颜色区分。(b) UMAP 图描绘了巨噬细胞的组织来源。(c) 条形图量化了队列 HD、Primary_NM、Primary_HM 和 HM 中每种巨噬细胞亚型的比例。(d) 显示了每种巨噬细胞亚型的前 15 个差异表达基因。(e) UMAP 图投射了已鉴定巨噬细胞亚型的标记基因表达。(f) 小提琴图描绘了每种巨噬细胞亚型的标记基因表达谱,显示了每个聚类内基因表达的变化。(g) 呈现了每种巨噬细胞亚型的差异富集基因集。(h) 气泡热图表示与每种细胞类型相对应的典型特征的得分。(i) 小提琴图显示每个亚型细胞的典型巨噬细胞特征。
04
PDAC转移的演变伴随DC的功能丧失
从上述每种组织中共鉴定出1812个树突状细胞(DC),并在UMAP图上自发聚类为5组(C0-C4)(图4a)。通过差异基因表达分析,对代表性基因进行表征,随后进行标签得分富集分析。总体而言,C0、C2、C3和C4组表现出明显的传统树突状细胞(cDC)特征,而C1组则表现出明显的浆细胞样树突状细胞(pDC)特征。代表性基因的详细消化表明,与2型常规树突状细胞(cDC2)、成熟树突状细胞(mDC)、1型常规树突状细胞(cDC1)和未成熟树突状细胞相关的基因分别在C0(CLEC10A,FCGR2B)、C2(CCL22、LAMP3、CCR7、CD80、CD83)、C3(CLEC9A、CADM1、CXR1)和C4(CD1A、CD207)中特异性上调(图4b-c)。而与pDC相关的基因,例如LIRA4和GZMB,在C1中上调。通过对DC亚型的典型标记基因的分析证实了这种细胞定义(图4c)。
当他们绘制每个DC亚群在总免疫细胞(CD45 +)中的比例时,他们注意到在肿瘤演变过程中cDC2群体(C0)显著减少(图4d)。为了阐明该功能群体丧失的潜在机制,他们通过两种独立的算法探索了这些DC的发育层次,即Velocyto和Monocle3,它们都显示了从未成熟DC到cDC2再到成熟DC的轨迹,这暗示了它们生命周期的路线图。这表明成熟DC(C2)可能代表这些细胞发育层次中的终末状态。实际上,与其他聚类相比,C2中的凋亡相关特征高度丰富(图4e)。然后他们关注mDC在肿瘤演变过程中经历细胞凋亡的原因。 CellPhoneDB 分析了从良性到恶性组织中各亚型树突状细胞 (DC) 与上皮细胞之间的分子相互作用。结果表明,在恶性转变过程中 ANXA1:FPR1/FPR3 相互作用表现出最显著且逐渐增加的趋势(图4f)。表达解剖表明,上皮细胞上的 ANXA1(而不是 DC 上的 FPR1/3) 从 HD 到非转移性原发性肿瘤再到转移性原发性肿瘤逐渐增加(图4g)。值得注意的是,在 TCGA PDAC 队列中,高 ANXA1 表达与较差的总生存期显著相关,进一步支持其作为胰腺癌预后生物标志物的潜在作用。此外,FPR1/3 主要分布在 C0、C2 和 C4 上。在这些聚类中,C0 的 FPR1/3 水平最高,这部分解决了肿瘤发展过程中群体的减少。为了验证 DC 的凋亡,他们对 HD、非转移性原发性肿瘤、转移性原发性肿瘤和 HM 病变的活检样本进行了多重免疫组织化学 (mIHC) 染色。结果表明,在肿瘤进展过程中,DC(CD11c +)的密度降低,并且它们经历进行性凋亡,这由裂解的 caspase 3 证明(图4h)。该过程伴随着上皮细胞(CK+)和 DC 中 ANXA1 的增加和 TNF-α 的减少。这些数据都表明,在恶性进展的过程中,肿瘤细胞的影响会导致树突状细胞功能丧失、数量减少。
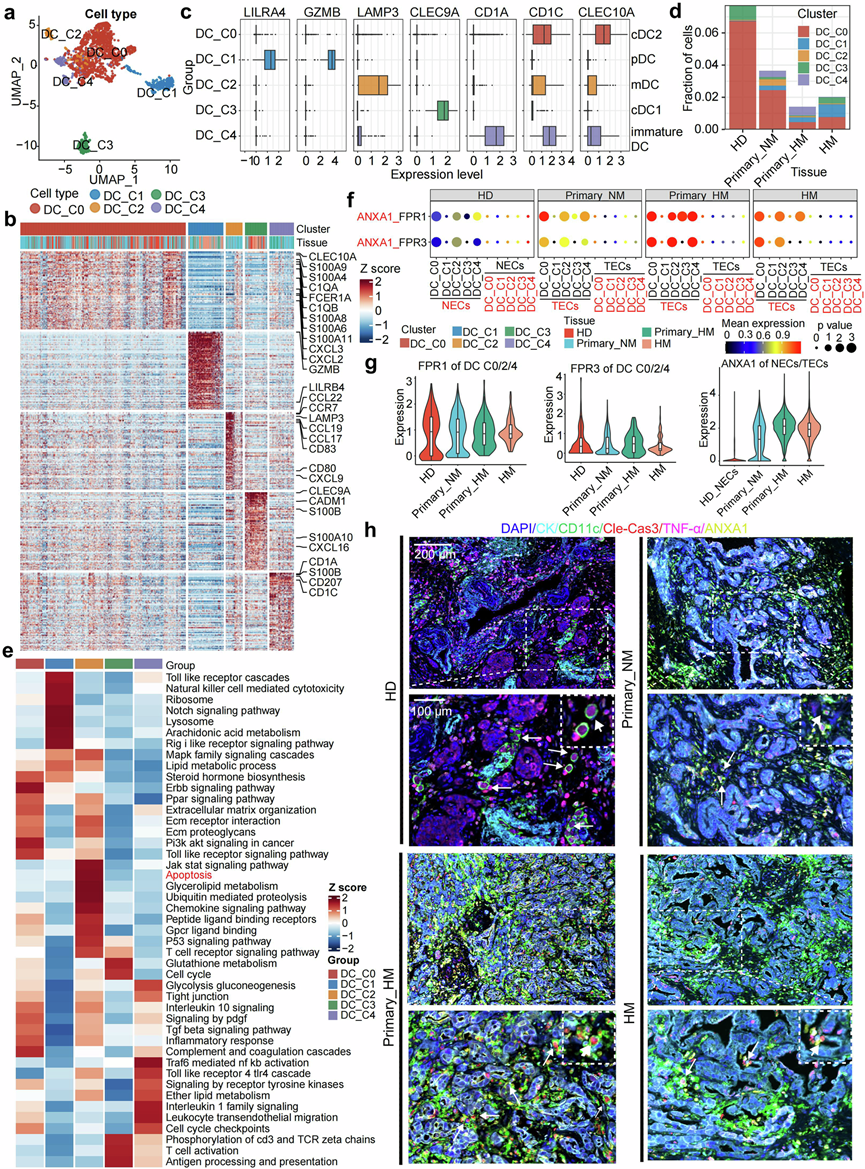
图4. PDAC 转移的演变伴随着树突状细胞 (DC) 的功能丧失。
(a) UMAP图表示来自所有活检的亚聚类树突状细胞 (DC),其中细胞根据细胞类型进行颜色编码以实现清晰区分。(b) 热图显示每个DC亚型的 DEG,其中突出显示代表性标记基因,颜色表示标准化的 z 分数。(c) 箱线图说明了标记基因在不同细胞类型中的表达。(d) 条形图显示免疫细胞群中每个 DC 亚型的比例。(e) 热图表示每个 DC 亚型的差异富集基因集。(f) 点图显示了不同组织中 TEC/NEC 和树突状细胞 (DC) 亚型之间配体-受体对(特别是 ANXA1_FPR1/2)的表达水平。(g) 小提琴图显示了不同组织中 cDC 上FPR1的表达水平(左)、cDC 上FPR3的表达水平(中)以及TEC/NEC 上ANXA1 的表达水平(右)。(h) HD组织、原发性 NM 肿瘤、原发性 HM 肿瘤和 HM 病变的 mIHC 染色代表性图像。
05
ANXA1 功能分析
研究团队试图探究 ANXA1 是否能够诱导DC细胞凋亡并影响 PDAC 免疫治疗的效率。首先,他们用不同剂量的 ANXA1 蛋白处理激活的骨髓来源树突状细胞 (BMDC),观察到体外细胞凋亡明显诱导(图5a-b)。该结果通过蛋白质印迹进一步证实(图5c-d)。结果显示,ANXA1 有效上调凋亡标志物 cleaved caspase-3 的表达,同时下调抗凋亡标志物 MCL-1 和 BCL-2。这些结果表明 ANXA1 诱导树突状细胞凋亡。
为了进一步验证ANXA1的体内功能,他们通过植入KPC细胞(分别在ANXA1表达水平和未改变ANXA1表达水平的情况下)建立了小鼠皮下和原位PDAC模型,随后用抗PD-1阻断抗体进行治疗。在皮下模型中,绘制了治疗期间的肿瘤生长曲线,并在治疗结束时记录了肿瘤重量(图5e-f)。结果表明,敲低ANXA1具有强效的抗肿瘤作用,而抗PD-1阻断抗体进一步增强了这种作用。相反,过表达ANXA1则略微加剧了肿瘤的生长。原位小鼠PDAC模型也证实了ANXA1敲低显著抑制肿瘤生长,而ANXA1过表达则促进肿瘤进展(图5g-h)。此外,ANXA1敲低可有效增强PD-1阻断剂在原位小鼠PDAC模型中的抗肿瘤作用。为了确定调控ANXA1的表达是否会调节细胞毒性T细胞和树突状细胞(DC)的浸润,他们通过免疫荧光法对CD8+ T细胞和CD11c+ DC进行了可视化(图5i-k)。与肿瘤曲线的结果一致,全切片成像的定量分析显示,ANXA1过表达导致CD8 + T细胞和CD11c+ DC的密度降低。相反,ANXA1敲低和抗PD-1治疗均显著增加了CD8+ T细胞和CD11c+ DC的密度。值得注意的是,PD-1阻断进一步增加了CD8+ T细胞和CD11c+ DC的密度。多参数流式细胞分析进一步验证了这一现象。肿瘤中的CD3+ T细胞、CD8 +细胞毒性T细胞(CTL,CD3+ CD8 +)、总树突状细胞(CD45+ CD11c +)和成熟树突状细胞(CD11c+ CD80+)均受到ANXA1敲低的持续刺激,而额外的PD-1阻断进一步增强了这种刺激。相反,ANXA1过表达导致这些免疫细胞群的浸润显著减少。有趣的是,他们发现ANXA1表达的变化并没有显著改变这些T细胞耗竭标志物(例如PD1、TIM3和CTLA4)的表达水平。在原位模型中,流式细胞分析和免疫荧光染色进一步验证了这些结果。流式细胞分析显示,ANXA1 敲低和抗 PD-1 治疗显著增强了 CD3+ T 细胞、CD8 +细胞毒性 T 细胞、CD11c+总树突状细胞和 CD11c+ CD80 +成熟树突状细胞的浸润,而 ANXA1 过表达则降低了它们的浸润。值得注意的是,PD-1 阻断进一步增加了 CD8 + T 细胞和 CD11c +树突状细胞的浸润,这表明抗 PD-1 治疗和 ANXA1 敲低协同促进了抗肿瘤免疫反应。CD8 和 CD11c 的免疫荧光染色进一步验证了这一现象。此外,在两种模型中,NK 细胞浸润均未受到 ANXA1 调节的显著影响。综上所述,肿瘤浸润 CD8+ T 细胞的数量与DC细胞的密度呈正相关,表明 ANXA1 诱导的 DC 功能障碍和随后的 DC 数量减少可能会阻碍抗肿瘤免疫反应。
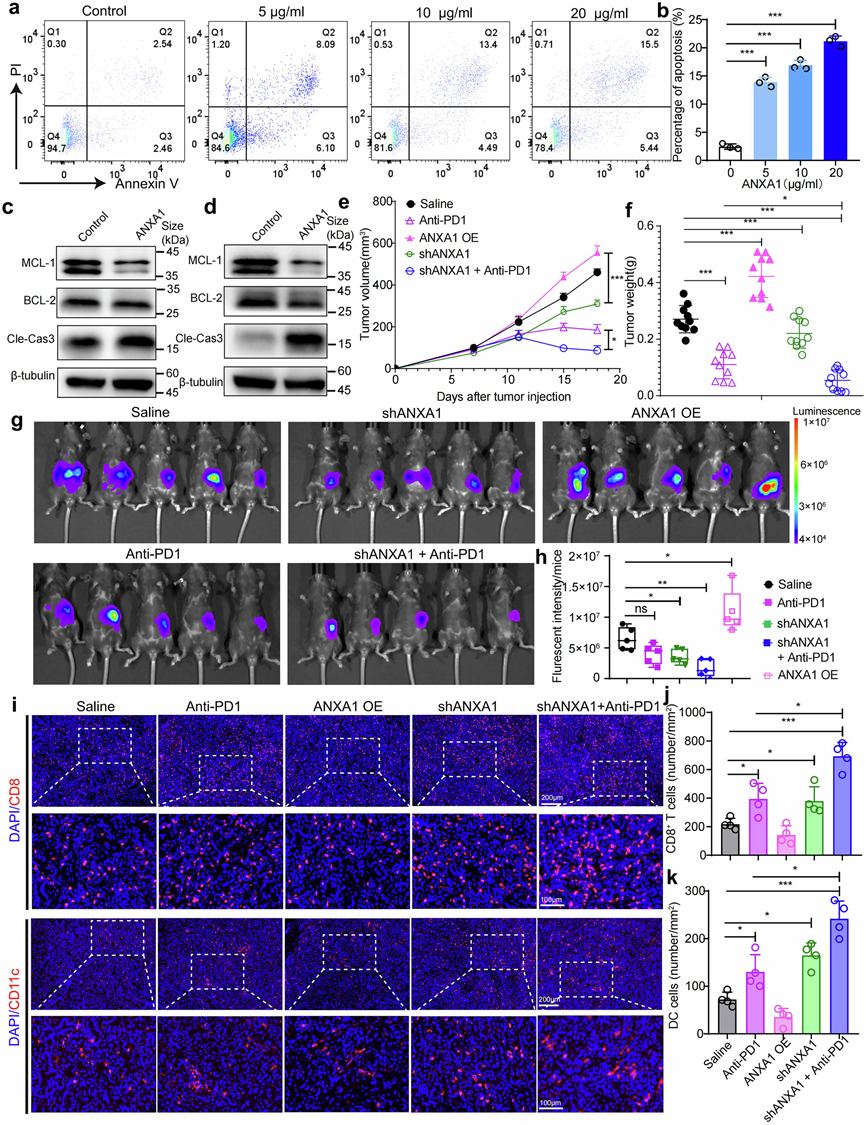
图5. 体外和体内验证 ANXA1 功能。
(a-b) 采用Annexin V-FITC/PI流式细胞分析评价指定剂量(0、5、10、20 μg/ml)ANXA1对BMDC细胞凋亡的影响,并对结果进行定量分析。(c-d) 在用 10 μg/ml ANXA1 处理 24 小时的BMDC和 DC2.4细胞中检测到指示凋亡途径活性的蛋白质,包括 MCL-1、BCL-2 和 cleaved caspase3。(e-f) 通过皮下注射 KPC 细胞(在操纵或不操纵 ANXA1 表达的情况下)建立 PDAC 异种移植模型。(g-h) 小鼠PDAC原位模型通过将过表达ANXA1、敲低ANXA1或空载体的荧光素酶标记的KPC细胞(KPC-Luc)注射到小鼠胰腺组织中建立。(i) CD8和CD11c的全玻片免疫荧光染色以评估T细胞和DC在皮下PDAC肿瘤中的浸润。(j-k) CD8+ T细胞和CD11c+ DC的密度定量。
06
PDAC进化过程中细胞毒性淋巴细胞的下调
理论上,如果没有DC的支持,细胞毒性淋巴细胞就无法完全激活。然后,他们通过 UMAP 图对 T 淋巴细胞和 NK 细胞进行分析(图6a-b)。总共呈现了 33059 个细胞,并根据其指示的典型标记基因将其定义为 CD8 Trm(ITGA1+,ITGAE+)、粘膜相关不变 T 细胞(MAIT)(KLRB1+,IL7R +)、GZMK CD8 效应细胞(EFF)(GZMK+,CCL5+)、GZMB CD8 EFF (GZMB +, GZLY +)、CD8 Ex (PDCD1+,LAG3+)、 Treg(FOXP3+, IL2RA+)、 CD4 记忆 T 细胞(LEF1 +,TCF7 +)、CD4 幼稚 T 细胞(CCR7 +, SEEL +)、NKT (CD3D+, KLRD1+)和 NK(CD3D -,KLRD1+)(图6c-d)。在每个起源组织和患者中都观察到了所有这些细胞类型的分布,这表明数据收集是全面的,并且不偏向任何特定的细胞类型或组织来源(图6e)。为了描绘 CD4+和 CD8 + T 细胞亚群之间的谱系关系,他们进行了区室特异性分析。对于 CD4 +细胞群,无监督聚类揭示了从 CD4 +记忆T 细胞向 Treg 的分化轨迹(图6f-g)。在 CD8+亚群中,轨迹推断确定了两条不同的路径:(1)细胞毒性分化轴,从幼稚到记忆再到终末分化的 GZMK 效应细胞,以及(2)耗竭途径,其中 GZMK+中间体转变为耗竭的 CD8+ T 细胞(图6h-i)。有趣的是,所有耗竭的CD8 +细胞都具有高水平的GZMB,而不是GZMK(图6d)。这种分歧凸显了细胞毒性效应细胞和耗竭细胞群体在个体发育上存在着显著差异。
在这些细胞中,MAIT 和 NKT 主要分布在肝转移病灶中(图6e)。其他亚型在所有组织来源中均有观察到。CD8+ EFF GZMK 和 CD8 + EFF GZMB 细胞是这些胰腺肿瘤中的主要 T 细胞类型。有趣的是,GZMK 和 GZMB 基因的表达显示出不同的模式,其中很大一部分细胞表达 GZMK 但不表达 GZMB,而较小一部分细胞表达 GZMB(图6d-j)。为了研究它们的功能,他们分别表征了代表性特征。一方面,GSVA 分析显示炎症、细胞周期、糖酵解和脂质代谢相关特征富集 CD8+ EFF GZMK 群体(图6k)。因此,与细胞因子(CXCR4、CXCR6、CCL3L1、CCL4L2、CXCR3)、细胞周期(DUSP2、DUSP4、DUSP1、FOSB、FOS)相关的基因在该群体中显著上调。另一方面,与免疫细胞介导的细胞毒性相关的特征在 CD8+ EFF GZMB 细胞中富集(图6l)。与此一致,与细胞毒性(FGFBP2、GNLY、GZMB、GZMH、NKG7、PRF1)、T 细胞活化(FCGR3A、KLRD1、KLRF1)和成熟(KLF2、CD52、ZEB2)相关的基因在该群体中上调。
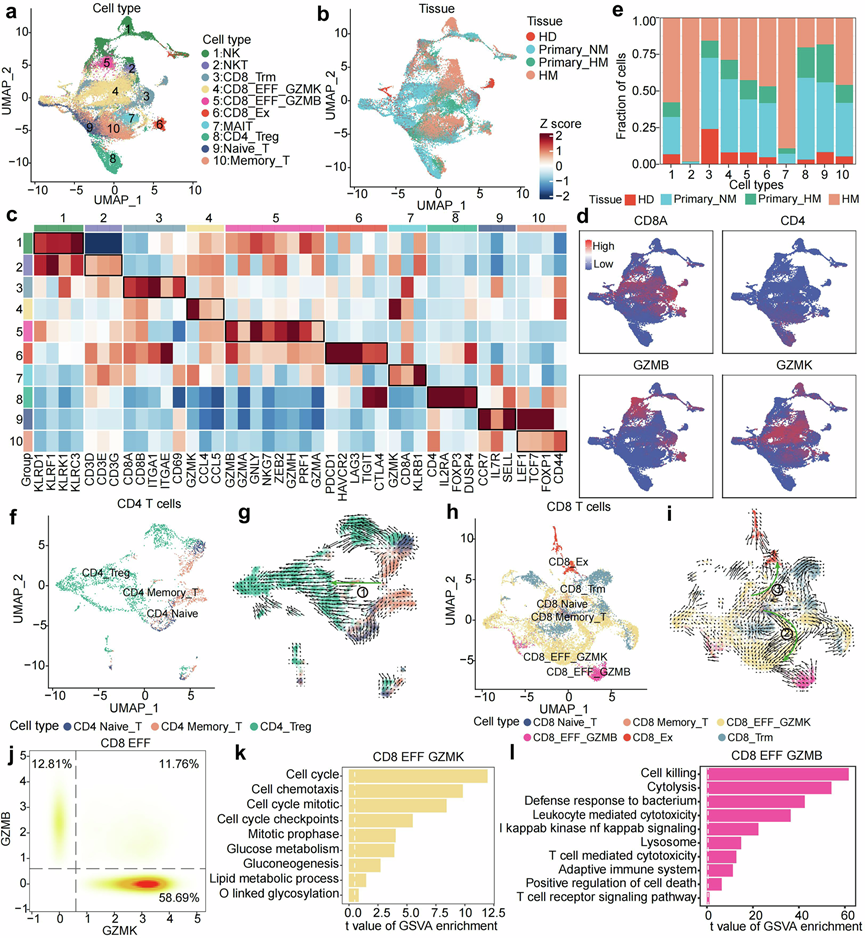
图6. PDAC 进化过程中细胞毒性淋巴细胞的下调。
(a) UMAP图描绘了所有活检样本中的亚聚类 T 淋巴细胞和 NK 细胞,并根据细胞类型对细胞进行颜色编码以便于清楚区分。(b) UMAP图说明了 T 淋巴细胞和 NK 细胞的组织来源。(c) 热图显示每种细胞类型特征性标记基因的表达模式。(d) UMAP图投射了指示细胞亚型的标记基因表达。(e) 条形图量化了 HD、Primary_NM、Primary_HM 和 HM 队列中 T 细胞亚型和 NK 细胞的比例。(f) UMAP投影说明了 CD4+T 细胞在 HD、Primary_NM 和 Primary_HM 组中的空间分布。(g) 通过 Velocyto 分析可视化 HD、Primary_NM 和 Primary_HM 中 CD4 + T 细胞亚型之间的细胞分化轨迹。(h) UMAP 可视化展示了HD、Primary_NM 和 Primary_HM 样本中CD8 + T 细胞的空间组织。(i) 基于 Velocyto 的 HD、Primary_NM 和 Primary_HM 中 CD8+ T 细胞亚型分化的轨迹映射。(j) 密度图描绘了 GZMK 和 GZMB 表达的双峰分布。(k) 条形图显示了CD8 EFF GZMK 细胞的富集基因集的 t 值,表明基因表达变化的重要性。(l) 条形图显示了CD8 EFF GZMB 细胞的富集基因集的 t 值,提供了差异表达的测量。
07
分析PDAC恶性转化过程中NK细胞的异质性
根据 DEG 和典型标记基因,共定义了 4057 个 NK 细胞,并将其分为 4 类:常规 NK(cNK、CX3CR1、FGFBP2、GZMB、GZMH)、应激反应 NK(strNK、HSPA1A、HSPA1B、HSPA6、HSPB1)、MHC-II 相关 NK(MHCII NK、HLA-DRA1、HLA-DQA1、HLA-DPB1、HLA-DQB1、HLA-DRAC)和组织驻留NK(trNK、CXCR6、CD160、GZMK、KLRB1)(图7a-c)。在 HD 组织、原发性肿瘤和 HM 病变中均观察到 cNK 和 strNK。而 MHC-II NK 和 TrNK 在 HM 中分布较多(图7d)。cNK 聚类中CX3CR1、FGFBP2、GZMB、GZMH等细胞毒相关基因表达水平较高。GSVA 分析显示,免疫相关的细胞杀伤特征在 cNK 中富集,暗示其具有内在的肿瘤免疫监视功能(图7e)。典型功能标记基因和富集评分进一步证实了 cNK 的细胞杀伤能力(图7f-g)。相反,trNK 表现出相对较低的细胞毒功能和炎症特征。有趣的是,在该人群中观察到高水平的免疫检查点基因 TIGIT(图7f),这与先前从肝细胞癌(HCC)图谱研究得出的结论一致。MHC-II NK细胞是trNK细胞群的一个亚群,其与抗原呈递相关的基因表达显著上调,包括HLA-DRA、HLA-DQA1、HLA-DPB1、HLA-DQB1和HLA-DR(图7c)。该基因表达谱表明MHCII NK细胞在免疫系统中可能发挥与抗原呈递细胞类似的作用。
值得注意的是,在所有 NK 细胞中,一组表现出显著应激相关热休克基因和特征的 NK 细胞鉴定为 strNK。与应激反应 T 细胞(Tstr)(鉴定为与免疫疗法抗性相关的 T 细胞群)一样,strNK 在肿瘤微环境中表现出不同的特性和功能。首先,应激反应相关基因(HSPA1A、HSPA1B、HSPA6、HSPB1)作为该细胞类型的标记基因,高表达(图7c)。其次,增殖相关基因和特征在 strNK 群中高度上调(图7e)。第三,strNK 群表现出负免疫调节和免疫抑制的特征(图7e)。有趣的是,一些典型的Treg相关基如FOXP3、CYLA4、ICOS和TNFRSF18在strNK中高表达(图7f)。此外,相对较低的细胞杀伤评分和下调的细胞毒性相关基因表明它们的细胞溶解功能缺陷(图7f-g)。简而言之,strNK是一类具有高增殖特性和负向免疫调节,但细胞溶解功能较弱的NK。使用TCGA数据集和独立队列(GSE183795)对PDAC患者进行进一步的临床生存分析表明,高水平的strNK意味着较差的预后(图7h-i)。此外,在cNK,trNK和strNK之间观察到免疫检查点的相对排他性分布(图7f)。在功能性cNK细胞中,KLRC1 (NKG2A)水平较低,这部分解释了莫那珠单抗(抗NKG2A单克隆抗体,NCT02459301、NCT02331875、NCT02557516)目前在晚期PDAC治疗中临床失败的原因。相反,免疫检查点分子KIR2DL1、KIR3DL1和CD226在cNK细胞中水平相对较高(图7f),提示它们可能作为治疗靶点。轨迹分析表明,cNK、trNK和strNK呈现出相对“独立”的发育路线图,暗示其细胞命运不同(图7j)。进一步考察各群体在其生命周期发育过程中的代表性功能(图7k)。结果显示,细胞杀伤、抗原呈递和炎症反应得分分别在cNK、trNK和strNK中高度富集。
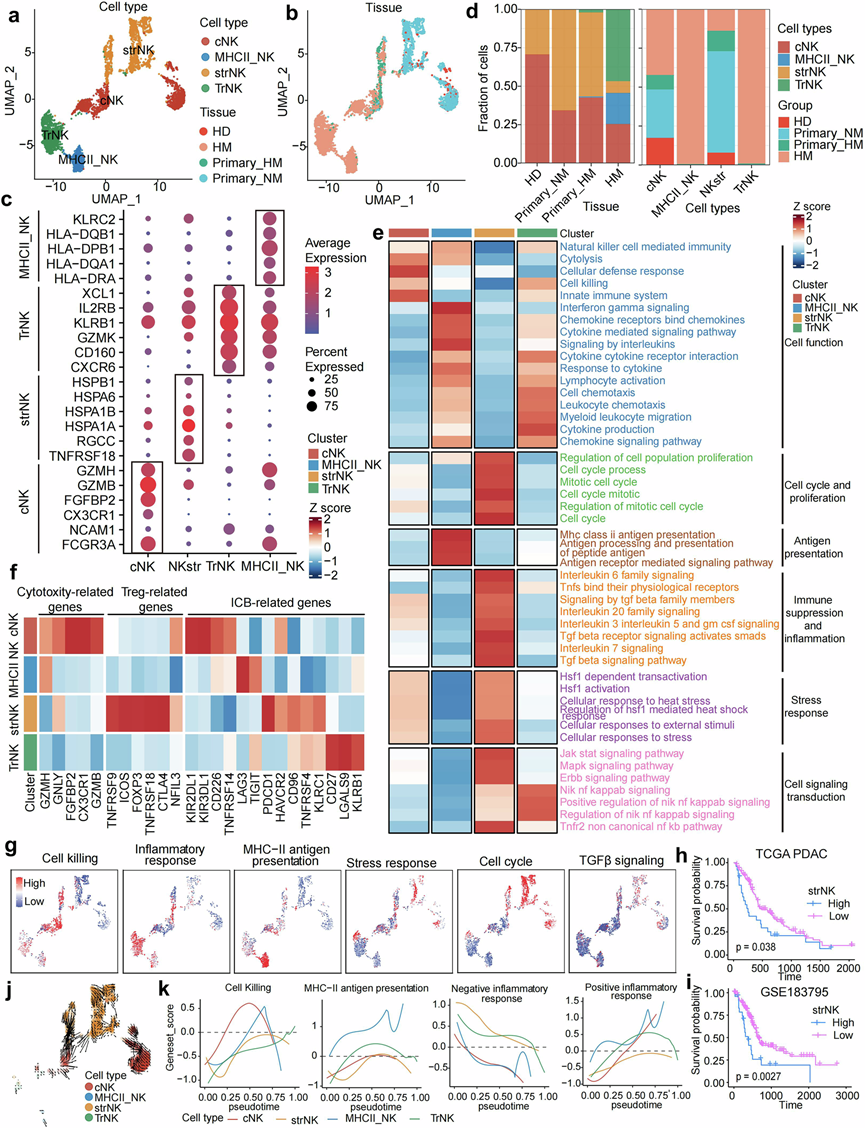
图7. NK 细胞亚型分析和功能分析。
(a) UMAP图显示来自所有活检的亚聚类 NK 细胞,其中细胞根据细胞类型进行颜色编码。(b) UMAP 图展示了 NK 细胞的组织来源,显示了其在各种组织类型中的分布。(c) 点图展示了与每种 NK 细胞类型相对应的典型标记基因的表达。(d) 条形图显示了队列HD、Primary_NM、Primary_HM 和 HM 中 NK 细胞亚型的比例。(e) 热图显示了 NK 细胞亚型之间差异富集的基因集,按功能分类。(f) 该图显示了每种 NK 细胞亚型中细胞毒性相关基因、Treg 相关基因和 ICB 相关基因的平均表达水平。(g) 典型基因集的富集得分投影在指示细胞亚型的 UMAP 图上,颜色从蓝色到红色编码以表示基因集表达的强度。(h-i)生存分析。(j) NK细胞的分化轨迹,其中细胞根据其相应的细胞类型进行颜色编码。(k) 二维图描绘了NK细胞亚型中四种代表性基因特征沿推断的伪时间的表达得分,提供了基因表达动态的时间视图。
+ + + + + + + + + + +
结 论
本研究通过分析来自 51 种组织(包括健康胰腺组织、非转移性 PDAC 原发性肿瘤、转移性原发性肿瘤和患者匹配的肝转移瘤)的 132115 个单细胞转录组,探究了 PDAC 肿瘤微环境的动态变化。本研究仔细表征了各细胞类型之间的细胞比例、生物功能和相互作用。在肿瘤发展过程中,上皮细胞 7 号和 20 号染色体上发现了指示恶性程度的异常拷贝数变异。本研究还观察到主要基因从生理性向胰腺癌发生和转移的生物功能转变。上皮细胞和免疫细胞的组合分析表明,在恶性转化过程中,免疫监视功能逐渐丧失。通过深入研究细胞间相互作用,本研究揭示了肿瘤细胞通过分子对ANXA1-FPR1/3逐渐引发DC凋亡的过程。因此,细胞毒性CD8+ T细胞的激活和浸润逐渐受到抑制。值得注意的是,本研究揭示了一种新的应激反应NK细胞亚型,其特征是增殖旺盛、细胞溶解能力下降以及负向免疫调节。值得一提的是,strNK细胞的存在与PDAC患者不良预后相关,提示其可能具有促肿瘤功能。总之,本项研究结果不仅揭示了PDAC肿瘤发展过程中逐步逃避免疫监视的复杂机制,还为通过增强DC功能来抑制恶性转化提供了一种潜在的策略。
+ + + + +



 English
English


