文献解读|Signal Transduct Target Ther(52.7):帕金森病伴快速眼动睡眠行为障碍患者的代谢组学和蛋白质组学特征独特
✦ +
+
论文ID
原名:Distinct metabolomic and proteomic signatures in Parkinson’s disease patients with REM sleep behavior disorder
译名:帕金森病伴快速眼动睡眠行为障碍患者的代谢组学和蛋白质组学特征独特
期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
发表时间:2026.03.30
DOI号:10.1038/s41392-026-02613-8
背 景
快速眼动睡眠行为障碍(RBD)是帕金森病(PD)最特异的前驱症状,影响40-50%的PD患者。伴有RBD的帕金森病(RBD-PD)是一种临床上更具侵袭性的亚型,其特征是更严重的运动和非运动症状、显著的自主神经功能障碍以及疾病进展加速;然而,其潜在的发病机制仍不甚明了。
实验设计
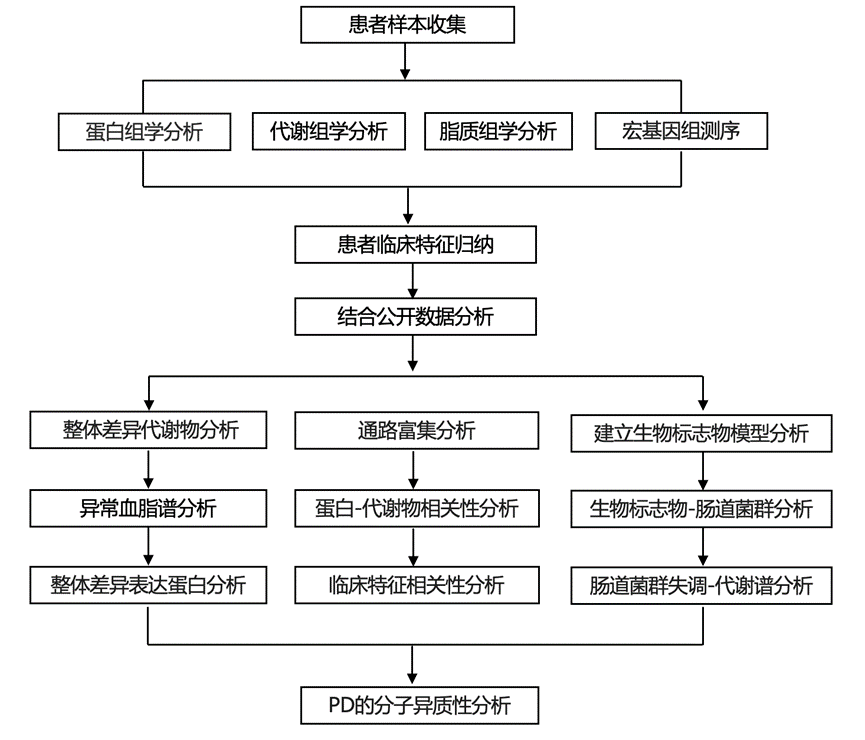
结 果
01
参与者群体和研究设计
在本研究中,研究团队首先招募了伴有和不伴有RBD的PD患者,以及匹配的健康对照组。所有参与者的血浆样本均通过液相色谱-质谱联用(LC-MS)和气相色谱-质谱联用(GC-MS)平台进行代谢组学和脂质组学分析(图1a-b),通过整合代谢组学和蛋白质组学数据,他们鉴定了两种PD亚型共有和亚型特异性的分子特征(图1c),还研究了这些代谢物与肠道菌群失调之间的关系(图1d)。本研究是迄今为止对这些帕金森病亚型进行的最大规模的比较分析。通过揭示亚型特异性的分子和生物学通路,旨在识别候选生物标志物,并阐明可能导致帕金森病临床病程异质性的不同分子机制。
本研究纳入了来自两个独立队列的424名参与者,包括135名RBD-PD患者、127名非RBD-PD患者、30名iRBD患者和132名健康对照者(Ctrl)。在探索阶段(队列1),采用已验证的问卷(RBDQ-HK,RBD诊断临界值为18分)评估RBD状态。非RBD-PD组、RBD-PD组和健康对照者组这三组在年龄和性别分布方面具有可比性。与非 RBD-PD 患者相比,RBD-PD 患者的运动障碍明显更严重,睡眠质量更差,白天嗜睡更严重。
在验证阶段,他们纳入了一个独立的队列(队列 2),该队列由四个年龄和性别匹配的组组成(30 例 RBD-PD 患者、14 例非 RBD-PD 患者、30 例特发性RBD(iRBD) 患者和 30 例对照组受试者,所有受试者均接受了金标准多导睡眠检测 (vPSG) 评估以确认 RBD 状态。正如预期的那样,虽然非 RBD-PD 患者和 RBD-PD 患者的日间嗜睡程度似乎相当(表1),但RBD-PD 组和 iRBD 组的 RBD 症状均比非 RBD-PD 组更为严重。
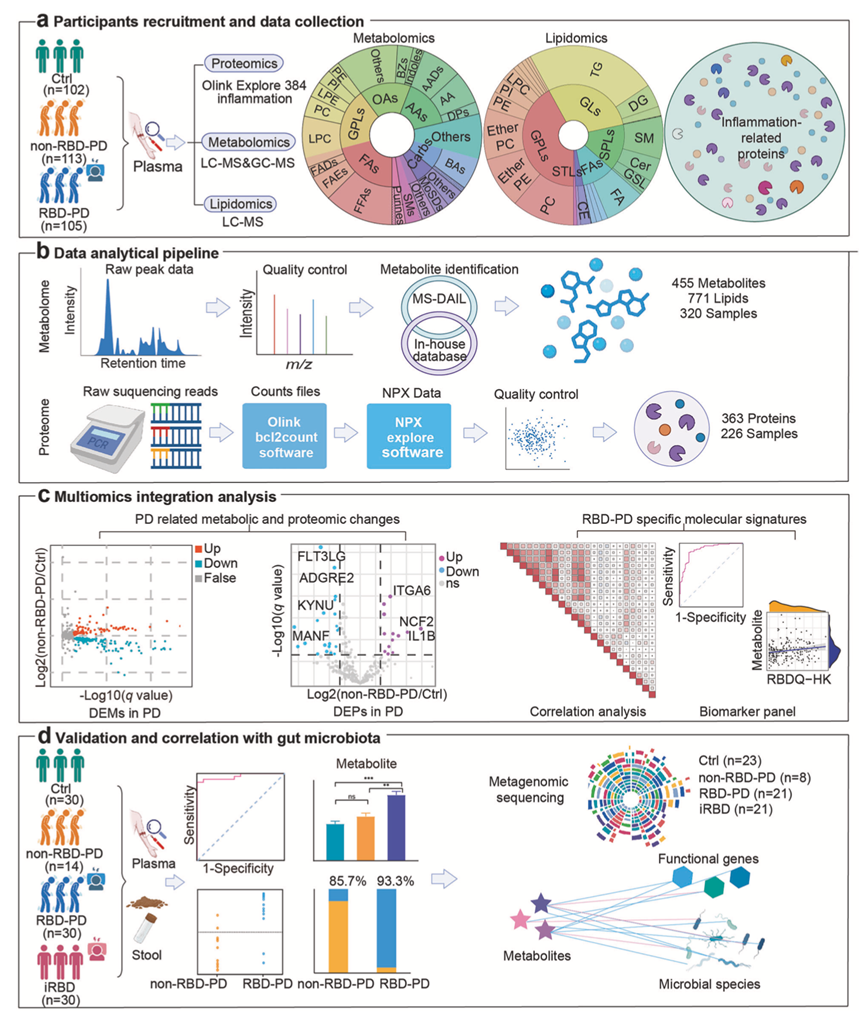
图1. 血浆代谢组学和蛋白质组学整合分析流程图。
(a) 采用多平台代谢组学和蛋白质组学方法,分析快速眼动睡眠行为障碍(RBD)帕金森病(PD)患者、非RBD-PD患者和健康对照组的血浆分子变化。(b) 共注释了455种极性代谢物、771种脂质以及363种炎症和免疫相关蛋白。(c) 通过整合多组学数据,鉴定了帕金森病相关的代谢和蛋白质组学变化以及RBD-PD特异性分子特征。(d) 在一个独立的临床队列中验证RBD-PD特异性代谢变化后,整合了宏基因组学数据,以鉴定与这些特定的微生物来源代谢物相关的肠道微生物和功能基因。
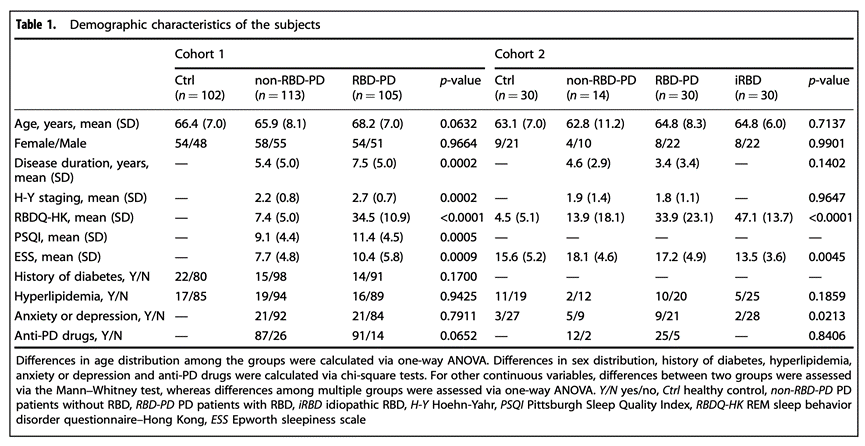
表1. 受试者的基本人口统计学特征
02
帕金森病患者的代谢特征
他们首先进行了正交偏最小二乘判别分析(OPLS-DA),以区分三个患者组的整体代谢谱变化。LC-MS代谢组学数据表明,各组之间存在不同的代谢特征,提示存在亚型特异性代谢模式(图2a)。此外,与组间差异相比,年龄和性别分层的影响甚微。GC-MS代谢组学和脂质组学数据集也显示出一致的改变。
为了鉴定各组间代谢特征的差异,他们首先通过逻辑回归校正了混杂因素(例如糖尿病、高脂血症、焦虑和抑郁以及抗帕金森病药物的使用)。然后,采用Mann-Whitney U检验对两组进行比较,并对所有p值进行多重比较校正。结果显示,与对照组相比,非RBD-PD患者中共有203种代谢物发生显著改变,其中154种(75.9%)在RBD-PD患者中也存在异常(图2b),表明两种亚型存在共同的核心病理生理紊乱。在203个差异表达代谢物(DEM)中,与对照组相比,非RBD-PD患者中79个代谢物[例如乳酸、天冬氨酸和溶血磷脂酰胆碱(LPC)]的水平升高,而124个代谢物(例如甘露糖和酰基肉碱)的水平降低(图2c)。这些失调的代谢物涉及多种化学类别,包括脂肪酰基、氨基酸、有机酸、碳水化合物和胆汁酸,其中99.0%的代谢物在两种PD亚型中均表现出一致的方向性改变(图2d-g)。
除了证实之前报道的改变[包括脂肪酸 (FFA) 和酰基肉碱的消耗、蛋白水解毒素(苯乙酰谷氨酰胺、对甲酚葡糖醛酸苷)的积累以及胆汁酸的升高]之外,多平台分析还揭示了PD患者能量代谢的显著紊乱,其特征是糖酵解和三羧酸 (TCA) 循环中间体(乳酸、丙酮酸、苹果酸、富马酸和α-酮戊二酸的积累(图2e)以及碳水化合物代谢物(甘露糖、核糖、山梨糖、鼠李糖等的消耗(图2g)。此外,他们检测到色氨酸衍生的吲哚衍生物(吲哚乳酸,ILA;3-吲哚丙烯酸,IAcrA;3-吲哚乙酸,IAA)显著减少(图2e),且在两个帕金森病亚组中氨基酸代谢均受到干扰(图2f)。这些发现表明,与RBD状态无关的病理生理机制是保守的。
全面的脂质组学分析揭示了非RBD-PD患者中392种差异表达的脂质种类(DEL),其中353种(90.1%)在RBD-PD患者中也发生了类似的改变(图2h)。值得注意的是,PD患者中大多数脂质含量降低,而选择性升高则局限于特定亚类,包括LPC、溶血磷脂酰乙醇胺(LPE)、磷脂酰乙醇胺(PE)、烷基酰基溶血磷脂酰胆碱(LPC O)以及几种鞘脂(图2i)。类别水平分析显示,PD患者中总LPC和LPC O水平升高,而其他脂质类别的总量则显著降低。后续按酰基链饱和度分层分析显示,增加的成分仅限于饱和磷脂酰乙醇胺(PE)、饱和和单不饱和LPC/溶血磷脂酰乙醇胺(LPC/LPE)以及多不饱和LPC。此外,PD患者体内多不饱和游离脂肪酸(FFA)与单不饱和和饱和FFA的比值显著降低。这些结果表明,异常的脂质重塑和去饱和酶活性受损在PD各亚型中均有发生。
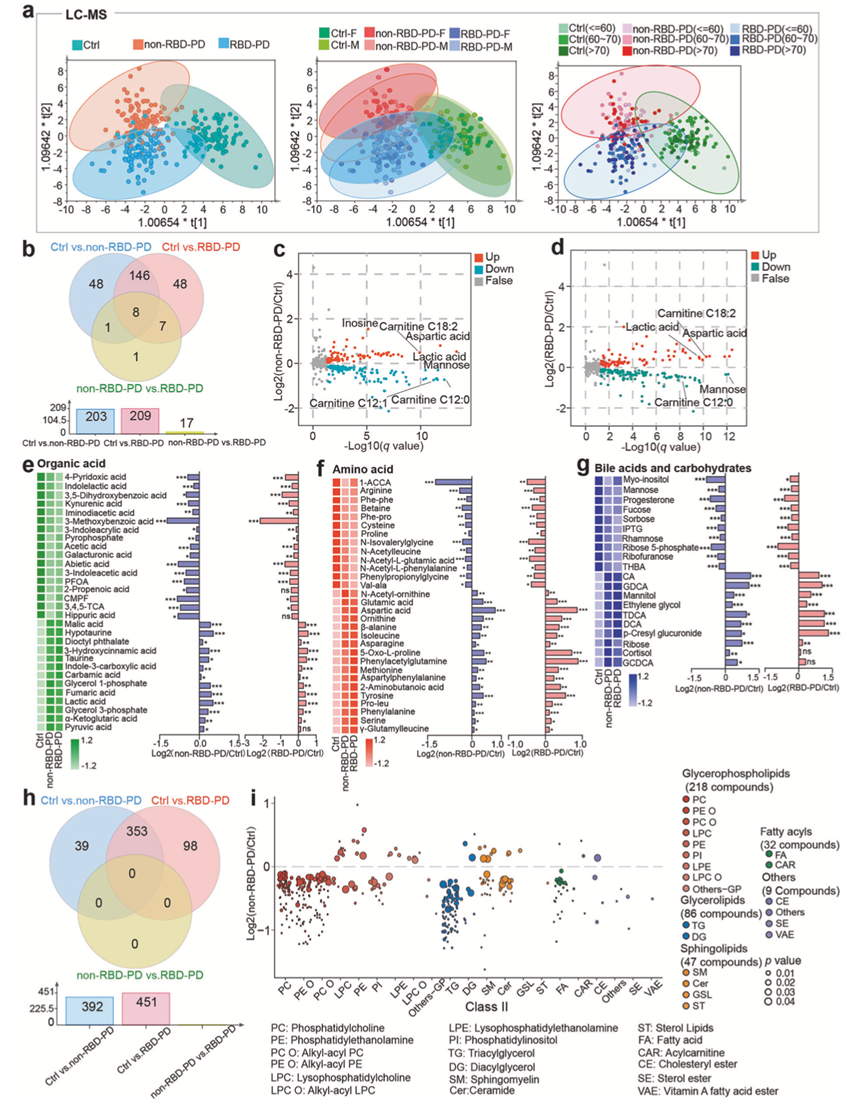
图2. PD中差异表达代谢物和脂质的鉴定。
(a) 基于液相色谱-质谱(LC-MS)代谢谱,构建了两个帕金森病亚组和对照组个体的正交偏最小二乘判别分析(OPLS-DA)模型。(b) 维恩图展示了组间比较中鉴定出的差异表达代谢物的数量。(c) 火山图展示了非RBD PD患者与对照组相比,差异表达代谢物的显著变化。(d) 火山图展示了RBD帕金森病组与对照组相比,差异表达代谢物的显著变化。(e-g) 非RBD-PD相关差异表达代谢物(例如有机酸、氨基酸、胆汁酸和碳水化合物)的相对浓度热图。(h) 维恩图,显示组间比较中差异脂质的数量。(i) 按化学类别分类的非RBD-PD患者差异脂质的气泡图。
03
PD患者的免疫炎症蛋白改变
鉴于神经炎症在PD中发挥的重要作用,他们对队列 1 中的 226 个样本中的 21 种血浆炎症蛋白进行了分析。OPLS-DA 得分图清晰地显示了各组之间的分离(图3a)。在非 RBD-PD 患者中鉴定出 34 个差异表达蛋白(DEP)(21 个下调,13 个上调)(图3b)。
在两种帕金森病亚型中均观察到促炎细胞因子白细胞介素-1β (IL-1β) 和氧化应激相关蛋白中性粒细胞胞质因子2 (NCF2) 的表达升高(图3b-c)。此外,他们发现免疫相关蛋白的表达显著降低,包括FLT3LG(fms相关酪氨酸激酶3配体)、ADGRE2(黏附G蛋白偶联受体E2)和CLEC4A(C型凝集素结构域家族4成员A),这些蛋白此前未见于帕金森病的报道。神经保护因子MANF(中脑星形胶质细胞衍生神经营养因子)在两种帕金森病亚型中也显著降低。两种调节色氨酸分解代谢和糖酵解通量的酶,KYNU(犬尿氨酸酶)和PKLR(丙酮酸激酶),也表现出明显的失调。Pearson相关性分析表明,KYNU与色氨酸代谢物(犬尿酸,KYNA;IAcrA和ILA)(图3d-f)之间存在显著的正相关性,PKLR与能量相关代谢物(苹果酸、α-酮戊二酸和乳酸)之间也存在显著的正相关性(图3g-i)。
功能注释显示,这些差异表达蛋白主要富集于多种生物过程,包括免疫应答、RNA聚合酶II对转录的正调控以及细胞黏附(图3j-k)。这些差异表达蛋白主要定位于质膜、细胞膜和细胞外区域。KEGG通路富集分析突显了细胞因子-细胞因子受体相互作用以及关键信号级联,包括PI3K-Akt、IL-17、NF-κB、MAPK和TNF信号通路,揭示了帕金森病中炎症和免疫应答的广泛激活(图3l)。
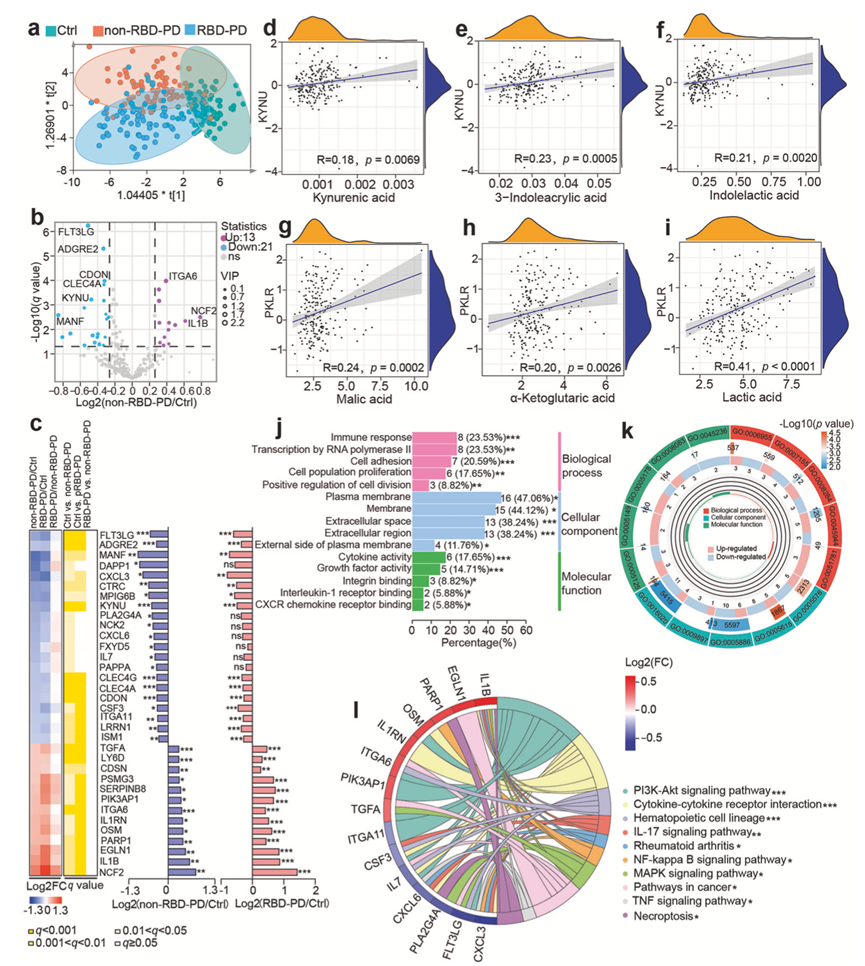
图3. 差异表达蛋白的鉴定。
(a) 基于蛋白质组学特征,构建了两个PD亚组和健康对照者的OPLS-DA模型。(b) 火山图可视化了非RBD-PD患者与健康对照者之间的差异表达蛋白。(c) 热图可视化了34种PD差异表达蛋白在三个组别中的表达情况。(d-f) KYNU与代谢物(犬尿酸、3-吲哚丙烯酸和吲哚乳酸)之间的相关性分析。(g-i) PKLR与代谢物(苹果酸、α-酮戊二酸和乳酸)之间的相关性分析。(j-k) GO分析。(l) DEP中前9个富集的KEGG通路。
04
RBD-PD患者与非RBD-PD患者的代谢差异
为了研究亚型异质性,他们比较了RBD-PD患者和非RBD-PD患者的代谢谱。采用逻辑回归分析,校正了潜在的混杂因素,包括糖尿病史、高脂血症、焦虑/抑郁状态和抗帕金森病药物治疗,结果显示有110种DEM(图4a)。Mann-Whitney U检验鉴定出90种代谢物(图4b),其中74种在两种方法中均有发现(图4c-d)。与非RBD-PD患者和健康对照组相比,RBD-PD患者的极性代谢物(包括氨基酸、有机酸和次级胆汁酸)的改变更为显著(图4d)。相反,非RBD-PD患者的脂质代谢紊乱更为严重(图4c)。为了全面分析与RBD-PD相关的代谢通路,他们重点关注了呈现渐进性变化的代谢物(图4d),这些代谢物主要参与氨基酸代谢和叶酸途径的单碳库(图4e)。与非RBD-PD患者相比,RBD-PD患者体内蛋氨酸、高丝氨酸、苏氨酸和5-氧代脯氨酸显著积累,而甘氨酸水平显著降低。此外,RBD-PD患者体内还检测到肠道菌群来源的代谢物显著富集,包括次级胆汁酸、2-苯乙酰胺、2-羟基喹啉、对甲酚、对甲酚硫酸酯、对甲酚葡糖醛酸苷和苯乙酰谷氨酰胺(图4f)。此外,RBD-PD患者的乙酰化氨基酸(N-乙酰-L-谷氨酸,NAcGlu;N-乙酰-L-苯丙氨酸,NAcPhe)和色氨酸衍生的ILA水平显著降低。经多重比较校正后,仍有17种代谢物发生显著变化(图4g),主要为芳香族氨基酸(ArAA)衍生的肠道菌群代谢物。
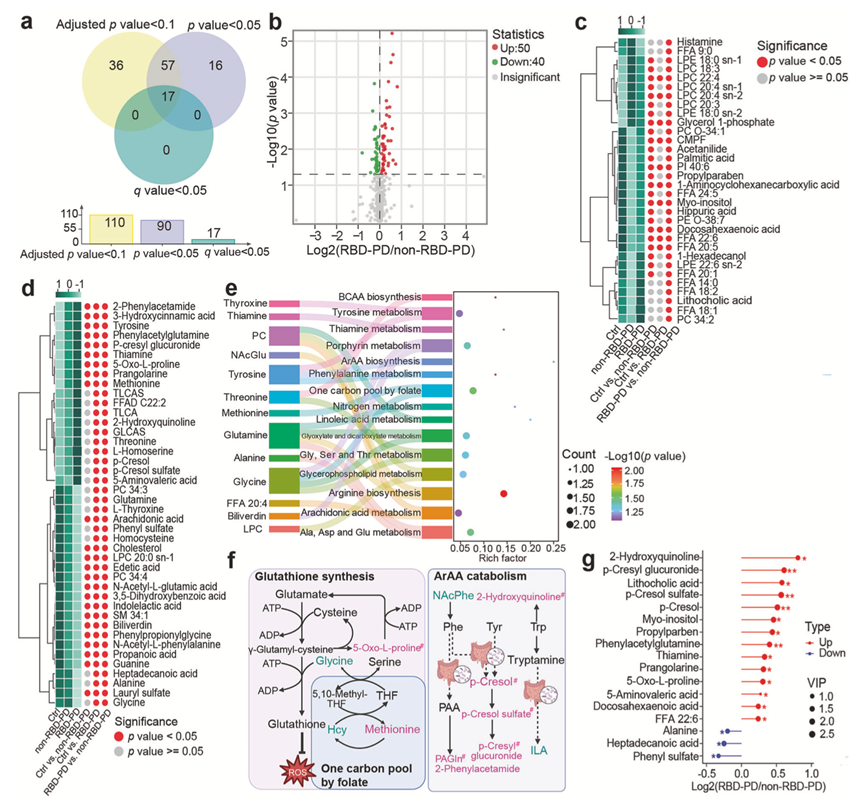
图4. RBD-PD 患者与非 RBD-PD 患者的代谢差异。
(a) 组间比较中与 RBD-PD 相关的DEM的 Venn 图。(b) 火山图可视化 RBD-PD 患者与非 RBD-PD 患者相比的DEM。(c) 热图显示对照组、非 RBD-PD 患者和 RBD-PD 患者中浓度变化呈 V 形或倒 V 形的代谢物。(d) 热图显示对照组、非 RBD-PD 患者和 RBD-PD 患者中浓度变化呈线性的差异表达代谢物。(e) 通路富集分析。(f) 与 RBD-PD 相关的特定代谢通路。(g) 最显著DEM。
05
RBD-PD患者与非RBD-PD患者的蛋白质组学差异
在校正混杂因素和进行单变量分析后,他们鉴定出24个可区分RBD-PD患者和非RBD-PD患者的候选蛋白(图5a)。然而,在进行多重比较校正后,这些蛋白均不再具有统计学意义。鉴于本研究的探索性性质,他们进行了GO分析,结果表明这些蛋白参与先天免疫反应、炎症反应中细胞因子产生的正向调控以及IL-12产生的正向调控。这些DEP主要定位于细胞外空间,并主要参与蛋白结合活动(图5b)。通路分析显示关键通路显著富集,包括PIP3激活AKT信号通路、免疫系统、免疫系统中的细胞因子信号通路以及细胞应激反应(图5c)。此外,这些蛋白质之间存在很强的相关性,特别是 TGFA、NCF2、EGLN1、PIK3AP1、PSMG3、DNPH1、SIT1、SERPINB8 和 PKLR 之间(图5d)。
为了进一步探究RBD-PD患者蛋白质组和代谢组改变之间的相互作用,通过Pearson相关性分析,将这些DEP与图4g中所示的最显著改变的代谢物进行关联。肠道菌群来源的代谢物(对甲酚、对甲酚硫酸盐、对甲酚葡糖苷酸和苯乙酰谷氨酰胺)的水平与关键蛋白的表达高度相关,这些关键蛋白包括神经炎症相关标志物CCL11(嗜酸性粒细胞趋化因子)、肠道炎症相关蛋白SPINK4(丝氨酸蛋白酶抑制剂Kazal型4)、氧化应激相关蛋白NCF2以及信号蛋白TGFA(转化生长因子α原)和WNT9A(Wnt-9a蛋白)。相反,丙氨酸与这些蛋白呈显著负相关(图5e)。
他们进一步研究了RBD-PD相关代谢物/蛋白与患者临床特征之间的相关性,发现十七烷酸水平与RBDQ-HK评分呈显著负相关。相反,2-羟基喹啉、对甲酚、对甲酚硫酸酯、对甲酚葡糖醛酸苷、苯乙酰谷氨酰胺和5-氧代-L-脯氨酸的水平与RBDQ-HK评分和年龄均呈显著正相关(图5f)。与代谢结果类似,SPINK4、CCL11 和 WNT9A 等蛋白的表达水平也与病程和年龄显著相关(图5g)。此外,CD6(T 细胞分化抗原 CD6)和 PKLR 等蛋白的表达与 RBDQ-HK 评分呈正相关,表明它们可能与 RBD 相关合并症有关。值得注意的是,NCF2 和 SERPINB8(丝氨酸蛋白酶抑制剂 B8)等蛋白与 ESS 评分呈正相关,表明它们可能在睡眠障碍的发病机制中发挥作用。
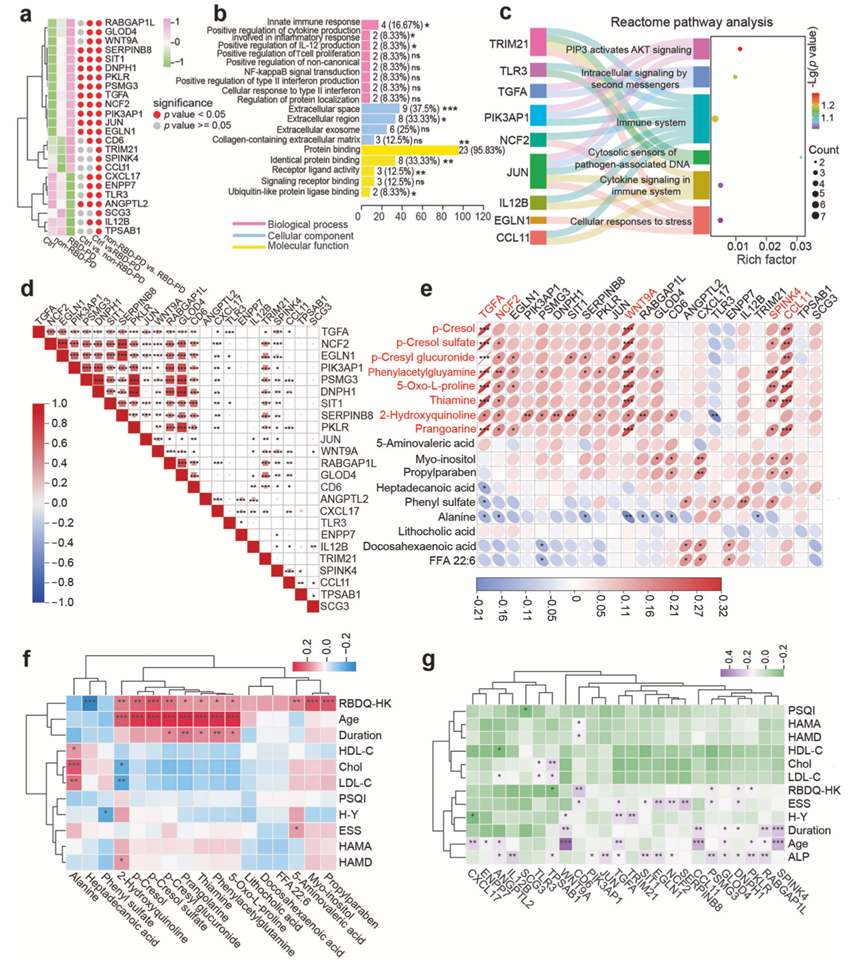
图5. RBD-PD 患者与非 RBD-PD 患者的蛋白质组学差异。
(a) 三组间DEP的相对浓度变化,以及 RBD 患者与非 RBD 患者之间组间比较的统计学意义。(b) GO分析。(c) 通路富集分析。(d) 对 24 个 RBD-PD 相关 DEP 进行 Pearson 相关性分析。(e) 对 RBD-PD 患者中 24 个 DEP 与 17 个DEM进行 Pearson 相关性分析。(f) RBD-PD患者前17个DEM与患者临床特征的Pearson相关性分析。(g) RBD-PD相关24个DEP与患者临床特征的Pearson相关性分析。
06
用于区分帕金森病亚型的生物标志物鉴定
他们采用了一种包含随机森林(RF)和二元逻辑回归(BLR)的两阶段流程来鉴定PD亚型鉴别的候选生物标志物。首先,他们使用在RBD-PD中表现出渐进性变化的42种代谢物构建了一个RF分类模型(图4d)。通过999次运行的平均准确率下降值(MDA)和平均基尼系数下降值(MDG)来判断每个特征在区分两种亚型中的重要性。随后,他们鉴定出RF排名前30的代谢物(图6a-b)。他们采用前向逐步选择算法,筛选出一个由9种代谢物组成的最优预测模型,这些代谢物包括对甲酚硫酸盐、甘氨酸、5-氨基戊酸、苏氨酸、N-乙酰-L-谷氨酸、十七烷酸、蛋氨酸、丙氨酸和普兰戈拉林。对该代谢物组合进行受试者工作特征(ROC)曲线分析,结果显示其曲线下面积(AUC)为0.826,能够区分RBD-PD患者和非RBD-PD患者,灵敏度为74.3%,特异性为81.4%。两种亚型的预测准确率分别为80.5%和74.3%(图6c-e)。此外,他们评估了该小组在区分 RBD-PD 患者和对照组方面的性能,结果显示 AUC 为 0.905,灵敏度为 88.6%,特异性为 75.5%。对对照组和 RBD-PD 患者的预测准确率分别为 78.4% 和 82.9%(图6f-h)。
为了获得模型预测性能的稳健且无偏估计,他们进行了迭代式留组交叉验证分析。经过1000次交叉验证后,该生物标志物组合在区分帕金森病亚型方面的平均AUC为0.787,平均灵敏度为74.0%,特异性为69.9%;在区分RBD-PD患者和对照组方面,平均AUC为0.873(灵敏度为76.7%,特异性为79.7%)。此外,该组合中的六种代谢物(不包括5-氨基戊酸、苏氨酸和甘氨酸)与RBD-PD相关的DEP显著相关(图5e,图6i),八种代谢物(不包括丙氨酸)与临床睡眠参数,特别是RBDQ-HK评分显著相关(图5f,图6j)。
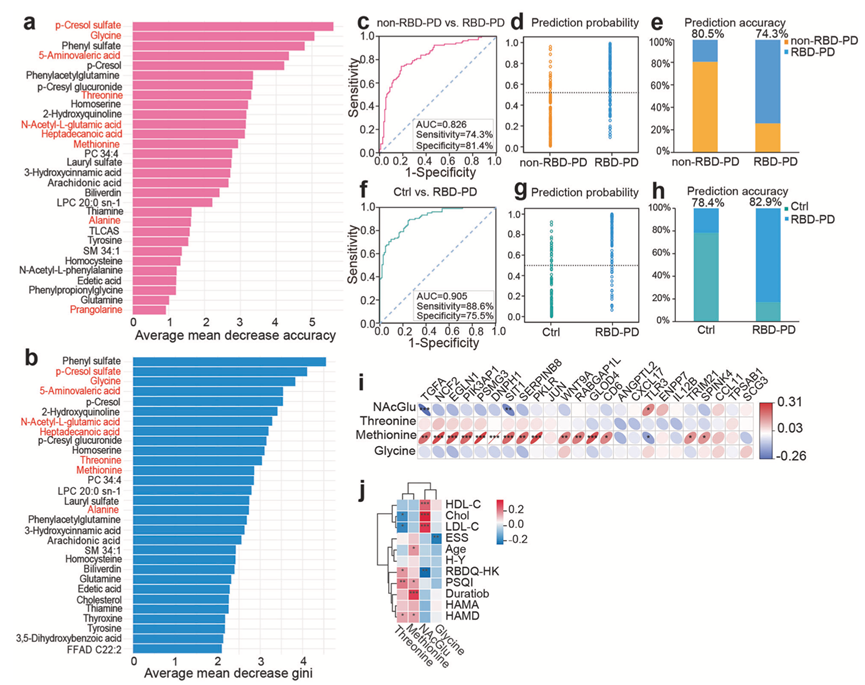
图6. 建立生物标志物模型以区分RBD-PD患者和非RBD-PD患者。
(a) 随机森林识别的前30个特征的平均准确率下降值。(b) 随机森林鉴定的前30个特征的平均基尼系数下降值。(c) ROC曲线评估生物标志物模型区分两种PD临床亚型的性能。(d-e) 分类模型区分两种临床亚型的预测概率和预测准确率。(f) ROC曲线评估分类模型区分RBD-PD患者和对照组个体的性能。(g-h) 分类模型区分RBD-PD患者和对照组个体的预测概率和预测准确率。(i) 代谢物水平与 24 种DEP水平之间的 Pearson 相关性。(j) 代谢物水平与临床参数之间的 Pearson 相关性。
07
在独立队列中进行验证
在由经vPSG确诊的非RBD-PD、RBD-PD或iRBD患者以及健康对照组组成的独立临床队列(队列2)中,从队列1中鉴定的17种主要代谢物中有10种表现出一致的趋势。值得注意的是,其中5种代谢物,包括对甲酚、对甲酚硫酸盐、对甲酚葡糖醛酸苷、苯乙酰谷氨酰胺和5-氧代-L-脯氨酸,在RBD-PD和iRBD患者中均显著升高(图7a-b)。
随后,他们在队列 2 中评估了 9 种代谢物模型,该模型在区分 RBD-PD 患者和非 RBD-PD 患者方面表现出色,AUC 为 0.967(灵敏度 90.0%,特异性 100%),预测准确率分别为 85.7%(非 RBD-PD 患者)和 93.3%(RBD-PD 患者)(图7c-e)。在区分 RBD-PD 患者和对照组时,该模型的 AUC 为 0.801(灵敏度 73.3%,特异性 76.7%),预测准确率分别为 76.7%(对照组)和 73.3%(RBD-PD 组)(图7f-h)。
此外,他们对队列 2 中的 73 名参与者进行了宏基因组测序,首先鉴定了在 RBD-PD 组和 iRBD 组中丰度差异显著的前 16 种微生物。相关性分析表明,这些微生物的相对丰度与关键 RBD-PD 代谢物的水平显著相关。这一点在Lactobacillus crispatus、未培养的Pseudoflavonifractor sp.、Marasmitruncus massiliensis、Flintibacter muris、Clostridiales bacterium GWC2_40_7和Paenibacillus flagellatus等菌种中尤为明显(图7i)。此外,他们还鉴定了在 RBD-PD 组和 iRBD 组中均显著失调的前 38 个功能基因。值得注意的是,这些关键代谢物与 K21556(malR,CRP/FNR 家族转录调节因子)和 K01181(xynA,内切-1,4-β-木聚糖酶)呈显著负相关,而 K21556 和 K01181 在 RBD-PD 和 iRBD 中均显著下调。相反,代谢物与参与 ATP 结合盒转运(K02031、K02032)、肽和氨基酸降解(K01426、K18123 和 K01269)以及黏液降解(K01628、K01207 和 K01820)的功能基因之间存在显著正相关(图7j)。
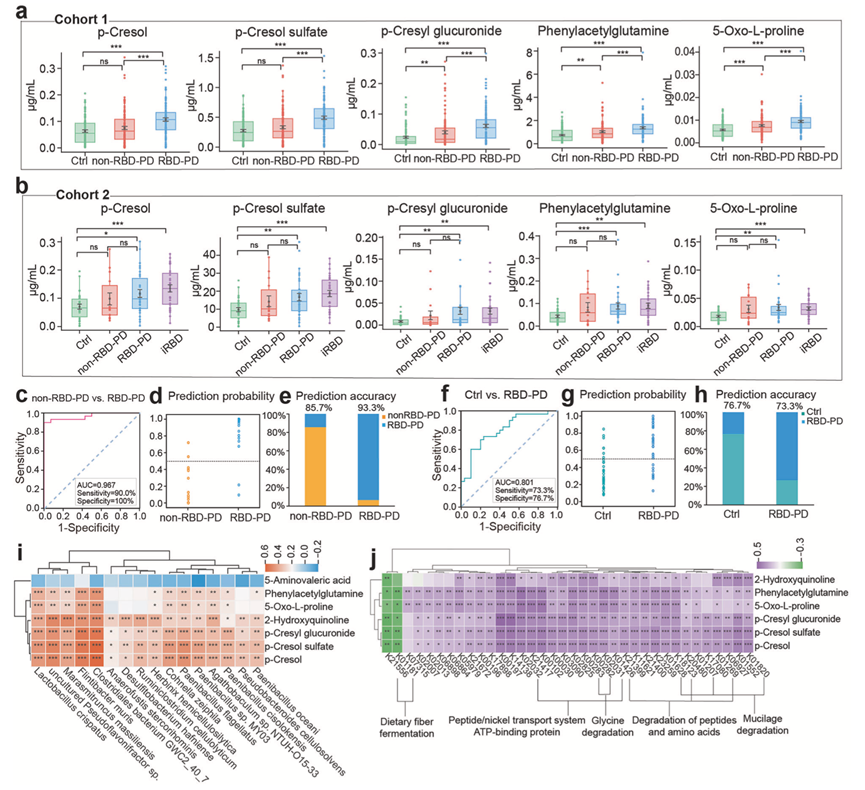
图7. 生物标志物验证及其与肠道菌群的相关性。
(a-b) 箱线图显示队列 1 和队列 2 中各组代谢物的相对浓度。(c) ROC 曲线评估生物标志物模型在队列 2 中区分两种临床亚型的性能。(d-e) 分类模型在队列 2 中区分两种临床亚型的预测概率和预测准确率。(f) ROC 曲线评估分类模型在队列 2 中区分 RBD-PD 和对照组的性能。(g-h) 分类模型在队列 2 中区分 RBD-PD 和对照组的预测概率和预测准确率。(i) 代谢物水平与前 16 种显著改变的微生物物种丰度之间的 Spearman 相关性分析。(j) 代谢物水平与前38个显著改变的功能基因丰度之间的Spearman相关性分析。
+ + + + + + + + + + +
结 论
本研究整合了多平台代谢组学和蛋白质组学以及精准的临床表型分析,旨在揭示不同PD亚型患者血浆中的分子特征。PD患者表现出显著的代谢重编程,其特征是能量代谢从三羧酸循环转向糖酵解、尿素循环失调和脂质重塑,以及涉及PI3K-Akt、IL-17、NF-κB、MAPK和TNF信号通路的炎症和免疫反应的广泛激活。值得注意的是,RBD-PD亚组表现出独特的代谢紊乱,其特征是肠道菌群来源的有毒芳香族氨基酸代谢产物的积累。重要的是,这些改变也见于iRBD患者,后者代表了PD的前驱期。通过整合宏基因组学数据,进一步揭示了RBD-PD和iRBD中的肠道菌群失调导致功能性转变,从膳食纤维发酵转向增强蛋白质、芳香族氨基酸、甘氨酸和肠道黏蛋白聚糖的降解。这种代谢重编程与氧化应激加剧、神经炎症和病理进展加速相关。这些发现阐明了PD的分子异质性,并强调肠道菌群驱动的功能障碍是iRBD和RBD-PD两种亚型的关键致病因素。
+ + + + +



 English
English


