文献解读|Cancer Cell(44.5):抗原呈递癌相关成纤维细胞微环境的单细胞分辨率空间分析
✦ +
+
论文ID
原名:Single-cell resolution spatial analysis of antigen-presenting cancer-associated fibroblast niches
译名:抗原呈递癌相关成纤维细胞微环境的单细胞分辨率空间分析
期刊:Cancer Cell
影响因子:44.5
发表时间:2025.09.25
DOI号:10.1016/j.ccell.2025.09.001
背 景
成纤维细胞是间充质细胞,对维持组织完整性、调节炎症反应和纤维化以及促进伤口修复至关重要。通常将癌症描述为一种永不愈合的伤口,这使得成纤维细胞成为肿瘤微环境的主要组成部分。在此背景下,它们发挥着多种功能,包括合成和修饰细胞外基质、与癌细胞进行复杂的信号传导以及与浸润的免疫细胞相互作用。因此,癌症相关成纤维细胞(CAF)已成为改善癌症治疗的理想靶点。然而,CAF的多样性和可塑性给开发有效的 CAF 靶向疗法带来了巨大挑战。单细胞转录组分析(scRNA-seq)技术显著增进了大众对成纤维细胞异质性的理解,揭示了在健康和病变组织中具有特定功能的不同成纤维细胞亚型。许多 CAF 群体已在不同类型的癌症中发现。然而,由于跨组织比较研究数量有限以及 CAF 命名法不一致,CAF亚型之间的谱系关系仍然知之甚少。根据分子特征,CAFs在表型上可分为三大亚型:炎症性CAF(iCAF)、肌成纤维细胞性CAF(myCAF)和抗原呈递CAF(apCAF),目前apCAF 仍然是 CAF 亚型中最不为人所知和表征最不明确的亚型。
实验设计
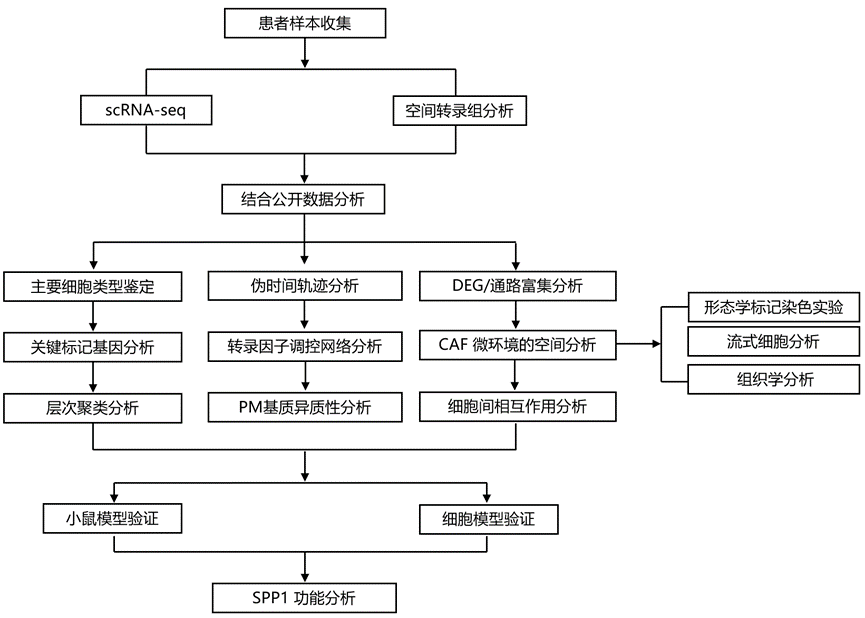
结 果
01
CAF表型在各种癌症类型中均保守存在
为了全面表征人类癌症中的apCAF,研究团队首先收集了来自13个不同器官[包括膀胱癌(BLCA)、乳腺癌(BRCA)、宫颈癌(CESC)、结直肠癌(COLO)、食管癌(ESCC)、肾癌(ccRCC)、肝癌(HCC)、肺癌(NSCLC)、卵巢癌(OV)、胰腺癌(PDAC)、腹膜癌(PM)、前列腺癌(PRAD)、皮肤癌(BCC/SCC)和胃癌(STAD)]的人类肿瘤及其相关正常组织的scRNA-seq数据集。经过批次效应校正和整合聚类后,构建了一个高质量的scRNA-seq图谱,包含532个样本和超过250万个细胞(图1A)。主要细胞类型通过不同的特征进行鉴定:上皮细胞、T细胞和NK细胞、成纤维细胞样细胞、髓系细胞、内皮细胞、浆细胞、B细胞和肥大细胞(图1A)。与其他癌症类型相比,PDAC、PM和OV中成纤维细胞样细胞的比例相对较高(图1B),但这可能反映了不同研究中组织处理方案的差异。他们使用标记基因COL1A1、COL1A2和COL3A1提取成纤维细胞样细胞,揭示了13个不同的细胞聚类(图1C-F)。虽然所有细胞聚类均表达COL1A2,但细胞聚类01、04和12(c01、c04、c12)缺乏泛成纤维细胞标志物PDGFRA和LUM(图1D)。相反,c01表达周细胞标志物(RGS5、MCAM、CSPG4),而c04和c12则表达平滑肌细胞(SMC)标志物(MYH11、PLN)(图1D-E),其余细胞聚类代表了不同组织中的成纤维细胞。
根据细胞特征和信号通路,成纤维细胞可分为6个主要亚型:iCAF(c09、c10)、myCAF(c03、c08)、apCAF(c05、c06)、稳态样CAF(sslCAF)(c02、c07)、神经元CAF(c11)和增殖性CAF(c13)。iCAF表达炎症基因(CXCL2、CXCL8、IL6),并富集白细胞介素/趋化因子/NF-κB信号通路和缺氧特征(图1D-F)。myCAF表达POSTN和MMP11,并激活细胞外基质和Hedgehog信号通路(c03以LRRC15特征标记,c08以PLAT特征标记)(图1D-1F)。相反,他们发现常见的活化CAF标志物ACTA2和FAP并非myCAF特异性标志物。他们发现了两个稳定的apCAF聚类(c05和c06),它们均表达HLA II类基因(CD74、HLA-DRA和HLA-DPA1)并具有抗原呈递功能。其中,c05表达SRGN、CD37和C1Q基因,而c06表达CD24和SERPINA1(图1D-E)。sslCAF表达普遍存在的驻留成纤维细胞标志物DPT和CD34,其中c02还表达祖细胞标志物PI16,可能是iCAF和myCAF的祖细胞(图1D-E)。两个较小的聚类c11 显示出神经元特征(DGL2、PIEZO2),而 c13 则具有增殖性(MKI67)(图1E)。TGFβ 信号在 c03 myCAF、c07 sslCAF、c11 神经元CAF和SMC中最高(图1F)。
层次聚类分析显示,sslCAF、iCAF和 myCAF属于同一分支,而apCAF则形成一个独立的分支,提示它们具有不同的祖细胞起源(图 1G)。虽然比例存在差异,但CAF亚型在不同癌症类型中出人意料地保守,唯一的例外是HGF高表达的 c09 iCAF,它们在皮肤癌和卵巢癌中富集(图1H)。比较正常组织和肿瘤中各成纤维细胞聚类的相对百分比变化,发现LRRC15+ myCAF(c03)、两种 apCAF 亚型 (c05, c06)、神经元 CAF和增殖性CAF在肿瘤中增加,而稳态样成纤维细胞 (c02, c07) 和炎症成纤维细胞 (c09, c10) 则相对减少(图 1I)。与正常组织成纤维细胞相比,肿瘤中的成纤维细胞普遍表现出肌成纤维细胞和抗原呈递特征增加,炎症特征降低(图1J)。
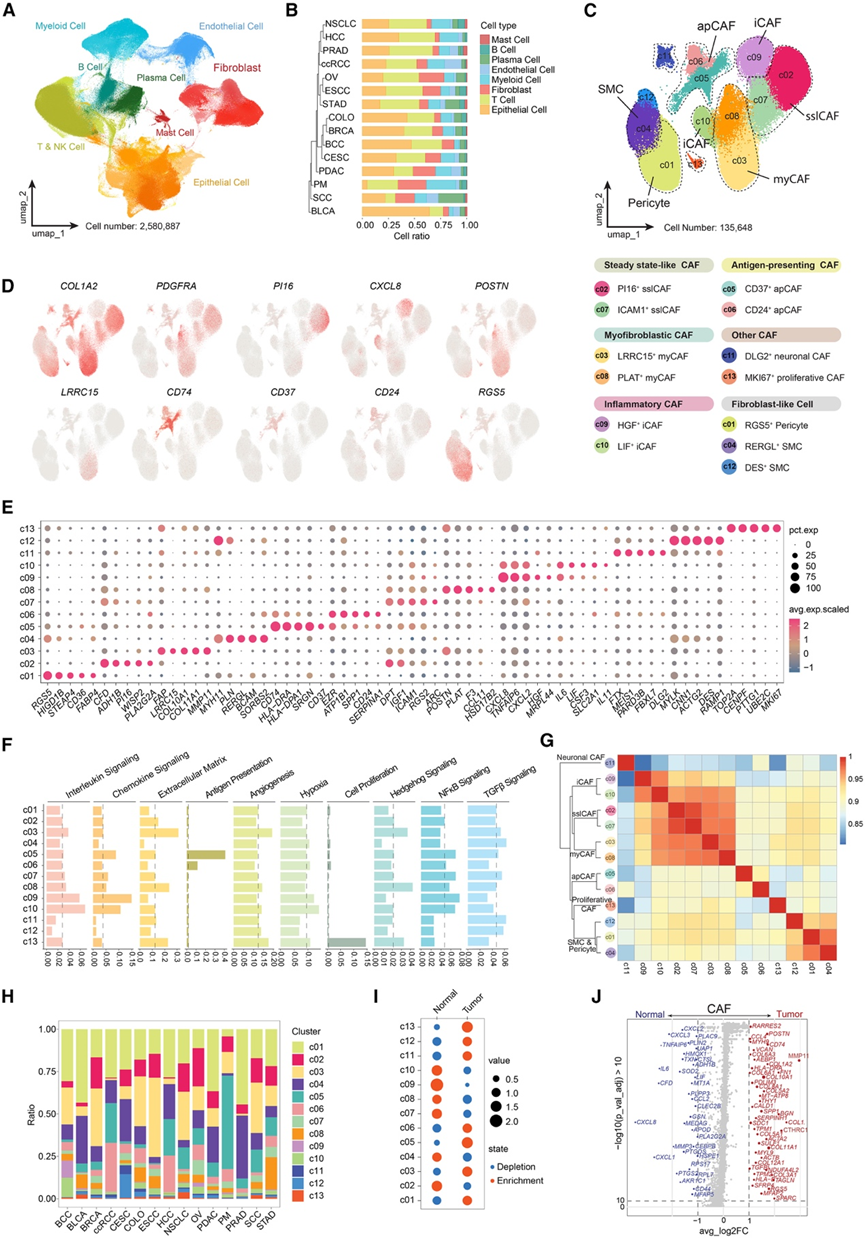
图1. CAF亚型的跨组织比较。
(A) 15 种组织和肿瘤类型的整合 scRNA-seq 图谱的 UMAP。(B) 按癌症类型划分的主要细胞类型比例。(C) 成纤维细胞聚类的 UMAP 显示 13 个 CAF 亚群。(D) 关键标记基因分析。(E) 气泡热图显示了成纤维细胞群体中特征基因的表达模式。(F) CAF 聚类的分子特征评分。(G) 热图显示了 CAF 子集之间的成对 Pearson 相关性,高度相似的 CAF 子集聚成相邻的模块。(H) 按癌症类型划分的 CAF 人口百分比。(I) 正常组织和肿瘤组织中成纤维细胞亚群的细胞丰度。(J) 将来自scRNA-seq的所有CAF亚群分为正常组和肿瘤组。
02
鉴定出两种不同的抗原呈递癌相关成纤维细胞群
为了进一步探究两种apCAF细胞群的起源和分子特征,他们从图谱中提取了c05和c06,并对这些细胞进行了重新聚类,结果显示存在两个不同的细胞群,每个细胞群包含4个亚聚类(图2A)。其中一个细胞群(聚类0和3)具有间皮样特征,以间皮基因(MSLN、UPK3B、KRT19)为标志(图2B)。此外,该细胞群还表达CD24,这是是一种近期报道的固有免疫检查点基因,参与细胞干性和分化的调控(图S1F)。这些数据与之前的研究结果一致,证实了apCAF的间皮起源。相比之下,他们发现另一个apCAF细胞群(聚类1和2)具有纤维细胞特征(图2A-B)。据报道,纤维细胞来源于造血系统,并同时表达造血标志物(如CD45)和成纤维细胞标志物(如细胞外基质蛋白)。已知纤维细胞能够迁移至伤口部位,促进炎症和纤维化反应。纤维细胞样apCAF表达多种造血基因,例如PTPRC(CD45基因)、CD37和CD52(图2B)。因此,在本研究中,他们将间皮细胞相关的细胞群命名为M-apCAF,将纤维细胞相关的细胞群命名为F-apCAF。随后,进行了伪时间分析,结果显示apCAF细胞群存在两种不同的动态转变轨迹(图2C)。在M-apCAF中间皮细胞基因MSLN的下调以及F-apCAF中PTPRC的下调,均伴随着HLA II基因(CD74、HLA-DRA)的上调。对F-apCAF(图2D)和M-apCAF(图2E)的通路分析表明,这两个apCAF细胞群均高度参与免疫调节活动。然而,他们发现这两个apCAF细胞群均缺乏主要共刺激分子(如CD40、CD80和CD86)的表达。这些数据表明apCAF能够呈递抗原,但缺乏共刺激分子,这种缺陷会导致调节性T细胞的诱导。
他们比较了两种apCAF群体中正常组织和癌组织之间的差异表达基因(DEG),并鉴定了在癌症中上调的基因,并通过评估每个基因在每种apCAF群体中与其他CAF亚型相比的特异性表达来评估其特异性。该分析最终鉴定出三个对F-apCAF(C1QC、APOC1和RARRES1)和M-apCAF(CD24、CA9和EGLN3)最具特异性的基因(图2F-G)。F-apCAF和M-apCAF的这三个基因特征均与癌症患者的不良生存预后显著相关(图2H)。此外,他们发现SPP1在两种apCAF群体中均普遍上调。重要的是,与其他CAF聚类相比,apCAF中SPP1的表达显著更高(图2G)。此外,SPP1表达在两种 apCAF 群体的伪时间轨迹中均有所增加(图2 C)。SPP1表达升高也是患者生存的强负性预后标志物。
为了解apCAF中的调控网络,他们进行了SCENIC分析,结果显示F-apCAF(SPI1、RUNX3、GATA3)和M-apCAF(BARX2、BHLHE41、HSF4、POU5F1)的基因表达程序分别由不同的转录因子驱动(图2I)。这些转录因子可能直接调控关键apCAF特征基因的转录。例如,他们发现SPI1可能是F-apCAF中HLA II类基因(CD74、HLA-DRA、HLA-DRB1、HLA-DRB5、HLA-DPA1、HLA-DPB1、HLA-DQA2、HLA-DQB1、HLA-DMA)的潜在调控因子(图2J)。他们还发现POU5F1(OCT4 的基因,OCT4 是调控干性的主要转录因子)可能调控M-apCAF中的SPP1(图2K)。随后,他们分析了两种apCAF群体在不同癌症类型中的丰度,发现 F-apCAF在PM、ccRCC、SCC、HCC和STAD中最为富集,而M-apCAF在 ccRCC、HCC、COLO、OV和PM中最为富集(图2L-M)。因此,在后续研究中,他们选择PM作为关键模型,以进一步了解 apCAF。
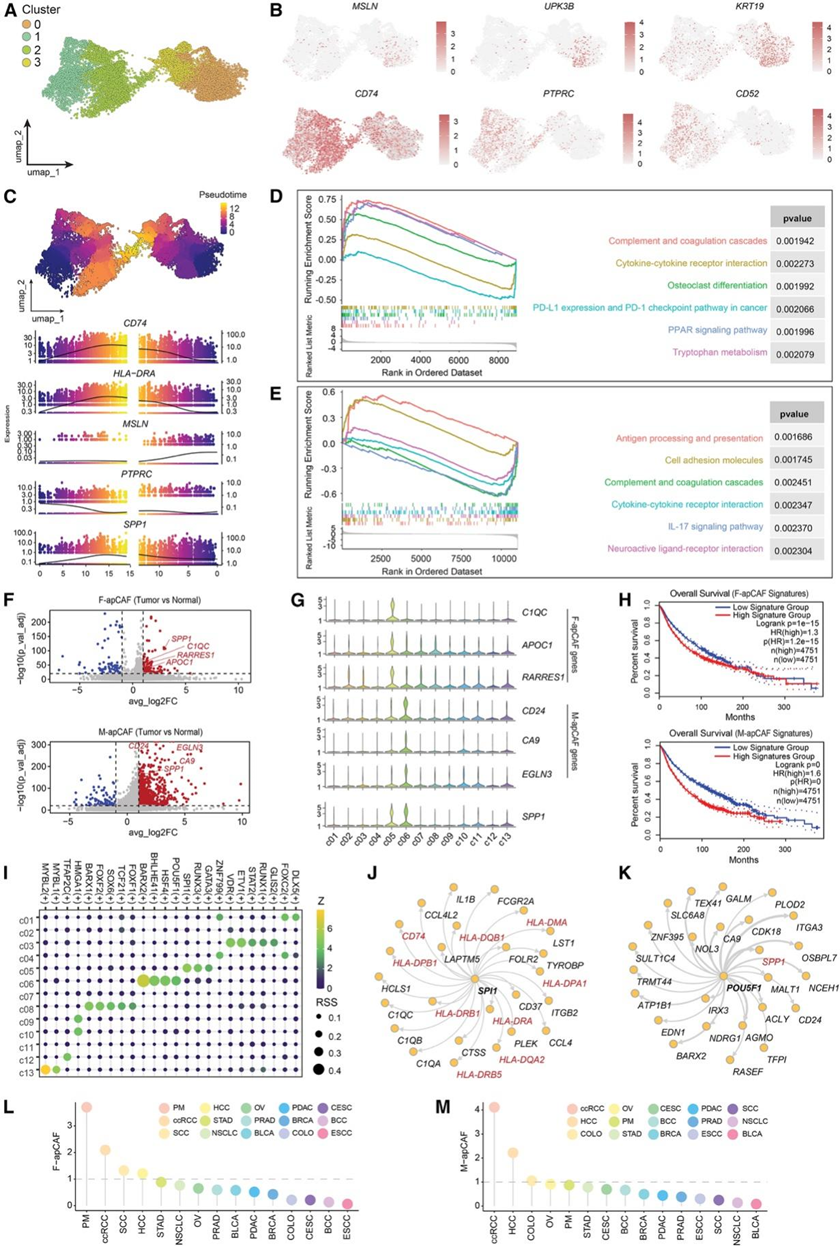
图2. 两种不同的 apCAF 细胞群。
(A) 从图 1 C 中提取的所有 apCAFs(HLA II+)的 UMAP,重新聚类后揭示了四个亚聚类。(B) 特征基因的UMAP。(C) 伪时间轨迹(Monocle3)显示 apCAF 亚组之间存在两种不同的过渡轨迹。(D) F-apCAF 亚聚类(2 个亚聚类 vs. 1 个亚聚类)的 GSEA 分析。(E) M-apCAF 亚聚类的 GSEA 分析。(F) 两种apCAF群体中正常组织和癌组织之间的DEG。(G) 小提琴图显示了CAF 亚聚类中C1QC、APOC1、RARRES1、CD24、CA9、EGLN3和SPP1的表达。(H)生存分析。(I) CAF 亚群中转录因子的调控子活性评分。(J) 预测的F-apCAF中SPI1转录因子调控网络。(K) 预测的M-apCAF中POU5F1转录因子调控网络。(L) F-apCAF在不同癌症类型中的相对比例。(M) M-apCAF在不同癌症类型中的相对比例。
03
腹膜转移瘤的基质异质
腹膜是一种复杂的组织,由多种基质细胞组成,包括间皮细胞、成纤维细胞、内皮细胞和免疫细胞。这种特殊的微环境可能促进转移过程中apCAFs的形成。腹膜转移最常见的起源之一是结肠癌。约20%的结肠癌患者会发生腹膜转移。根据共同的上皮发育程序,原发性结肠癌的癌细胞可分为两种内在上皮表型(iCMS2和iCMS3)。因此,腹膜转移也可能来源于两种不同的癌细胞谱系,并由异质性基质组成。在专门研究apCAF之前,他们首先尝试使用空间转录组学方法,对腹膜转移的上皮和基质异质性进行整体研究。
他们收集了8例结肠癌原发性PM患者的组织标本,对肿瘤上皮和邻近间质的分子特征进行了表征(图3A-B)。对感兴趣上皮区域(ROI)的特征进行反卷积和主成分分析,揭示了两种分子亚型:iCMS2样或iCMS3样(图3C-D)。细胞类型特异性富集分析显示,iCMS2上皮细胞类似于肠上皮细胞,而iCMS3上皮细胞类似于杯状细胞,表明PM癌细胞内存在两种不同的细胞谱系程序(图3E)。为了评估其预后意义,他们使用iCMS3标记物SPINK4进行免疫组化染色,检测了T4期原发性结肠癌病例(图3F)。他们发现 SPINK4+侵袭前沿与 PM 风险升高之间存在显著关联,与 SPINK4-的对应物相比(图3G),强调 iCMS3 上皮细胞是 PM 的潜在驱动因素。
接下来,他们分析了肿瘤细胞邻近间质的转录组信息。基于反卷积分析,他们将间质ROI分为iCMS2和iCMS3两类,发现iCMS3间质在HLA II抗原呈递和炎症相关通路中富集(图3H-I)。考虑到iCMS3 PM中观察到的独特炎症特征,他们推测iCMS2 PM和iCMS3 PM之间免疫细胞浸润可能存在差异。为了验证这一推测,他们对两种亚型均采用了成像质谱流式细胞分析。分析结果表明,iCMS3 PM中T细胞和HLA II+Vimentin+间质细胞的数量有增加的趋势(图3J-K)。他们在更大规模的PM样本队列中验证了T细胞的变化,进一步证实iCMS3 PM具有更高的免疫活性。
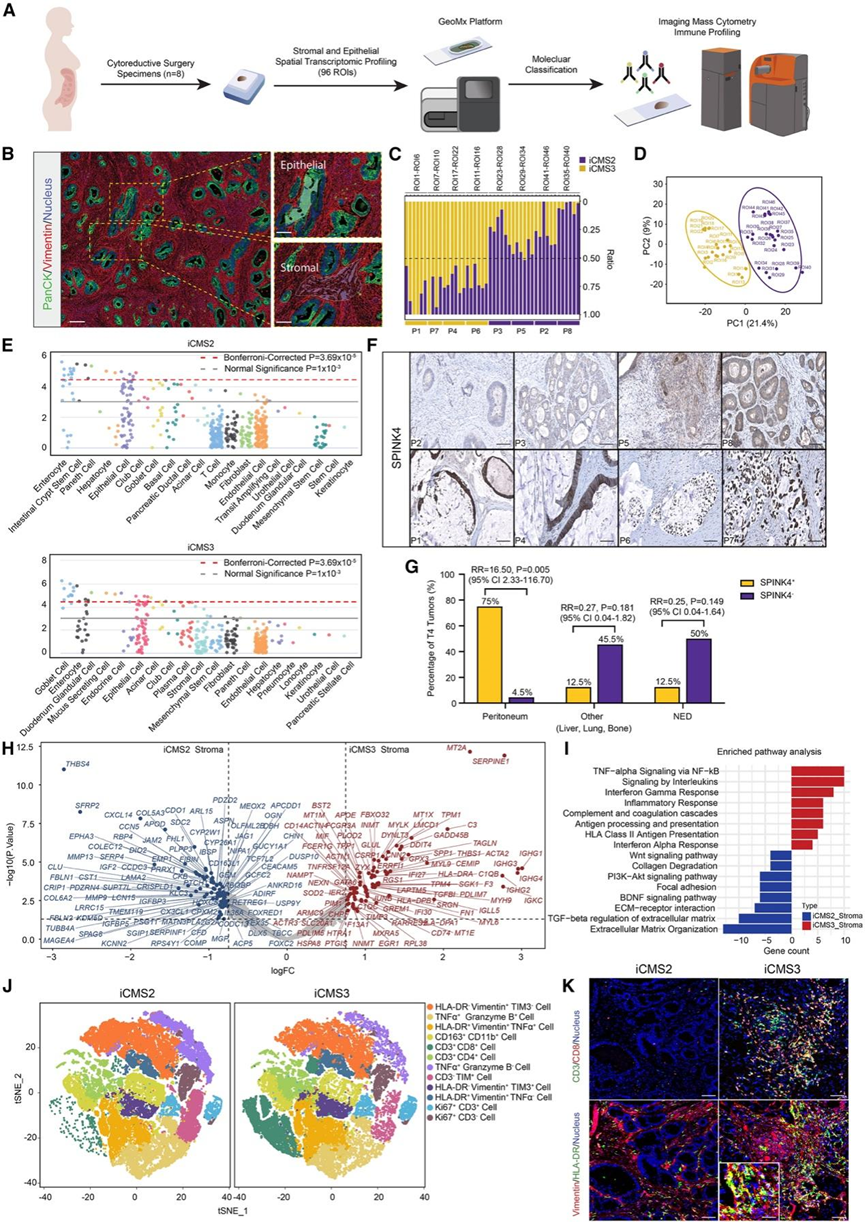
图3. PM基质的分子分类。
(A) 使用 GeoMx 空间转录组学和成像质谱流式细胞的 PM 分子分类工作流程。(B) GeoMx 检测的代表性形态学标记染色。(C) 利用 iCMS2/iCMS3 特征对 GeoMx 空间转录组数据进行反卷积。(D) 对 iCMS2 和 iCMS3 PM 组中所有 ROI 进行 PCA 分析。(E) 利用 iCMS2 和 iCMS3 PM 中差异表达的基因进行细胞类型富集分析。 (F) iCMS2(P2、3、5、8)和iCMS3(P1、4、6、7)PM组中SPINK4 IHC。(G) SPINK4 +/-浸润边界的 T4 期结肠癌中 PM 和其他部位转移的百分比和相对风险。(H) iCMS2 和 iCMS3 PM 基质之间的差异表达基因。(I) 基于 iCMS2 和 iCMS3 PM 基质之间差异表达基因的通路富集。(J) 对 iCMS2 和 iCMS3 PM 样本进行成像质谱流式细胞分析。(K)免疫荧光染色。
04
F抗原呈递癌相关成纤维细胞微环境的空间分析
iCMS3 PM中的HLA II +基质特征可能部分归因于apCAF的存在。虽然GeoMx平台能够提供无偏倚的转录组特征,但该技术的细胞分辨率有限。为了进一步解析apCAF及其相关微环境在单细胞分辨率下的空间分布,他们利用了高通量空间成像平台,基于构建的scRNA-seq图谱(图1)设计了一个包含480个基因的完全定制探针组。随后,他们使用8个结肠来源的人类PM样本(包括一个PM邻近组织)进行了检测。最终,他们从所有样本中获得了799455个高质量细胞。无监督聚类分析鉴定出主要细胞类型,包括CAF、SMC、内皮细胞、淋巴细胞、髓系细胞、iCMS2 和 iCMS3 癌细胞(图4A-B)。在 8 个 PM 样本中,3 个样本具有明显的 iCMS3 上皮细胞特征(PM1、PM2 和 PM3),2 个样本具有 iCMS2 特征(PM6 和 PM7),而另外 2 个样本则同时具有 iCMS2 和 iCMS3 特征(PM4 和 PM5)(图 S3A)。iCMS3 癌细胞的存在与淋巴细胞浸润增加相关(图4C),这与 GeoMx 检测揭示的基质细胞特征一致(图 3)。
接下来,他们利用泛癌单细胞RNA测序图谱构建的参考图谱(图4D),对空间转录组数据进行稳健的细胞类型分解,从而将其分解为不同的细胞类型,并进行细胞微环境组成分析(图4E)。在淋巴细胞浸润显著的iCMS3 PM样本中,可以鉴定出四个不同的空间微环境:血管富集微环境、淋巴细胞富集微环境、基质富集微环境和肿瘤富集微环境。微环境组成分析表明,在基质富集微环境和肿瘤富集微环境中,myCAF和髓系细胞是主要的基质细胞群,而血管富集微环境主要由内皮细胞和周细胞组成。值得注意的是,F-apCAF是淋巴细胞富集微环境中最丰富的细胞类型(图4E)。为了验证这种空间关联性,他们从含有iCMS3癌细胞的PM样本中选取了10个淋巴细胞富集的微环境,并定量了每种细胞类型的比例(图4F-G)。该分析证实,F-apCAF是淋巴细胞富集区域中最常见的CAF亚型(图4G)。
虽然myCAF在淋巴细胞富集微环境中也占据了相当大的细胞比例,但他们发现F-apCAF的密度更高,且与淋巴细胞聚集体的相互作用更紧密(平均距离分别为37.86 μm和66.06 μm)(图4H)。为了研究F-apCAF与免疫细胞之间的相互作用,他们首先从泛癌scRNA-seq图谱中鉴定了髓系细胞和淋巴细胞亚型。然后,他们利用F-apCAF衍生的配体和免疫细胞表达的受体进行了配体-受体相互作用分析。结果揭示了许多介导F-apCAF免疫调节功能的重要信号(图4I-J)。例如,CCL5可转录 T 细胞和单核细胞的趋化因子,可能有助于淋巴细胞的募集。然而,也发现了免疫抑制基因,例如SPP1和LAIR1,这表明 F-apCAF在炎症性肿瘤中发挥着复杂的作用。
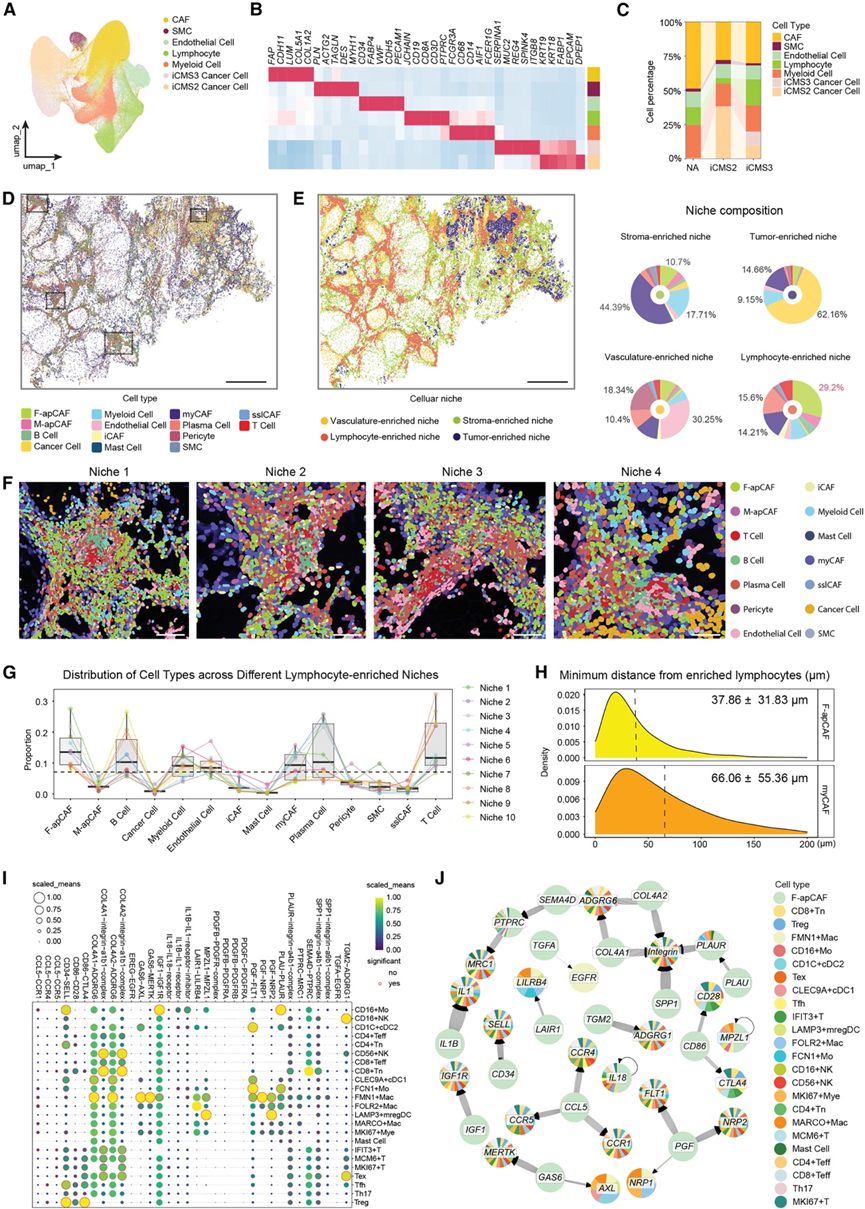
图4. F-apCAF 生态位的空间分析。
(A) 来自 Xenium 检测的 8 个人类 PM 样本中主要细胞类型的 UMAP。(B) 每个 PM 细胞聚类的标记基因的热图。(C) 非肿瘤邻近(NA)、iCMS2 和 iCMS3 PM 样本中的主要细胞类型比例。(D) 代表性 iCMS3 PM 样本中的细胞类型。(E) 左图:利用k近邻算法计算的空间生态位。右图:四个不同空间生态位中的细胞类型组成。 (F) 四个代表性的淋巴细胞富集微环境中的细胞空间分布。(G) 来自 5 个 PM 样本的 10 个淋巴细胞富集微环境中细胞类型的比例分布。(H) 对淋巴细胞富集聚集体中的 F-apCAF 或 myCAF进行细胞密度和空间距离分析。(I) F-apCAF(配体)与免疫细胞(受体)配体-受体对的概率分析。(J) F-apCAF衍生的配体与免疫细胞受体之间存在显著的配体-受体对。
05
M抗原呈递癌相关成纤维细胞微环境的空间分析
与F-apCAF相比,M-apCAF的空间分布更具环境依赖性。由于腹膜内衬有间皮细胞,癌细胞转移至该部位可能通过与间皮细胞的直接相互作用诱导M-apCAF的形成。M -apCAF表达细胞角蛋白基因(图2B),免疫组化染色显示细胞角蛋白阳性CAF浸润腹膜基质,通常位于细胞角蛋白阳性间皮附近(图5 A)。使用癌细胞标志物(SPINK4)和CAF标志物(PDGFRα)进行多重免疫组化染色证实,这些CAF并非来源于癌细胞(图5 A)。在细胞角蛋白阳性CAF浸润显著的样本中,空间转录组细胞类型反卷积和微环境组成分析鉴定出独特的间皮细胞富集微环境,以及基质、血管和肿瘤细胞富集微环境(图5B-C)。这些间皮细胞富集微环境的主要基质成分包括M-apCAF(23.89%)、髓系细胞(15.48%)和T细胞(12.38%)(图5C)。一些间皮细胞富集微环境与正常间皮(以MSLN和UPK3B标记)相连,提示间皮细胞向M-apCAF分化。大多数间皮细胞富集微环境邻近肿瘤上皮(图5D),表明M-apCAF可能与免疫细胞和癌细胞密切相互作用。
公开的研究表明,M-apCAF能够在小鼠模型中诱导免疫抑制性T细胞的形成。与此一致,他们发现间皮细胞富集微环境中的T细胞高表达多种抑制性标志物(TIGIT、CTLA4、LAG3、PDCD1、ICOS、FOXP3)(图5E)。进一步的配体-受体相互作用分析表明,SPP1是介导M-apCAF与免疫细胞或癌细胞相互作用的主要配体。
SPP1,又称骨桥蛋白,是一种高度磷酸化的分泌蛋白,通常在骨骼中发挥细胞外结构蛋白的作用。在伤口和癌症环境中,SPP1作为一种急性期蛋白表达上调。它与炎症和纤维化反应相关。在癌症中,已知SPP1通过促进癌细胞的细胞可塑性和化疗耐药性以及作为T细胞的免疫检查点,发挥多方面的促肿瘤作用,但SPP1在PM中的作用尚不清楚。有趣的是,他们观察到iCMS3 PM中基质来源的SPP1水平较高,这可能有助于该PM亚型的腹膜趋向性。SPP1可由癌细胞、髓系细胞和CAF表达。一项关于乳腺癌的研究报道,apCAF是 SPP1 的重要产生细胞。在其他 CAF 亚型中,apCAF是 SPP1 的主要来源。他们通过检测从MC38小鼠结肠癌细胞建立的体内PM中分离的癌细胞 (EpCAM+)、髓系细胞 (CD11b+)、apCAF(PDGFRα+MHC II+) 和其他 CAF(PDGFRα+MHC II−)中总 SPP1 和分泌型 SPP1 的表达来验证这一结果。数据显示,与其他基质细胞相比,apCAF产生的 SPP1 水平最高。此外,他们用肿瘤条件培养基处理从正常小鼠大网膜分离的间皮细胞(OmMeso 细胞),并观察到OmMeso 细胞中 SPP1 表达显著升高(图 5 F)。
为了检测SPP1对癌细胞迁移和侵袭的影响,他们利用MC38细胞进行了划痕实验和Matrigel侵袭实验。结果显示,添加SPP1蛋白显著增强了癌细胞的迁移和侵袭,而抗SPP1单克隆抗体(mAb)则抑制了癌细胞的迁移和侵袭。随后,通过将MC38细胞腹腔注射到野生型或Spp1基因敲除(KO)小鼠体内,研究了宿主SPP1在PM形成中的作用。结果发现,宿主Spp1 KO显著减少了PM和腹水的形成(图5 G)。用抗SPP1 mAb治疗携带PM的野生型小鼠也观察到了类似的表型(图5H)。为了评估apCAF来源的SPP1的重要性,他们利用MC38细胞在野生型或Spp1 KO小鼠体内建立了PM结节。将分离的apCAF(PDGFRα+MHC II+)和其他CAF(PDGFRα+MHC II−)与MC38细胞共培养,进行克隆形成和Matrigel侵袭实验。apCAF分泌的SPP1显著增强了MC38细胞的克隆形成和侵袭能力,而抗SPP1单克隆抗体则抑制了这种作用(图5I-J)。综上所述,这些数据表明基质SPP1可能驱动PM的形成,而apCAF产生SPP1以促进这一过程。
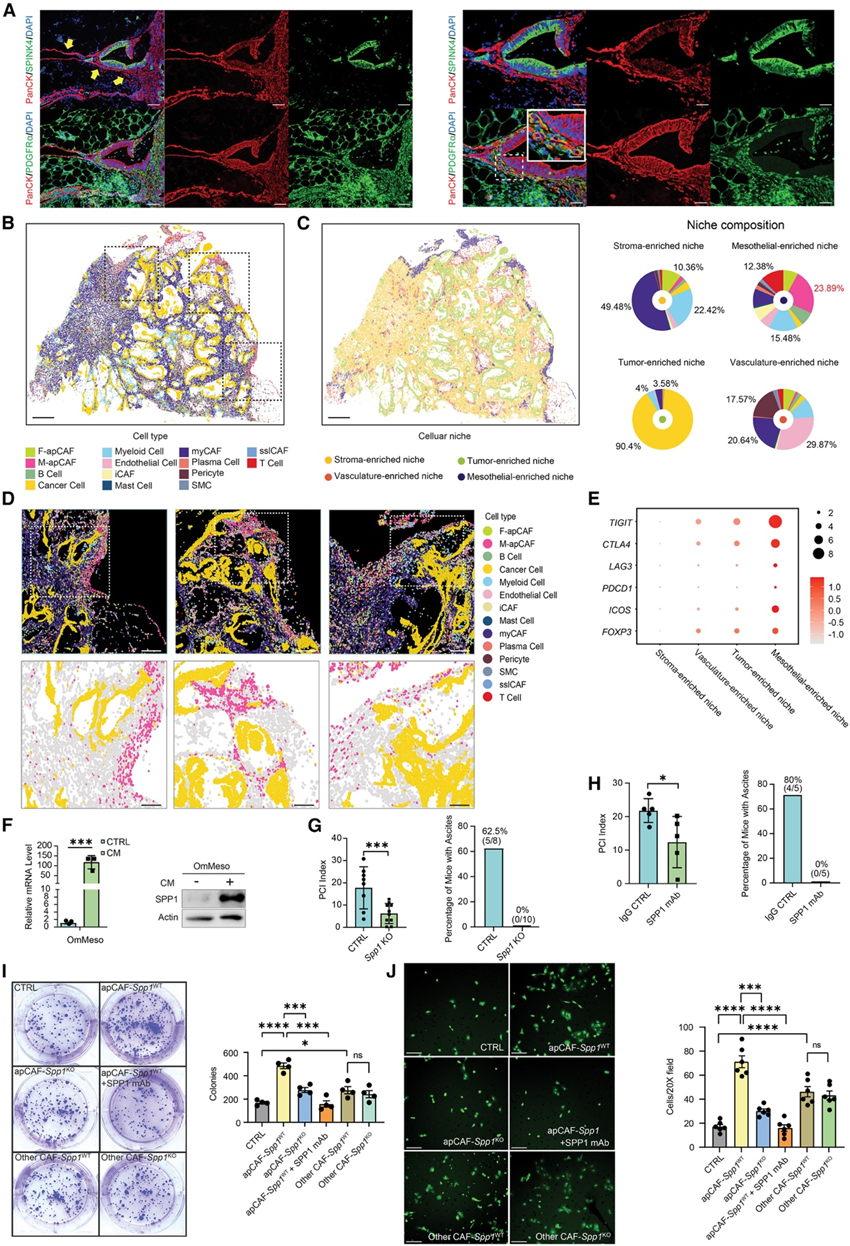
图5. M-apCAF 生态位的空间分析。
(A) 人PM组织的多重免疫组化染色显示PanCK、SPINK4、PDGFRα和DAPI。(B) 代表性PM样本中的细胞类型。(C) 左图:利用k近邻算法计算的空间生态位。右图:四个空间生态位中的细胞类型组成。(D) 三个富含M-apCAF区域的细胞空间分布。(E) T 细胞免疫抑制基因在四个空间生态位中的表达。(F) 通过 RT-PCR和免疫印迹法检测肿瘤条件培养基(CM)处理后 OmMeso 细胞中 SPP1 的表达。(G-H) 分析腹膜癌指数(PCI)评分和腹水情况。(I)克隆形成分析。(J) Transwell 和单克隆抗体分析。
06
胰腺导管腺癌中,M-apCAF与SPP1阳性微环境相关
鉴于公开对PDAC中 apCAF 的研究,他们也对 PDAC 模型进行了研究。他们对 3 例未经治疗和 3 例接受放化疗的人类 PDAC 样本进行了检测。无监督聚类分析鉴定出 6 种主要细胞类型,包括 CAF、内皮细胞、淋巴细胞、髓系细胞和两种癌细胞群(癌细胞 1 和癌细胞 2)。他们发现,放化疗后,组织间质增生性增强,CAF 比例增加,这与最近的一项报道一致。在六个样本中,他们发现三个样本具有更显著的 T&B 细胞特征。细胞反卷积后,他们发现 F-apCAF 也与 PDAC 中富含淋巴细胞的区域相关(图 6A-C)。他们通过多重免疫组化(IHC)在更大规模的人类PDAC样本队列中进一步验证了这一结果。在30例患者中,8例表现出淋巴细胞富集区域(CD3+CD19+)。他们对这8例样本的14个区域中的PDGFRα+HLA-DRA+CD45+F-apCAF进行了定量分析,并比较了淋巴细胞富集区域和非富集区域。结果显示,淋巴细胞富集区域中F-apCAF的丰度显著高于非富集区域(图6D-E)。
化疗和放疗后,癌细胞1的比例下降,而癌细胞2的比例保持稳定,表明癌细胞2具有治疗耐药性。差异基因分析显示,癌细胞2的特征是SPP1高表达,从而在组织中形成SPP1阴性和SPP1阳性的肿瘤上皮。有趣的是,M-apCAF在SPP1阳性肿瘤区域富集(图6F-G),这些区域也包含浸润的SPP1阳性髓系细胞,代表促肿瘤极化(图6F)。这些发现表明,M-apCAF有助于形成SPP1阳性微环境,从而促进PDAC的肿瘤进展和治疗耐药性。
为了证实apCAF是PDAC中SPP1的主要来源,他们用PDAC类器官条件培养基处理胰腺间皮细胞系(PanMeso细胞),结果发现SPP1表达上调(图6H)。随后,他们通过将GFP标记的PanMeso细胞与PDAC细胞系(BMFA3或CT1BA5)原位共注射,检测体内诱导情况。从已建立的肿瘤中分离的GFP+PanMeso细胞,Spp1表达较亲代细胞显著升高(图6I)。接下来,他们通过将同源PDAC细胞系(6620c1)原位注射到野生型或Spp1敲除小鼠体内,研究了宿主SPP1对PDAC进展的影响,发现宿主Spp1缺失显著抑制了肿瘤生长(图6J)。抗SPP1单克隆抗体治疗也得到了类似的结果(图6K)。为了评估apCAF来源的SPP1的具体作用,他们从野生型或Spp1敲除肿瘤中分离出PDGFRα+MHC II+apCAF,用于共培养实验。apCAF来源的SPP1显著增强了6620c1细胞的克隆形成和化疗耐药性(图6L-M)。同样,PanMeso细胞共培养也增强了6620c1细胞的化疗耐药性,而Spp1敲低或抗SPP1单克隆抗体则消除了这种效应(图6N)。这些结果表明,apCAF来源的SPP1直接促进PDAC的进展和化疗耐药性。
为了解宿主Spp1 KO对肿瘤微环境的影响,他们对对照组和敲除组的肿瘤组织进行了scRNA-seq。结果显示,宿主Spp1 KO肿瘤中T细胞浸润显著增加(图6 O)。然而,Spp1 KO也导致成纤维细胞数量增加(图6O),提示成纤维细胞可能发生表型改变,从而促进T细胞浸润。对两组成纤维细胞进行非监督重聚类分析,鉴定出iCAF、myCAF和apCAF(图6 P-Q),其中Spp1表达主要富集于apCAF。通过检测从 6620c1 原位肿瘤中分离的不同细胞群(EpCAM +癌细胞、CD11b +髓系细胞、PDGFRα+MHC II+apCAF和 PDGFRα+MHC II −其他 CAF)中的总SPP1和分泌的 SPP1 来验证这些发现,证实 apCAF是基质 SPP1 的主要来源。
在比较Spp1 KO后CAF亚型的比例时,观察到myCAF减少,而iCAF和apCAF增加(图6Q)。apCAF的扩增可能代表一种试图恢复SPP1信号的补偿机制。重要的是,敲除组的CAF上调了sslCAF标志物(Pi16、Dpt)(图6R),表明其向正常组织中发现的稳态特征趋于正常。CytoTRACE分析支持iCAF/sslCAF是myCAF的前体细胞。此外,Spp1 KO的CAF中T细胞趋化因子特征上调,这可能解释了T细胞浸润的增加。通过用TGFβ(一种myCAF分化的主要信号)处理胰腺星状细胞来验证这些发现,同时在野生型或Spp1 KO apCAF存在的情况下进行处理,结果表明apCAF来源的SPP1显著促进了myCAF的分化,表现为祖细胞基因(Pi16)表达降低和成熟myCAF标志物(Postn、Acta2、Lrrc15)表达增加(图6S)。综上所述,这些结果证实apCAF是基质中SPP1的主要来源,促进了促纤维增生屏障的形成。
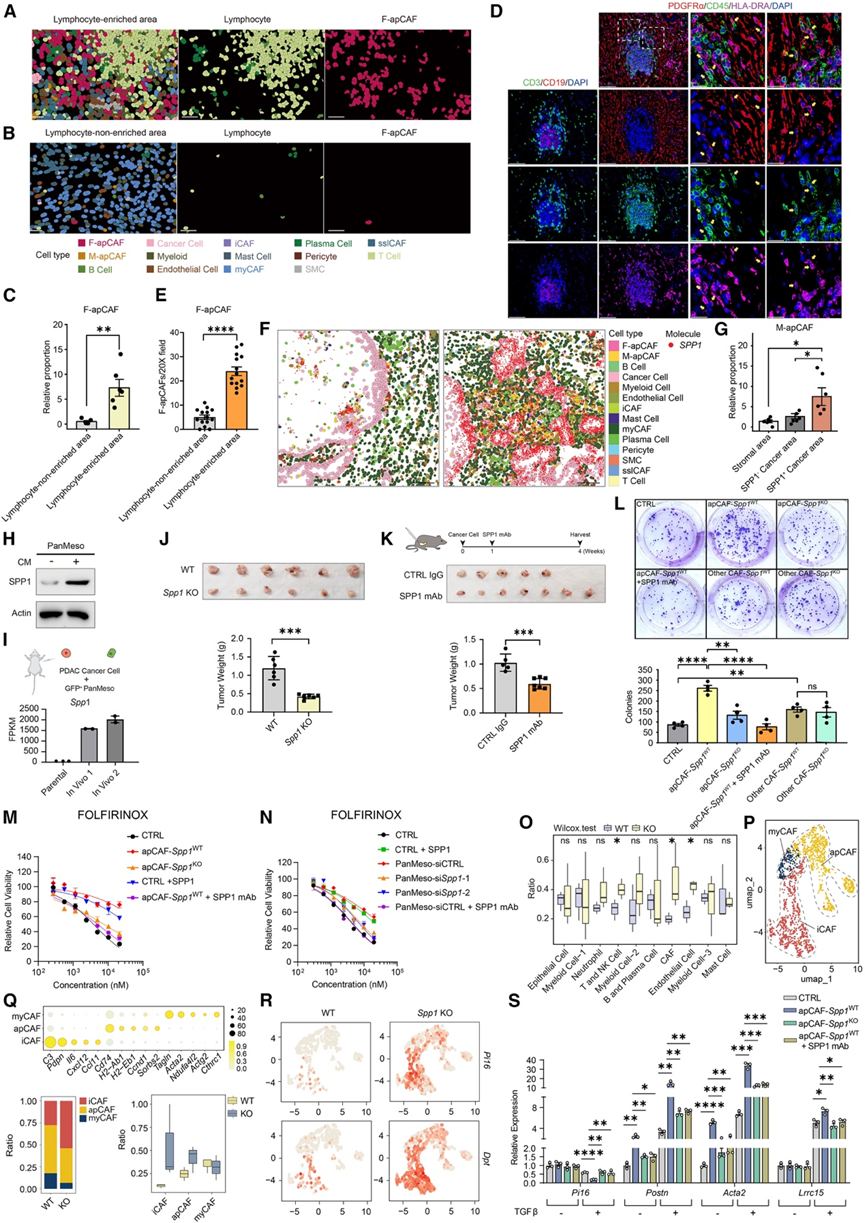
图6. apCAF促进 SPP1+肿瘤促进微环境的形成。
(A) 使用RCTD算法进行反卷积后,显示了PDAC中富含淋巴细胞的微环境中的细胞类型。(B) 使用RCTD算法进行反卷积后,显示了PDAC中非淋巴细胞富集微环境中的细胞类型。(C) 在 PDAC 样本中,对淋巴细胞富集和非富集微环境中的 F-apCAF进行 Xenium 检测定量。(D) 人胰腺导管腺癌组织多重免疫组化染色显示CD3、CD19、PDGFRα、HLA-DRA、CD45和DAPI。(E) 对 PDAC 样本中淋巴细胞富集和非富集微环境中的 F-apCAF进行多重 IHC 定量分析。(F) SPP1-和SPP1+癌区细胞的空间分布和SPP1表达。(G) 对基质、SPP1-和 SPP1 +癌区的 M-apCAF比例进行 Xenium 检测定量。(H) 检测 PDAC 肿瘤 CM 处理后 PanMeso 细胞中 SPP1 的表达。(I) 将 GFP+ PanMeso 细胞与小鼠 PDAC 细胞(BMFA3:体内1 或 CT1BA5:体内2;1:1 比例)共注射形成肿瘤。然后对 GFP+细胞进行流式分选。(J) 将 6620c1 PDAC 细胞原位注射到 WT 或Spp1 KO 小鼠后肿瘤重量。(K) 将 6620c1 细胞原位注射到接受对照抗体或抗 SPP1 mAb治疗的小鼠体内后,肿瘤重量。(L)克隆形成分析。(M) 将 CFSE 标记的 6620c1 细胞与从野生型 (WT) 或Spp1敲除型 (KO) 胰腺导管腺癌 (PDAC) 肿瘤中分离的 apCAFs (PDGFRα+ MHC II+ ) 混合(1:1),并在 FOLFIRINOX 处理后检测其存活率。(N) 将CFSE标记的6620c1细胞与PanMeso细胞(1:1)混合,转染对照siRNA(siCTRL)或两种独立的针对Spp1的siRNA (si Spp1-1和si Spp1-2),并在FOLFIRINOX处理后检测其存活率。(O) 通过scRNA-seq分析野生型(WT)和Spp1 KO肿瘤的细胞类型比例。(P) 从 WT 和Spp1 KO 肿瘤 scRNA-seq 数据中鉴定的 iCAF、myCAF 和 apCAF 聚类。(Q) 上图:CAF亚群中标记基因的表达情况。点的大小表示聚类内表达各基因的细胞比例;颜色表示归一化的表达水平。下图:WT组和Spp1 KO组之间CAF亚型的比例变化。箱线图显示了每种细胞类型比例的范围。(R) 野生型和Spp1 KO肿瘤中sslCAF标记物Pi16和Dpt表达的UMAP。(S) 采用RT-PCR检测PSC与Spp1野生型或KO型apCAF共培养(有或无TGFβ)后基因表达的变化(Pi16、Postn、Acta2、Lrrc15)。
+ + + + + + + + + + +
结 论
本研究构建了一个涵盖15种组织和实体瘤的成纤维细胞分子图谱,通过整合研究意外地揭示了大多数癌症类型中存在两种不同的apCAF群体:一种与间皮样细胞相关,另一种与纤维细胞相关。利用高分辨率单细胞空间成像平台,本研究对这些apCAF群体的空间微环境进行了表征。间皮样apCAF位于癌细胞附近,而纤维细胞样apCAF则与富含淋巴细胞的微环境相关。此外,本研究还发现这两种apCAF群体均可上调SPP1的表达,而SPP1能够促进原发肿瘤的形成、腹膜转移和治疗耐药性。综上所述,本研究在分析apCAF及其空间生态位方面提供了新的理论依据。
+ + + + +



 English
English


