文献解读|Cell(42.5):泛神经退行性疾病蛋白质组学揭示疾病亚型和分子特征
✦ +
+
论文ID
原名:Pan-neurodegeneration proteomics reveals disease subtypes and molecular signatures
译名:泛神经退行性疾病蛋白质组学揭示疾病亚型和分子特征
期刊:Cell
影响因子:42.5
发表时间:2026.03.23
DOI号:10.1016/j.cell.2026.02.026
背 景
神经退行性疾病(ND)是一类复杂的疾病,其特征是进行性神经元功能障碍和丢失,最终导致严重的认知和运动障碍。这些疾病构成日益严重的全球健康危机,全球已有超过5500万人受到影响,并且由于人口老龄化,未来几十年这一数字可能显著上升。尽管如此,目前的治疗方法仍然有限,且临床疗效甚微,这也凸显了研究疾病机制以制定更有效的治疗策略的紧迫性。
实验设计
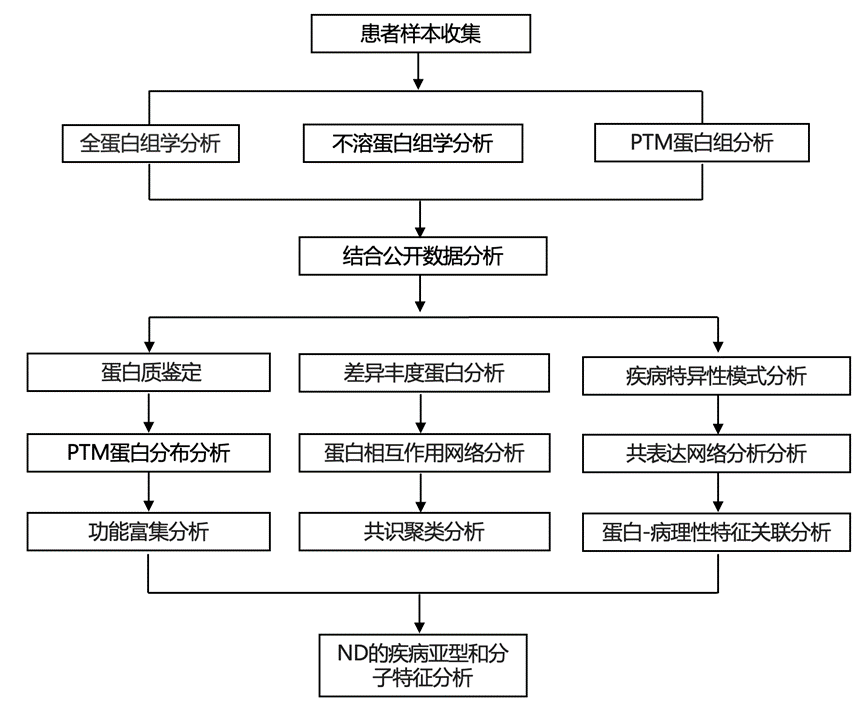
结 果
01
神经退行性脑组织样本的多层蛋白质组学分析
研究团队使用从三个互补的蛋白质组学维度对代表6种主要ND和对照组的2279个脑组织样本进行了分析(图1A):全蛋白质组(1713个样本)、不溶性蛋白质组(166个样本)以及磷酸化和泛素化的PTM富集分析(238个样本),此外还进行了脑区分析(162个样本)(图1B-F)。鉴于PTM富集分析的样本数量有限,他们开发了JUMP-PTM流程,用于直接从数千个全蛋白质组和不溶性蛋白质组中鉴定未富集的PTM肽段。总体而言,全蛋白质组分析平均每个疾病组鉴定出 14767 个蛋白质和225个 PTM 肽段,所有组共鉴定出 22263 个蛋白质(11378 个基因)和 569 个 PTM 肽段(图 1G)。他们对多个 TMT 批次的不溶性蛋白质组和富集的 PTM 进行了分析。不溶性蛋白质组分析平均每个批次产生 11995 个蛋白质(8481 个基因)和 93 个 PTM 肽段,所有组共鉴定出 12235 个蛋白质(8668 个基因)和 102 个 PTM 肽段。富集磷酸化分析平均每批次鉴定出23980个磷酸化肽,总计65148个,其中5141个在所有批次中均有发现。泛素化分析平均每批次检测到8118个修饰肽,总计17719个,其中2372个在所有批次中均有发现。这些丰富的数据能够深入研究神经退行性疾病中的分子改变和疾病特异性亚型。
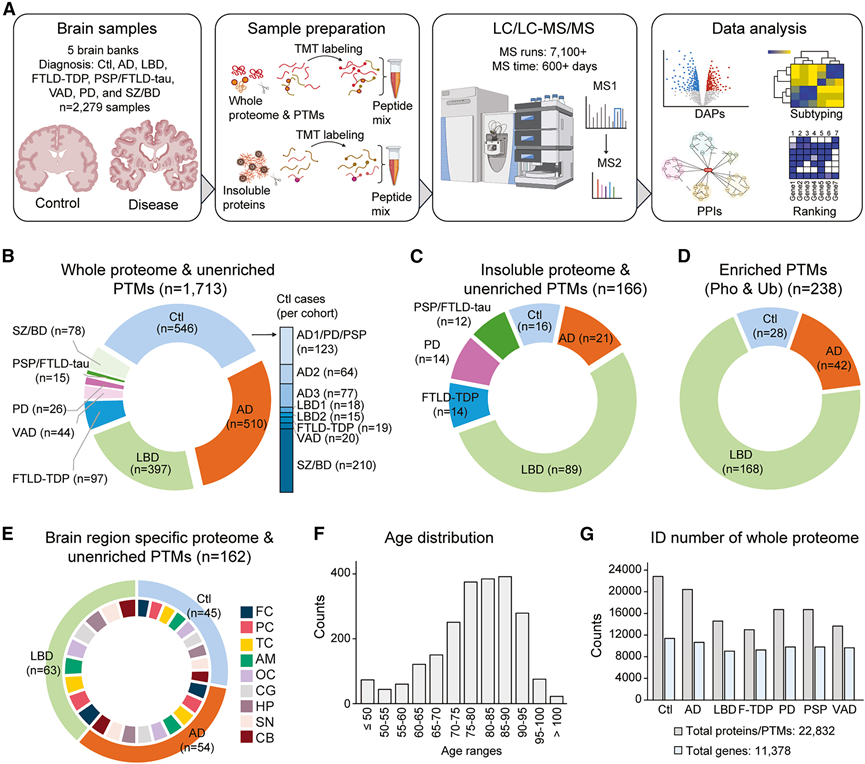
图1. ND的多层蛋白质组学分析。
(A) 实验工作流程示意图。(B) 不同ND患者全蛋白质组样本的分布。(C) ND中不溶性蛋白质组样品的分布。(D) 富集的PTM样本分布,显示了磷酸化富集(Pho)和泛素化富集(Ub)的修饰。(E) 脑区样本分布。(F) 脑捐献者的年龄分布。(G) 对ND患者蛋白质组中鉴定的蛋白质/未富集的PTM及其对应基因进行计数。
02
AD蛋白质组学揭示了三种不同的分子亚型和改变的通路
在阿尔茨海默病(AD)队列中,他们整合了多层蛋白质组:全蛋白质组、不溶性蛋白质组以及PTM富集蛋白质组[来自14例对照组和21例AD患者的5141种磷酸化富集肽段(Pho)和2372种泛素化富集肽段(Ub)](图2A)。在全蛋白质组中,与对照组相比,AD患者的β-淀粉样蛋白(Aβ)和磷酸化tau蛋白(pTau)水平显著升高(图2B)。他们进一步鉴定出2056个错误发现率(FDR)< 0.05的蛋白质,筛选了340个差异丰度蛋白(DAP)(图2C)。上调的DAP包括Aβ、载脂蛋白E(APOE)、微管相关蛋白tau(MAPT,tau)、中肾素(MDK)、ICAM1和GPNMB;而NPTX2、VGF和SST则显著下调。与三项近期AD脑蛋白质组学研究的比较显示出高度一致性,与AD转录组和脑脊液(CSF)蛋白质组的比较则显示出微弱但正相关的关系。功能分析表明,DAP富集于淀粉样原纤维形成、细胞外基质组织、脂肪酸运输和长期突触电位等过程。
为了鉴定阿尔茨海默病(AD)的分子异质性,他们对Banner Sun队列(发现队列)进行了聚类分析。共识聚类和主成分分析(PCA)显示了三种不同的分子亚型(ST1、ST2和ST3)(图2D-E),每种亚型富集于不同的生物学通路(图2F):ST1亚型富集突触信号通路(占样本的32.0%),ST2亚型富集细胞骨架调控通路(33.5%),ST3亚型富集血脑屏障(BBB)转运通路(34.5%)。这些蛋白质组学亚型与已建立的病理学和临床分类有所不同,但它们与神经纤维缠结和斑块负荷、Braak分期以及认知评分存在一定的关联。这些蛋白质组亚型的稳健性已通过两个独立的AD队列(分别包含174个和198个样本)得到验证(图2G-H)。他们进一步通过分析两个CSF蛋白质组队列(分别包含70个和150个病例)评估了其转化意义。超过10%的组织来源的DAP可在CSF中检测到,且这些共有蛋白始终能区分三种AD亚型。值得注意的是,两个CSF队列中23个重叠蛋白在受试者工作特征(ROC)曲线分析中表现出优异的分类性能,平均曲线下面积(AUC)为0.89,这表明不同患者的经典淀粉样蛋白和tau蛋白病理可能涉及多种通路,并且这些蛋白具有作为疾病亚型转化生物标志物的潜力。
除了Aβ和pTau外,U1-70K (SNRNP70)、DDX46和SNRPN等蛋白在不溶性组分中也高度富集(图2I-J)。这些不溶性蛋白主要与剪接体、SMN和CDC5L复合物等蛋白复合物相关。磷酸化和泛素化蛋白质组分析进一步鉴定出MAPT、NEFH、NEFM和SPP1等蛋白中位点特异性PTM失调,提示PTM在调节神经元细胞骨架和囊泡运输中发挥作用(图2K-L)。他们利用机器学习算法,基于酶-底物网络推断激酶和泛素E3连接酶的上游活性变化。例如,推断的活性分析表明,GSK3B信号异常可能驱动tau蛋白和其他参与细胞骨架和突触组织的神经元底物的过度磷酸化。类似地,Parkin (PRKN) E3连接酶活性的失调可能与AD中的线粒体功能障碍和突触功能衰竭有关。
基于多层蛋白质组学数据整合的DAP网络分析显示,RNA剪接异常、轴突发育异常、突触调控异常以及运输功能异常(图2M-N)。这些发现强调Aβ和pTau水平升高与更广泛的蛋白质组学变化同时发生。为了确定各个DAP的优先级,基于多组学数据集(全基因组关联研究[GWAS]、转录组、全蛋白质组、不溶性蛋白质组、PTM富集蛋白质组、相互作用组)进行了整合排序,并将MAPT、APP、APOE、MDK、NTN1和NEFH确定为主要候选基因(图2O)。
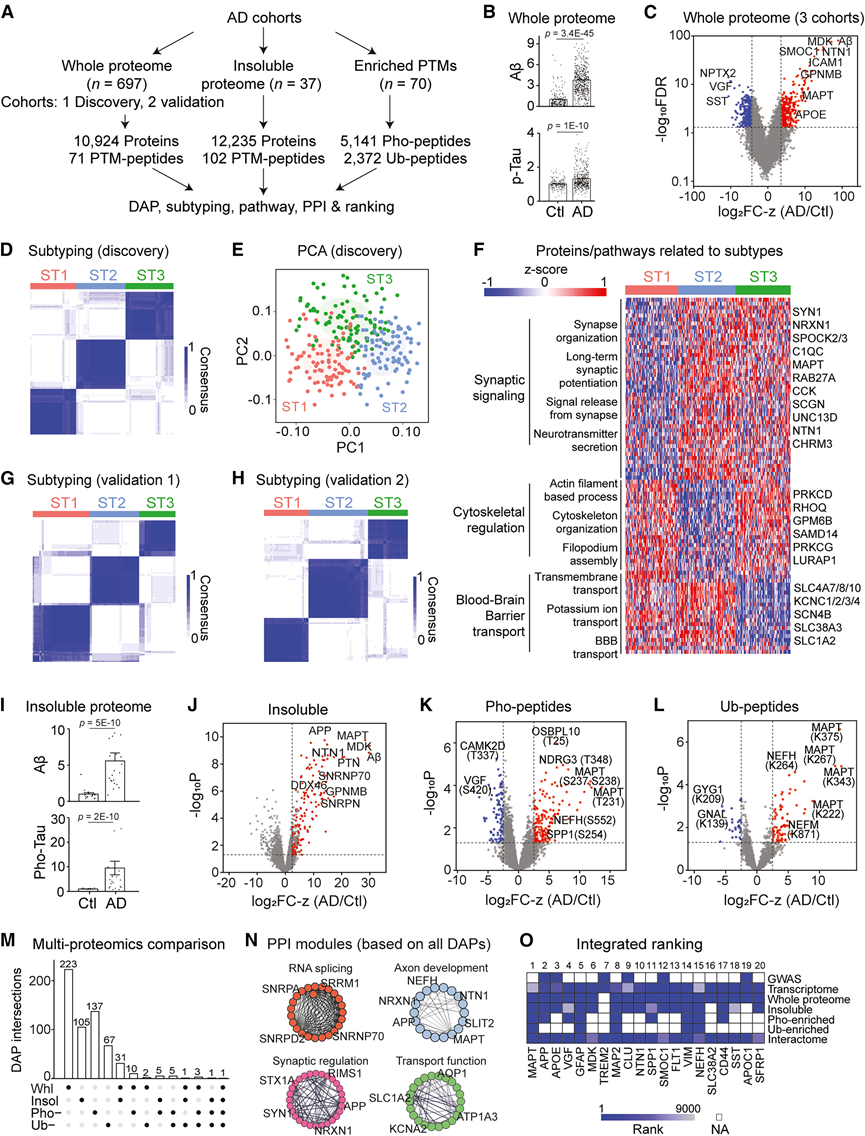
图2. 利用多层蛋白质组学进行AD的分子表征和亚型分类。
(A) 描述 AD 队列分析的工作流程。(B) 蛋白质组中Aβ和pTau的水平。(C) 火山图展示了三个队列中的 DAP。(D) 共识聚类显示发现队列中的三种 AD 亚型。(E) 发现队列中三个亚型的 PCA 图。(F) 蛋白质/通路与 AD 亚型关联的热图。(G-H) 共识聚类显示验证队列中的三种 AD 亚型。(I) 不溶性蛋白质组中Aβ和pTau的水平。(J-L) 火山图显示了不溶性蛋白质组、富集磷酸化蛋白质组和泛素组数据集中的 DAP。(M) UpSet 图显示了多层蛋白质组学中 DAP 的交集。(N) 基于组合DAP的选定PPI网络。(O) 对多个 AD 数据集中的蛋白质/基因进行综合排名。
03
LBD蛋白质组学和脑区分析
在路易体痴呆(LBD)中,他们分析了全蛋白质组(来自55例对照组和397例LBD患者的14442个蛋白质和148个PTM肽段)、不溶性蛋白质组(来自16例对照组和89例LBD患者的12,235个蛋白质和102个PTM肽段)以及PTM富集组分(14例对照组和84例LBD患者共有的5141个Pho肽段和2372个Ub肽段)(图3A)。正如预期,在全蛋白质组中,Aβ、pTau和α-syn的表达水平随LBD病理的不同而变化(图3B)。统计分析鉴定出2400个FDR < 0.05的蛋白质,其中包括627个DAP(图3C;)。其中,Aβ、GRHPR、MDK 和 GPNMB 在 LBD 中显著上调,而 NPTX2、FADS2 和 VGF 则下调。这些DAP与 AD 具有一些相似性,并且富集于脂肪酸 β-氧化、线粒体基因表达和超分子纤维组织等生物学过程。
蛋白质组的共识聚类将LBD(发现队列)分为四个分子亚型(ST1-ST4)(图3D),主成分分析(PCA)证实了不同的聚类模式(图3E)。每个亚型都表现出独特的生物学特征:ST1亚型(36.6%的样本)以线粒体功能为特征,ST2亚型(20.6%)以脂质代谢为特征,ST3亚型(23.2%)以转运过程为特征,ST4亚型(19.6%)以免疫和炎症反应为特征(图3F)。这些亚型与先前定义的病理和临床分组不同,虽然它们与路易体病理、Thal期和Aβ分期存在微弱关联。在独立队列中进行的亚型验证获得了高度一致的聚类结果(图3G-H)。
至关重要的是,不溶性蛋白质组分析显示Aβ、pTau、SNCA以及斑块相关蛋白(如MDK、PTN、ANKRD11和GPNMB)的水平升高(图3I-J);并且多种蛋白复合物富集。此外,PTM富集分析揭示了SPP1、NUCKS1、NEFH、NEFM和MAPT等蛋白的磷酸化和泛素化存在广泛的失调(图3K-L)。进一步的机器学习分析揭示了某些激酶和泛素E3连接酶的活性变化。例如,CAMK2A 活性降低可能会破坏突触信号传导和可塑性,而 SIAH1 活性增强可能会促进 LBD 中异常 α-突触核蛋白的泛素化。
跨层整合分析表明,全蛋白、不溶性蛋白和PTM数据集分别捕捉了LBD发病机制的独特方面,并共同突显了RNA剪接、线粒体翻译、脂肪酸氧化和炎症信号通路的改变(图3M-N)。最后,整合排序结果始终将MAPT、SNCA和APP列为排名靠前的蛋白,同时还发现了其他一些新兴候选蛋白,例如GPNMB、SPP1和HBA1(图3O)。综上所述,这些发现构建了LBD的蛋白质组学框架。
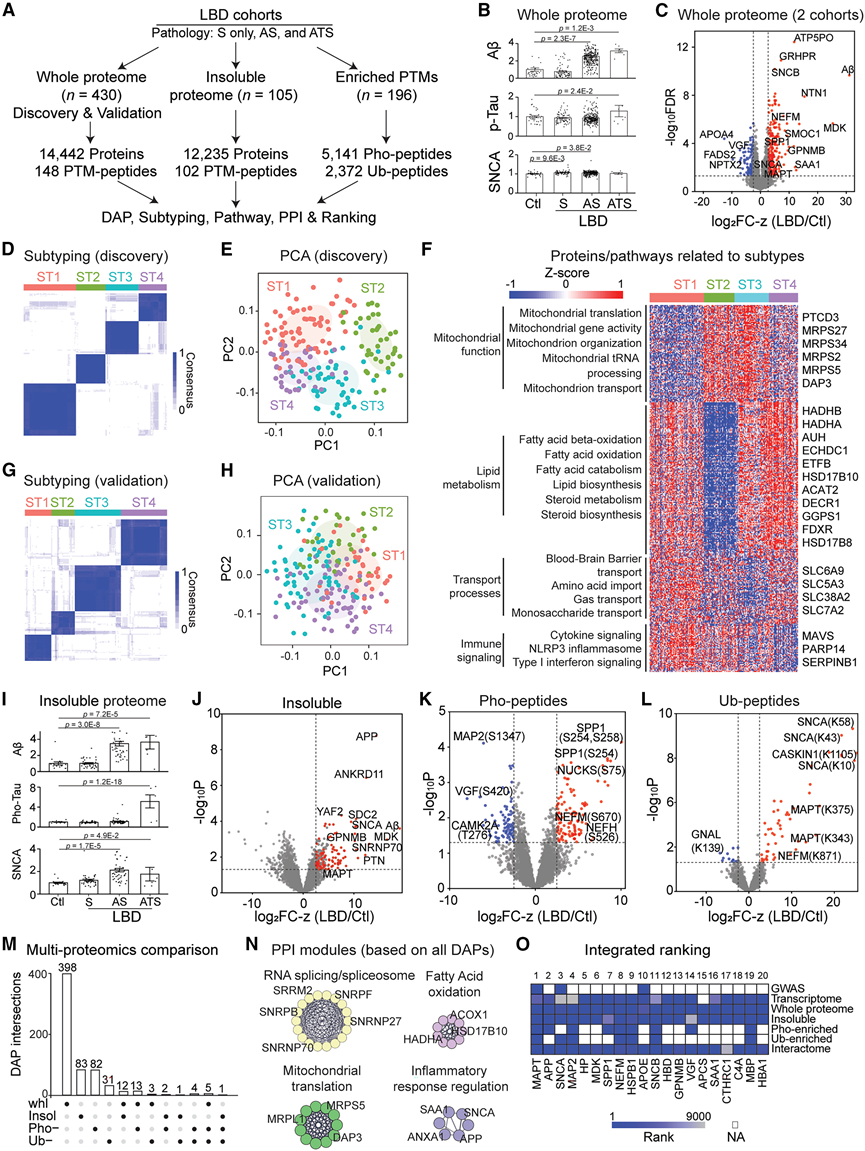
图3. 利用多层蛋白质组学对LBD进行分子表征和亚型分类。
(A) LBD队列分析的工作流程。(B) 全蛋白质组中Aβ、pTau和SNCA的水平。(C) 两个 LBD 队列中的DAP。(D) 共识聚类显示发现队列中的四种 LBD 亚型。(E) 发现队列中四个亚型的 PCA 图。(F) 蛋白质/通路与亚型关联的热图。(G-H) 共识聚类和 PCA 图显示验证队列中的四种 LBD 亚型。(I) 不溶性蛋白质组中 Aβ、pTau 和 SNCA 的水平。(J-L) 不溶性蛋白质组、磷酸化蛋白质组和泛素组数据集中的DAP。(M) UpSet 图显示了多层蛋白质组学中 DAP 的交集。(N) 基于组合DAP的选定PPI网络。(O) 对多个数据集中的蛋白质/基因进行综合排名。
04
FTLD-TDP蛋白质组学揭示疾病相关变化和分子异质性
在额颞叶变性(FTLD)-TDP中,他们分析了全蛋白质组(来自19例对照组和97例FTLD-TDP患者的12766个蛋白质和227个PTM肽段)和不溶性蛋白质组(来自16例对照组和14例FTLD-TDP患者的12235个蛋白质和102个PTM肽段)(图4A)。与对照组相比,FTLD-TDP全蛋白质组中TDP-43显著积累,在不溶性组分中的积累更为显著(图4B-G)。DAP分析鉴定出455个蛋白质,其中CLU、SCIN、GPNMB和ANXA1在FTLD-TDP中上调,而NPTX2、NEFM和INSC下调(图4C)。
为了解析FTLD-TDP的分子异质性,他们进行了共识聚类分析,并鉴定出四个具有不同蛋白质组学特征的亚型(ST1-ST4)(图4D)。主成分分析(PCA)也清晰地显示了这些亚型之间的分离(图4E)。亚型特异性分子模式包括:ST1亚型(占20.4%)的离子稳态和转运异常;ST2亚型(占21.7%)的线粒体功能异常;ST3亚型(占26.1%)的脂质调控异常;以及ST4亚型(占21.7%)的神经内分泌信号通路异常(图4F)。这些亚型表现出不同的TDP-43水平,并且与先前定义的病理和临床类型不同,虽然它们与遗传分组相关。在对先前发表的另一个 FTLD 队列的重新分析中也观察到了这四种亚型。
为了深入了解聚集蛋白,他们分析了不溶性蛋白质组,并鉴定出GPNMB、CD44、ANKRD11和组织蛋白酶家族蛋白显著富集(图4H)。全蛋白质组和不溶性DAP的比较分析仅发现一个显著的重叠(GPNMB),提示其在FTLD-TDP发病机制中可能具有重要意义(图4I)。对联合DAP的网络分析发现线粒体功能、突触功能、神经元细胞死亡和离子转运均受到显著扰动(图4J)。他们还利用GWAS、转录组、全蛋白质组、不溶性蛋白质组和相互作用组数据集进行了整合排序(图4K)。该分析将CD44、GFAP、GPNMB、ANXA1和TARDBP列为FTLD-TDP的关键相关蛋白。总体而言,这些结果提供了 FTLD-TDP 的大规模蛋白质组学图谱,通过整合多组学数据,鉴定出亚型并确定候选蛋白质和通路的优先级。
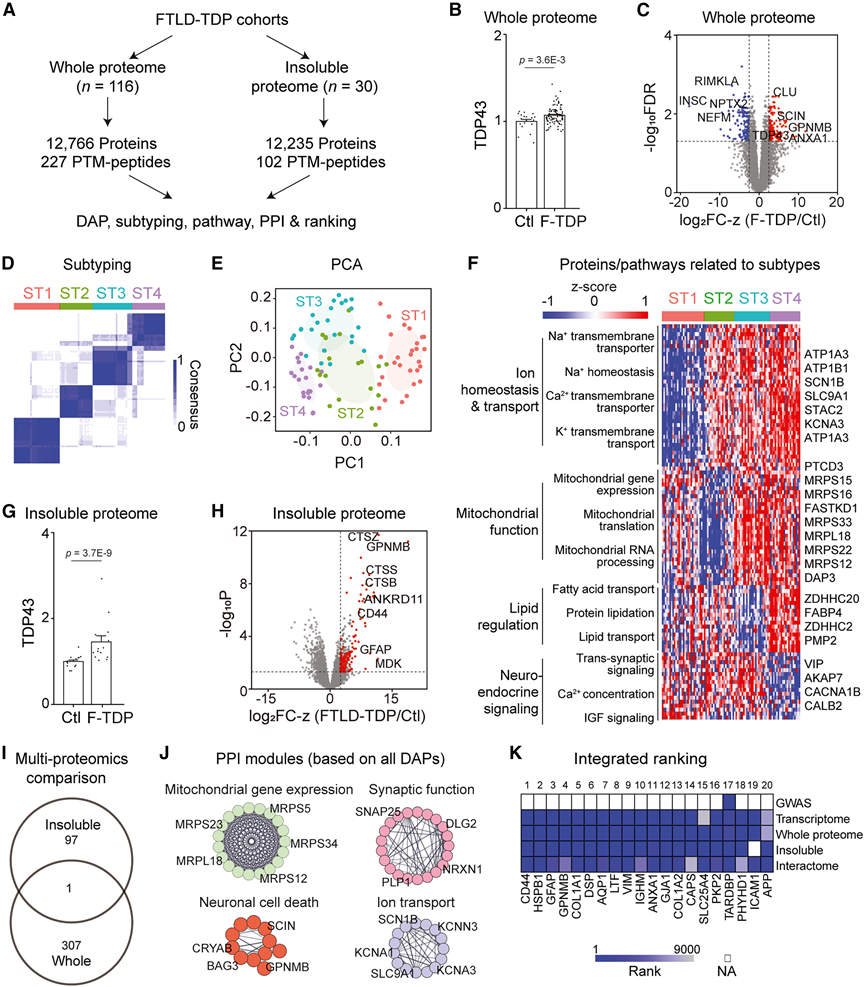
图4. FTLD-TDP 的蛋白质组学特征。
(A) 描述 FTLD-TDP 队列分析的工作流程。(B) 全蛋白质组中TDP-43的水平。(C) FTLD-TDP 中整个蛋白质组的 DAP。(D) FTLD-TDP 样本的共识聚类。(E) PCA 图显示了四种亚型的分布。(F) 蛋白质/通路与四种 FTLD-TDP 亚型关联的热图。(G) 不溶性蛋白质组中TDP-43的水平。(H) 不溶性蛋白质组中的DAP。(I) 在全蛋白质组和不溶性蛋白质组中鉴定的 DAP 的重叠。(J) 基于组合DAP的选定PPI网络。(K) 对多个 FTLD-TDP 数据集中的蛋白质/基因进行综合排名。
05
DAP分析揭示了疾病特异性改变
为了解共有和疾病特异性的蛋白质改变,他们对不同ND的DAP进行了比较。在上调的DAP中,鉴定出211种在至少两种ND中发生改变的蛋白质,以及11种在至少四种ND中发生改变的蛋白质(图5A)。TRIP10、SLC5A3、CHGA、GMPR、SLC39A12、GPNMB、B7Z8P9、NRIP2、SLC38A2、AMD1和IGFBP5等蛋白质在多种ND中均持续发生改变(图5B)。这些蛋白质参与多种关键生物学过程,包括神经元死亡调控、血脑屏障转运和生长因子信号传导(图5C)。值得注意的是,大多数DAP具有疾病特异性。例如,AD 中的 SPOCK2 和 PTN 蛋白、LBD 中的 ATP5PO 和 CHMP2A 蛋白、FTLD-TDP 中的 ZC3HAV1 和 PSME2 蛋白、血管性痴呆(VAD)中的 S100A8 和 NPTX1 蛋白、PD 中的 HOPX 和 L1CAM 蛋白以及 PSP 中的 SH3BGRL3 和 HNRPQ 蛋白均表现出疾病特异性的明显失调(图 5 D)。
他们进一步检测了ND中下调的DAP,发现类似的趋势,大多数DAPs具有疾病特异性。总共有150种下调蛋白在至少两种ND中共有,8种蛋白在4种或更多种疾病中均有下调(图5E)。这些蛋白包括NPTX2、两种SERPINE2亚型、VWF、SLC30A3、APOC1、ADI1和ETNPPL,它们与神经递质活性、血小板颗粒形成、胆固醇代谢和嘌呤代谢相关,提示神经退行性疾病中存在广泛的基本细胞功能紊乱(图5F-G)。相比之下,疾病特异性下调蛋白反映了不同ND中不同的分子缺陷(图5H)。
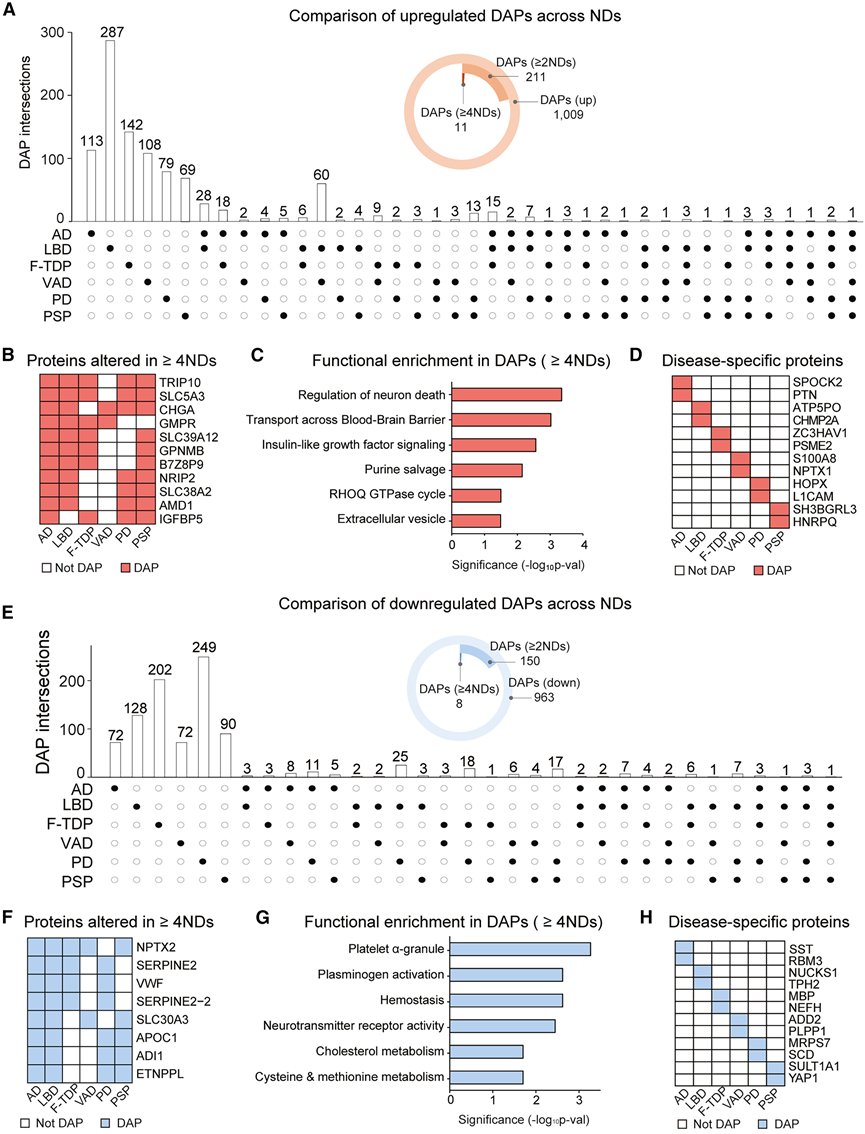
图5. ND中 DAP 的比较分析。
(A) UpSet 图比较 ND 中上调的 DAP。(B) 热图显示在至少四个ND中上调的蛋白质。(C) 使用 Enrichr 对至少在四种 ND 中上调的 DAP 进行功能富集分析。(D) 针对每种 ND 选择的疾病特异性上调蛋白的热图。(E) UpSet 图比较 NDs 中下调的 DAP。(F) 热图显示在至少四个ND中表达下调的蛋白质。(G) 对至少在四个 ND 中下调的 DAP 进行功能富集分析。(H) 针对每种 ND 选择的疾病特异性下调蛋白的热图。
06
共表达网络分析识别枢纽调控因子
为了揭示每种ND中共表达蛋白和关键枢纽蛋白的复杂网络,他们采用了多尺度嵌入式基因共表达网络分析(MEGENA)。在6种ND中,MEGENA平均识别出710个模块,每个数据集的模块数量在506到878之间。每个模块平均包含74个成员蛋白。然后,他们通过模块中DAP特征的富集情况来评估这些模块与其各自ND的相关性。AD、LBD和VAD网络中排名靠前的模块主要呈上调表达,而FTLD-TDP、PD和PSP网络中排名靠前的模块则主要呈下调表达(图6A)。
接下来,他们分析了这些排名靠前的模块在同种疾病队列中的保守性。对于阿尔茨海默病(AD),在3个独立的队列中,排名前30的模块中有超过80%是保守的,这与之前的报道一致。同样,在2个LBD队列中,排名前30的模块中有97%是保守的。然而,不同ND之间疾病相关模块的重叠度较低(平均约为50%)。在排名前30的AD模块中,分别有43%、40%、73%、27%和20%的模块与LBD、额颞叶痴呆-TDP(FTLD-TDP)、进行性核上性麻痹(PSP)、VAD和帕金森病(PD)重叠(图6 A)。接下来,他们通过GO 富集分析研究了每种 ND 中前 30 个模块的功能意义,结果显示,这些模块主要具有疾病特异性的生物学过程,疾病之间的重叠极少。
为了鉴定驱动这些共表达网络的关键调控因子,他们对MEGENA网络进行了关键驱动因子分析,以确定整体关键蛋白(GHP)。结果显示,AD、LBD、FTLD-TDP、PSP、VAD和PD分别有197、397、296、44、178和391个GHP(图6B)。具体而言,MDK在AD共表达网络中位列GHP前列(图6C),且MDK子网络激活,因为其许多连接节点在全蛋白组和不溶性蛋白组中均上调。Western blot进一步验证了MDK在AD脑组织中的积累,免疫染色证实了其在淀粉样斑块中的定位。该子网络中存在来自多个阿尔茨海默病风险基因的蛋白质,包括APOE、APP和CLU。总体而言,GHP也具有很强的疾病特异性,不同疾病之间的重叠有限(图6D)。
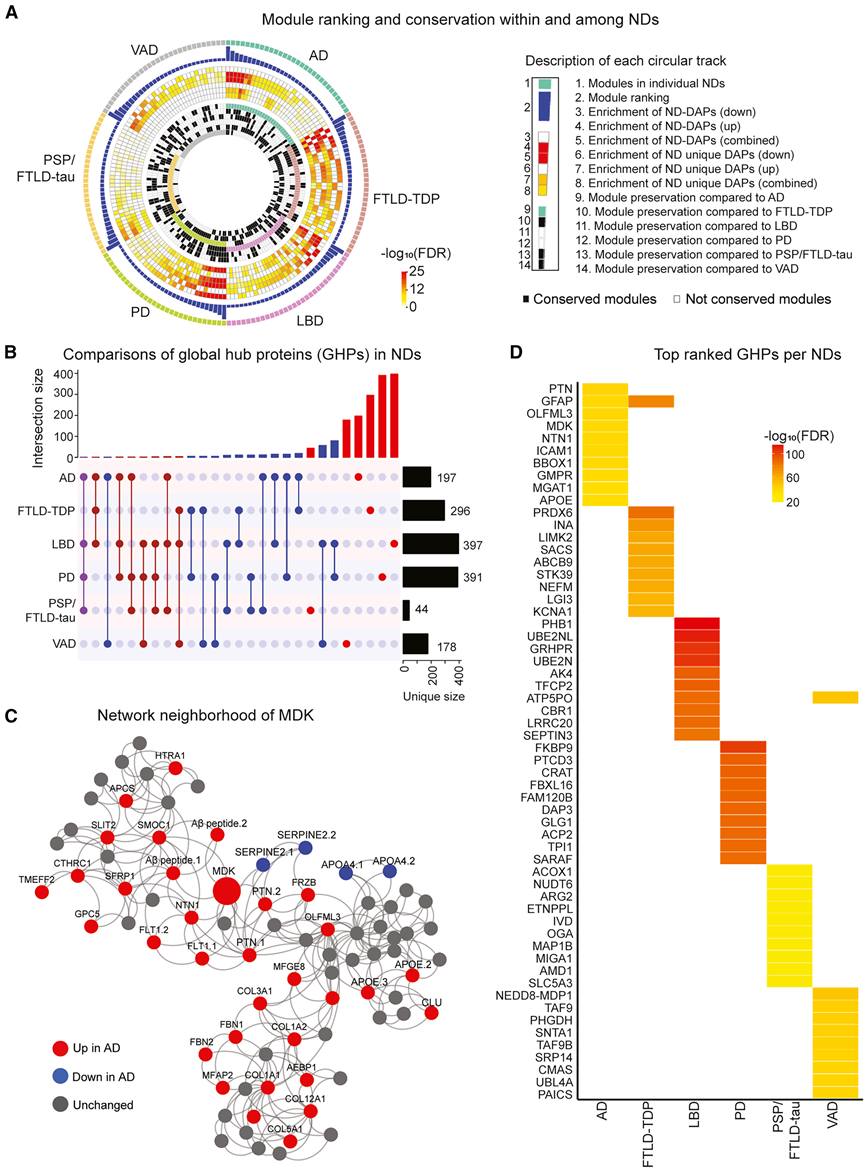
图6. ND中的蛋白质共表达网络和 GHP。
(A) Circos图可视化ND中模块的排序和保留情况。(B) GHP 特征的交集。(C) AD队列中GHP、MDK的网络邻域图。(D) 显示 ND 队列中排名最高的 GHP 的热图。
07
相关性分析揭示了与核心聚集蛋白的分子关联
为了探究已知的蛋白质聚集体如何与更广泛的蛋白质组变化相关联,他们将Aβ、pTau、SNCA、TDP-43和U1-70K(SNRNP70)与全蛋白组和不溶性蛋白组中的其他蛋白质进行了关联分析(图7A)。Aβ和pTau的相关蛋白质存在重叠,包括一些与U1-70K共有的蛋白质,这表明淀粉样蛋白、tau蛋白和剪接相关通路存在部分汇聚。相比之下,SNCA和TDP-43的相关蛋白质则大体不同,这与其在突触核蛋白病和TDP-43蛋白病中的作用相符。
随后,他们重点分析了与Aβ和pTau相关的单个蛋白质。在整个蛋白质组中,MDK、SMOC1、NTN1、SFRP1、FLT1和SLIT2是与Aβ相关性最高的蛋白质(图7B),这与之前的报道一致。类似地,SQSTM1、YPEL5、MAP2、RNPS1、SPOCK2和WDR26也是与pTau相关性最高的蛋白质(图7C)。YPEL5-WDR26-CTLH E3连接酶复合物的鉴定表明,它可能是参与pTau降解的潜在E3酶。进一步分析发现,一些蛋白质,例如SFRP1和SLIT2,与Aβ和pTau水平均相关(图7D),提示它们可能参与了这两种病理过程的关联。
不溶性蛋白质组直接反映了在ND病理过程中相关或共聚集的蛋白质。虽然不溶性组分中与Aβ和pTau相关的前20个蛋白质中有几个与整个蛋白质组重叠,例如Aβ相关的MDK和SFRP1,以及pTau相关的SPOCK2和SLIT2,但其他一些蛋白质则在不溶性蛋白质组中特异性富集,例如Aβ相关的U1-70K和CTHRC1,以及pTau相关的CCDC85B和SPIN1(图7E-G)。对不溶性蛋白质组中其他聚集蛋白(如SNCA、TDP-43和U1-70K)的进一步分析揭示了不同的相关性特征(图7H-J)。这些发现表明,不同形式的蛋白质聚集会引发独特的细胞反应,这可能与疾病特异性发病机制有关。
为了描绘疾病进展轨迹,他们对ND、对照组和轻度认知障碍(MCI,一种疾病前驱期)患者进行了伪谱系轨迹分析,识别出三个不同的谱系。谱系 1 连接了对照组、MCI、AD和FTLD-TDP患者;谱系 2 连接了对照组、MCI、AD、PSP和PD;谱系 3 涵盖了对照组、MCI、AD、PSP、VAD和LBD,突显了共同的和独特的分子进展通路。早期样本(对照组和 MCI)聚集在轨迹的起始位置,而 AD、FTLD-TDP、VAD 和 LBD 样本则更为分散,反映了分子异质性的增加。
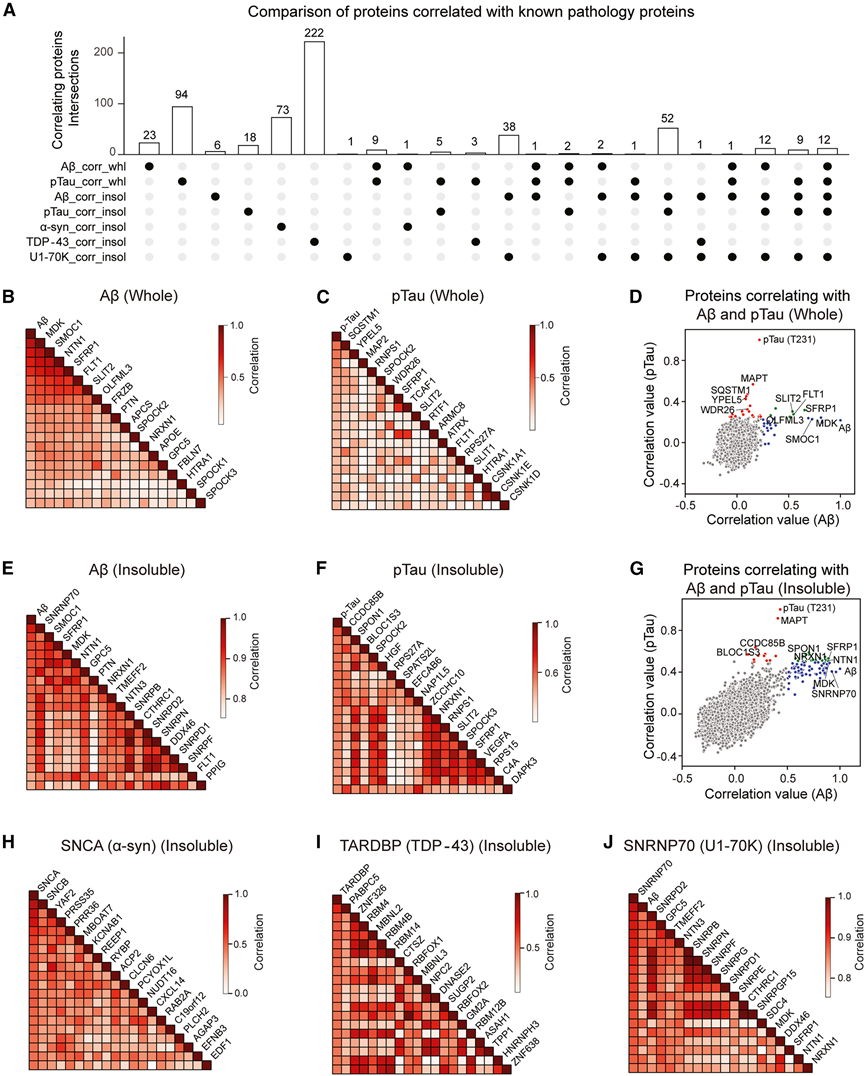
图7. 神经退行性疾病病理标志蛋白的相关性分析。
(A) 比较不同蛋白质组数据集(全蛋白质组和不溶性蛋白质组)中与 Aβ、pTau、SNCA、TDP-43 和 U1-70K 显著相关的蛋白质。(B-C) 在整个蛋白质组中与 Aβ 和 pTau 相关性最高的 20 种蛋白质。(D) 散点图显示蛋白质与Aβ和pTau的相关系数。(E-G) 对不溶性蛋白质组进行类似分析,显示相关系数 >0.4 的蛋白质。(H-J) 不溶性蛋白质组中与 SNCA 、TDP-43和 U1-70K相关性最高的 20 个蛋白质。
+ + + + + + + + + + +
结 论
本研究介绍了一种泛神经退行性疾病图谱,该图谱基于对2279例人脑样本的多层深度蛋白质组学分析构建而成,这些样本涵盖六种主要神经退行性疾病: AD、LBD、FTLD-TDP、PSP、VAD和PD。整合了全蛋白质组、不溶性蛋白质组以及翻译后修饰(磷酸化和泛素化)的数据,从而能够进行疾病内部和疾病之间的比较。疾病内部分析揭示了不同的分子亚型(例如,AD中有三种,LBD中有四种),揭示了失调的通路,并确定了排名靠前的蛋白质。疾病间比较揭示了ND中共同的改变,例如小胶质细胞和溶酶体激活中的GPNMB以及突触调节中的NPTX2,以及疾病特异性改变和蛋白质网络中的关键调节因子。
+ + + + +



 English
English


