文献解读|Cancer Cell(44.5):胰腺导管内乳头状肿瘤的多组学分析揭示了不同的模式和潜在的进展标志物
✦ +
+
论文ID
原名:Multi-omic profiling of intraductal papillary neoplasms of the pancreas reveals distinct patterns and potential markers of progression
译名:胰腺导管内乳头状肿瘤的多组学分析揭示了不同的模式和潜在的进展标志物
期刊:Cancer Cell
影响因子:44.5
发表时间:2025.08.28
DOI号:10.1016/j.ccell.2025.08.001.
背 景
胰腺癌是一种恶性肿瘤,五年生存率为 13% 。胰腺癌造成的死亡人数正在增加,据预测,到 2030 年,胰腺癌将成为美国和欧洲部分地区第二大癌症死亡原因。早期发现大大降低了其他类型癌症造成的死亡人数,低期胰腺癌患者的生存率明显高于晚期患者。然而,即使是小的侵袭性胰腺癌也可能致命。这意味着需要筛查非侵袭性前体病变,例如导管内乳头状肿瘤 (IPN),以更有效地预防胰腺癌造成的死亡。IPN 包括导管内乳头状黏液性肿瘤 (IPMN)、导管内嗜酸细胞乳头状肿瘤 (IOPN) 和导管内管状乳头状肿瘤 (ITPN),是临床上可检测到的宏观非侵袭性囊性病变,其中一些会发展为侵袭性胰腺癌。然而,胰腺囊肿的临床治疗面临错误分类、诊断不准确和过度治疗的挑战,这可能导致不必要的手术和并发症。因此,需要新的方法来准确诊断和分层 IPN 的进展风险。
实验设计
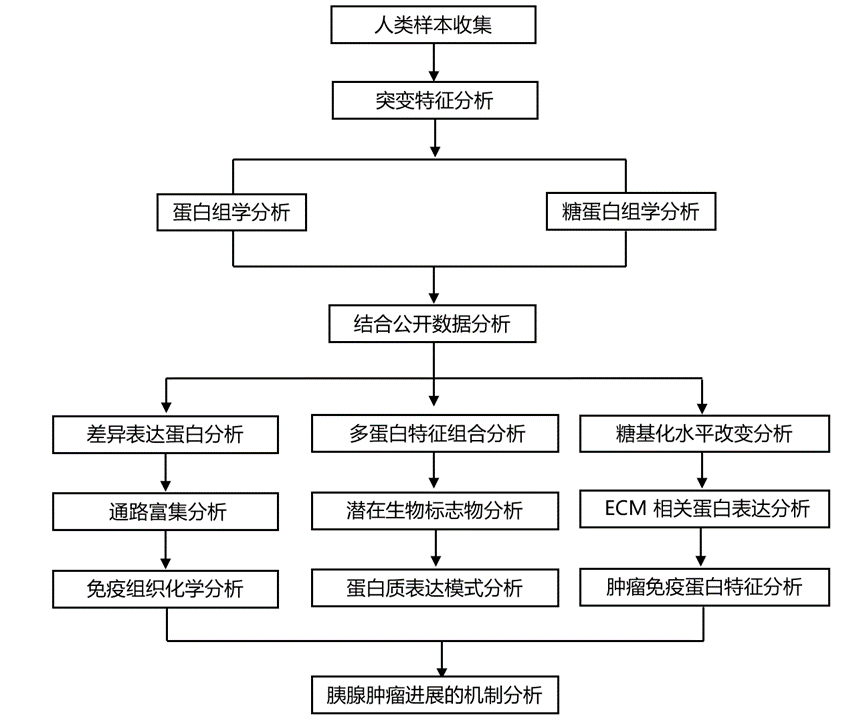
结 果
01
导管内乳头状肿瘤群的概况
研究团队进行患者样本进行分析,这些样本包括 69 个 IPN(64 个 IPMN 和 5 个 IOPN)、76 个大体正常导管组织(ND)和 32 个囊液样本(22 个来自匹配的 IPMN 患者,3 个匹配的 IOPN 患者,2 个来自无关的 IPMN 患者,5 个其他囊肿)(图 1A)。使用大体正常胰管作为对照至关重要,因为 IPN 具有导管分化,而大部分正常胰腺主要由腺泡细胞组成。从五个不同国家之一接受胰腺手术的患者身上收集了新鲜的病变组织和正常导管组织样本(图 1A),这些肿瘤中具有相似的体细胞突变基因(图1B)。具体而言,69 个 IPN 中有 37 个(54%)携带KRAS突变,69 个中有 32 个(47%)携带GNAS突变(图1C)。此外,在 33 个KRAS突变变异等位基因分数(VAF) > 0.075的 IPN 中,大多数携带常见的热点KRAS突变之一 G12D(35%)、G12R(19%)或 G12V(19%)(图 1C)。同样,在 VAF > 0.075 的GNAS突变的 IPN 中,大多数携带R201C(50%)或R201H(41%)的GNAS热点突变之一(图 1D)。GNAS R201C 主要见于肠型 IPMN,而胃型 IPMN 更常携带GNAS R201H 突变,胰胆型 IPMN 均未发现 GNAS 热点突变。
利用捕获离子迁移谱 (TIMS) 高通量蛋白质组学和糖蛋白质组学分析,他们在所有组织样本中鉴定并定量了总共 10246 种蛋白质和 22284种糖肽(包含 7041 个糖基化位点和 2924 种糖蛋白),在胰腺囊液样本中鉴定并定量了5314种蛋白质和7146种糖肽(图 1E)。
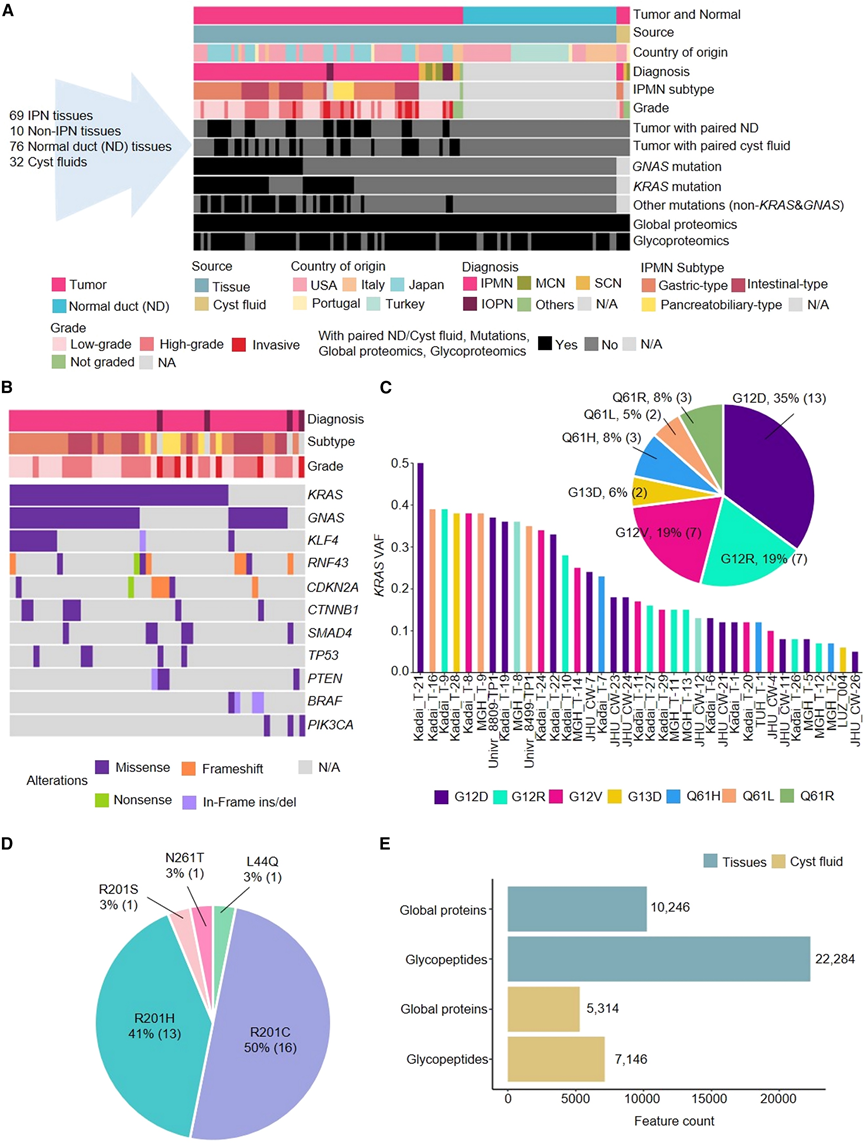
图1. 队列概况。
(A) 根据样本类型、组织学亚型、组织学等级和可用数据类型对队列进行分布。(B) 突变景观。(C) KRAS VAF 和KRAS热点突变的分布。(D) GNAS热点突变的分布。(E) 从整个队列的组织和囊液中鉴定出的总蛋白质和糖肽。
02
导管内乳头状黏液肿瘤的蛋白质组学分析
与 76 个 ND 相比,64 个 IPMN 中的 756 种蛋白质显著上调超过 1.5 倍,438 种蛋白质下调超过 1.5 倍(图 2A)。正如 IPMN 名称中包含“粘液”所暗示的那样,聚糖和多糖在这些肿瘤中显著上调。携带KRAS或GNAS热点突变的 IPMN表现出特别升高的糖基化和糖蛋白加工蛋白。KEGG通路富集分析显示,IPMN 蛋白质组在聚糖生物合成和代谢途径中显著富集,特别是粘蛋白型 O-聚糖生物合成(图2B)。确定了与宿主防御相关的免疫途径,其中免疫系统识别并消除抗体标记的病原体。
值得注意的是, IPMN 中过表达的 756 种蛋白质中有 88 种也在 PDAC 中上调。一些之前报道在低阶段 PDAC 中过表达的蛋白质,例如 S100P、SERPINB5 和 THBS2,在 IPMN 中也发生上调(图 2A)。ND中高度富集的蛋白质与正常的胰腺功能相关,包括蛋白质和脂肪酸的消化和吸收以及胰腺分泌(图 2B)。
IPN 和 PDAC 样本包含肿瘤细胞和非肿瘤细胞的混合物。肿瘤细胞过表达的蛋白质比基质中表达的蛋白质更有可能释放到囊液中。他们利用先前发布的 PDAC 肿瘤细胞和基质中差异表达基因的数据库来确定在 IPMN 组织中发现的每种过表达蛋白质最可能的区室。S100P 和 SERPINB5 等转录本已证明在 PDAC 肿瘤细胞中升高,而血小板反应蛋白 2 (THBS2) 和聚合免疫球蛋白受体 (PIGR) 等转录本已确定为在基质区室中升高。血小板反应蛋白在细胞-基质相互作用中发挥作用,据报道 PIGR 是免疫“热”肿瘤巢的标志物。接下来,他们通过免疫标记验证了所选蛋白质的表达,这不仅证实了它们的过表达,还揭示了它们定位的特定细胞区室。S100P 和 SERPINB5 抗体显示这些蛋白质在肿瘤细胞中过表达,而 THBS2 抗体标记了基质细胞(图2C)。
他们通过分析 24 个样本(包括 22 个匹配的 IPMN 组织样本(发现队列)(图 S2A)来探究 IPMN 中上调的蛋白质是否也存在于囊液中。IPMN 中上调的许多蛋白质在囊液样本中也有相似的表达模式。S100 蛋白家族成员,包括 S100A6、S100A11 和 S100P,在 IPMN 中高度表达,并在囊液样本中含量丰富。此外,CA-19-9 的主要载体蛋白 MUC5AC 也在囊液中高表达(图 S2B)。他们从独立队列中额外提取了 23 个囊液样本(10 个 SCN、6 个低级别 IPMN、7 个高级别 IPMN;验证队列),并观察到上述蛋白质的相似表达模式(图S2B)。
区分低度不典型增生的 IPMN、高度不典型增生的 IPMN 以及伴有浸润性癌的 IPMN 具有重要的临床意义。低度不典型增生的患者可以安全地随访,而高度不典型增生或伴有浸润性癌的 IPMN(以下分析中的“高度不典型增生”指高度不典型增生和伴有浸润性癌的 IPMN)通常需要手术切除。与低度不典型增生相比,高度不典型增生中共有 67 种蛋白质显著过表达。这些包括与糖基化生物合成相关的蛋白质,例如 PLOD3、GXYLT1、UAP1、GNE 和 B3GNT3。在这些聚糖合成蛋白中,GNE(葡萄糖胺(UDP-N-乙酰基)-2-表异构酶/N-乙酰甘露糖胺激酶)是糖蛋白上唾液酸修饰所需的关键酶,是糖蛋白稳定性和识别的关键修饰,并且与肿瘤进展有关。其他上调的蛋白质如 CDH17、AGPS、CDK5、LGALS9、CDCP1、TACSTD2 和 CDK13 参与影响肿瘤侵袭和进展的途径和网络。为了确定与高级别 IPMN 进展风险相关的蛋白质,他们重点研究了高级别 IPMN 相对于低级别 IPMN 和高级别 IPMN 相对于 ND 过表达的蛋白质(图2D)。据报道,其中一些上调的蛋白质,例如半乳糖凝集素 9(LGALS9)、多功能原胶原赖氨酸羟化酶和糖基转移酶 LH3(PLOD3)和胰岛素受体底物 2(IRS2),在 PDAC中上调(图S2C)。他们对 PLOD3、IRS2 和 LGALS9 进行了免疫组织化学标记,证实了它们在高级别 IPMN 中的表达升高(图S2D)。接下来,他们开发了基于激光显微切割 (LMD) 的蛋白质组学工作流程,该工作流程能够深度覆盖蛋白质组,鉴定出胰腺组织中的6000 多种蛋白质。在对来自三名患者的 12 对匹配的低级别和高级别 IPMN 样本进行独立 LMD 分析中,与囊液中的 SCN 样本相比,低级别和高级别 IPMN 样本中的 PLOD3 升高(图S2E-F)。
他们进一步通过受试者工作特征 (ROC) 分析评估了高级别 IPMN(与低级别 IPMN 相比)中过表达蛋白作为单个蛋白质特征及其不同组合的潜在临床效用。单独来看,PLOD3、LGALS9、IRS2、肿瘤相关钙信号转导蛋白 2(TACSTD2,也称为 Trop-2)和序列相似性家族 3 成员 D(FAM3D)在区分高级别和低级别 IPMN 方面具有良好的表现,曲线下面积 (AUC) 范围为 0.75 至 0.83(图 2E)。使用多蛋白质特征组可以提高性能,当结合 LGALS9 和 Trop-2 时,AUC 增加到 0.87(图 2F)。
不同组织学亚型的 IPMN 表现出不同的蛋白质表达模式。在胃型 IPMN 中,他们鉴定出 47 种与其他亚型 IPMN 相比上调的蛋白质。有趣的是,这 47 种蛋白质中有 23 种在低级别 IPMN 中相对于高级别 IPMN 也表现出上调。对于肠型 IPMN,有 57 种蛋白质上调,包括 CEACAM5、MUC2、GNE 和 CDH17(图S2G)。其中,与低级别 IPMN 相比,高级别 IPMN 中有 14 种蛋白质也上调。MUC2 参与肠型 IPMN 分化和进展的关键过程。这些结果提示了肿瘤级别/组织学亚型和进展的潜在生物标志物。
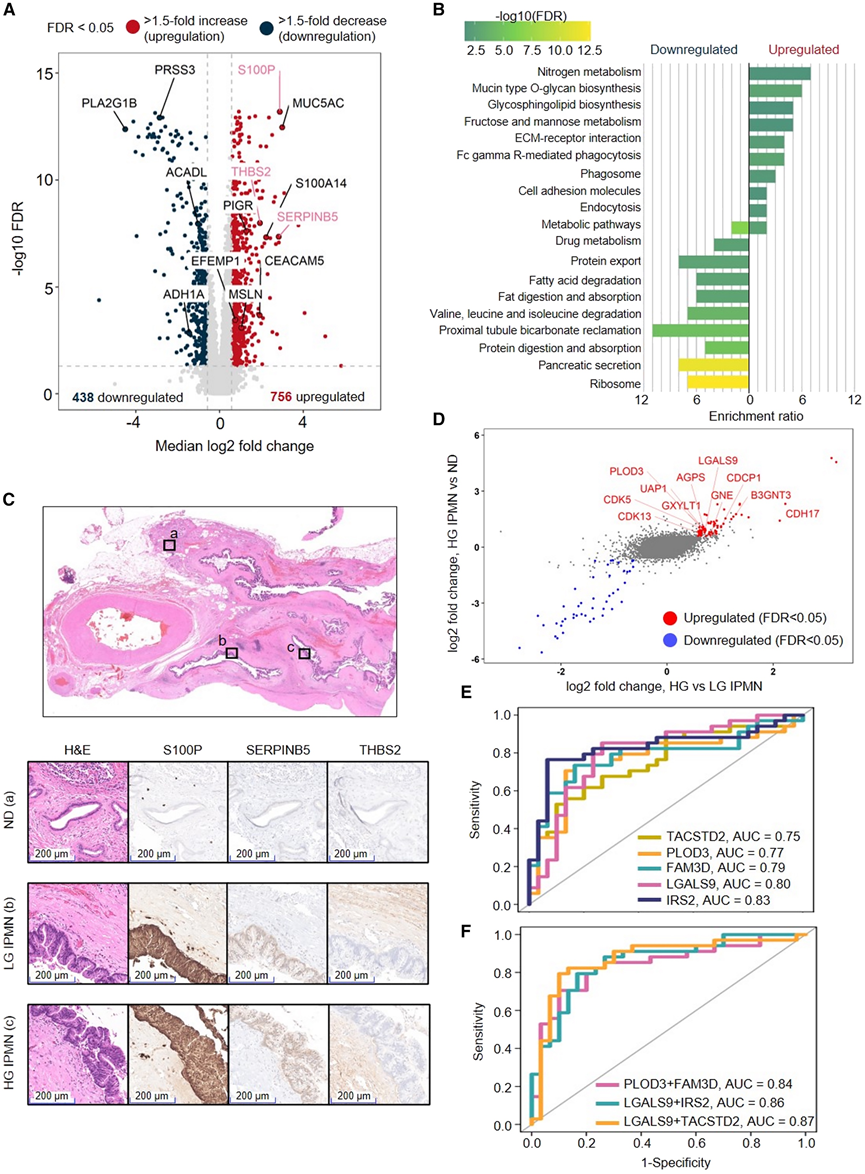
图2. IPMN和等级相关蛋白的鉴定和验证。
(A) 64例IPMN与76例正常导管组织(ND)的比较。(B) KEGG 通路富集了 IPMN 组织中相对于 ND 的上调和下调蛋白。(C) ND、低级别 (LG) IPMN 和高级别 (HG) IPMN 中 S100P、SERPINB5 和 THBS2 的 IHC 标记结果。(D) 34例HG IPMN中显著上调(红色)和下调(蓝色)的蛋白质。(E) 根据 ROC 分析,单个蛋白质显示出对 HG IPMN 检测的潜在临床实用性。(F) 多蛋白质组合提高了区分 HG IPMN 与 LG IPMN 的性能。
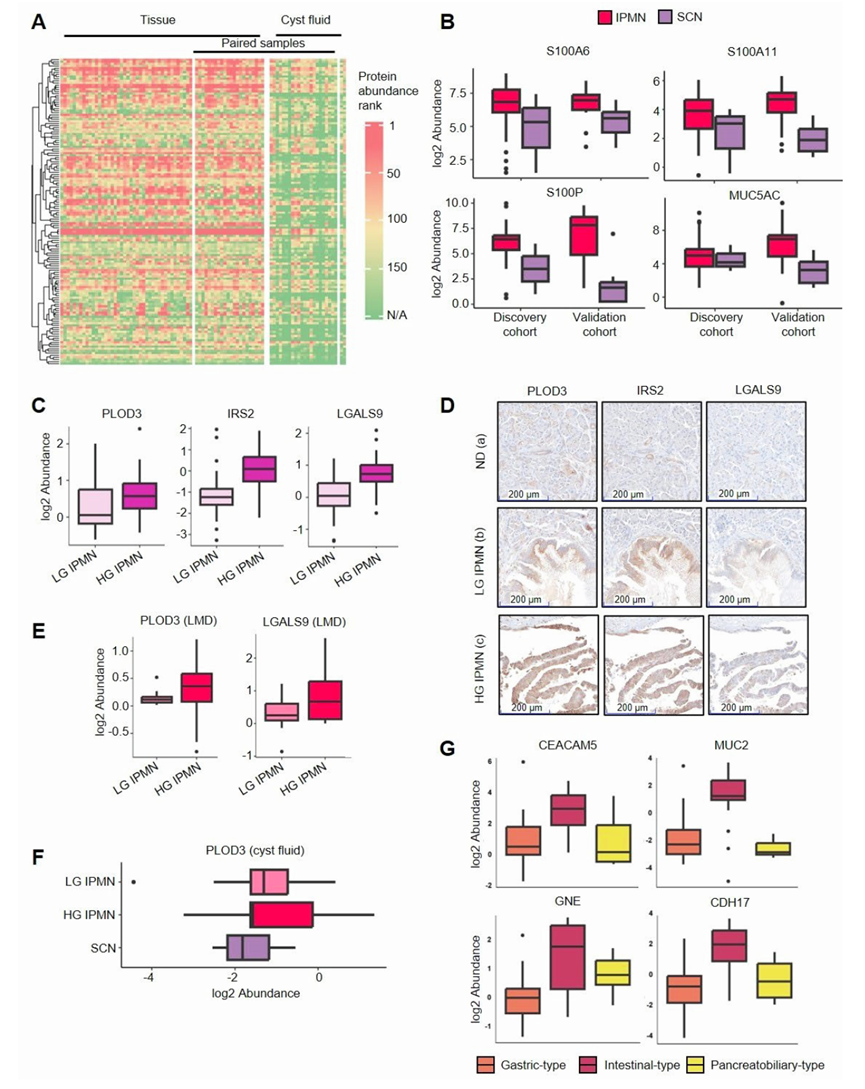
图S2. 不同IPMN亚型之间的比较。
(A) 与ND相比,IPMN中表达上调的蛋白有144种,且在囊液中也可检测到。(B) 囊液的发现队列(64个IPMN和3个SCN)和验证队列(13个IPMN和10个SCN)之间蛋白质表达谱分析。(C) 上调的蛋白分析。(D) 免疫组化染色分析。(E) PLOD3和LGALS9的LMD结果。(F) PLOD3的蛋白表达分析。(G) 与肠型和胰胆管型IPMN相比,胃型IPMN中高表达的蛋白。
03
导管内乳头状黏液肿瘤的糖蛋白表达谱
将 53 个 IPMN中鉴定出的糖肽与 66 个 ND中鉴定出的糖肽进行比较,结果显示,在 IPMN 中,2327 种糖肽显著上调超过 1.5 倍,1270 种糖肽下调超过 1.5 倍(图 3A)。细胞表面糖蛋白,例如 CEACAM5、整合素(ITGA5、ITGB1)和粘蛋白(包括 MUC1、MUC2、MUC4、MUC5AC、MUC5B、MUC6 和 MUC13)过表达可促进细胞粘附并在肿瘤表面形成保护屏障。此外,CD276、 CD47和其他先前发现为 PDAC 相关蛋白的免疫相关糖蛋白也在 IPMN 中上调。当仅考虑具有体细胞突变的 IPMN 时,观察到类似的糖蛋白表达模式。
超过130种蛋白质在整体蛋白质和糖蛋白水平上均上调。这些包括粘蛋白(MUC5AC、MUC6和MUC13)和粘蛋白型O-聚糖合成酶(C1GALT1C1、GALNT3、GALNT6和GCNT1)。细胞外基质(ECM)相互作用蛋白,例如CD47、整合素(ITGA2、ITGA9、ITGB4、ITGB6和ITGB8)和层粘连蛋白(LAMA3、LAMB3和LAMC2),也在整体蛋白质和糖蛋白水平上调,表明IPMN中的肿瘤微环境发生了变化。糖肽表达与整体蛋白质表达的比较表明,一些表达差异仅在糖肽水平观察到,而其他表达差异仅在蛋白质水平观察到(图 3B)。这一发现强调了表征蛋白质和糖肽的重要性,因为蛋白质表达可能并不总是等同于糖基化修饰。为了揭示 IPMN 中糖蛋白表达与蛋白质表达相比的独特模式,他们分析了整体蛋白质表达保持不变的上调或下调糖肽的生物学功能。一些上调的糖蛋白在整合素介导的信号传导和白细胞迁移中发挥作用,表明肿瘤微环境发生了变化(图 3C)。在整体蛋白质表达保持不变的情况下,IPMN 糖蛋白质组中的代谢相关功能也上调。下调的糖蛋白包括那些参与由钙粘蛋白介导的细胞间粘附的糖蛋白,钙粘蛋白是肿瘤进展过程中上皮间质转化(EMT)的重要调节剂。
比较 53 个 IPMN 与 69 个 ND 中的糖肽表达,发现许多与 IPMN 相关的糖蛋白变化。几种糖肽和糖肽组合在区分 IPMN 和 ND 时产生的平均自举 AUC > 0.7。包括上调和下调的糖肽在内,单个标记物(包括 CADM4-N262、FCGBP-N1317、LMF2-N489 和 PIGR-N469)的 AUC 在 0.71 到 0.87 之间(图 3D)。当标记物组合时,这些 AUC 提高到 0.9(图 3D)。
接下来,他们比较了 17 个携带KRAS和GNAS突变的 IPMN与 15 个野生型 IPMN的糖肽表达模式(下文和图中的“野生型 IPMN”是指未检测到任何体细胞突变的 IPMN)(图 3E)。与野生型 IPMN 相比,在同时携带KRAS和GNAS突变的IPMNS 中,有 71 种糖肽(涉及 56 种糖蛋白)表达上调。这些包括 O-糖基化酶,例如 C1GALT1C1、GALNT3、GALNT5、GCNT1 和 ST6GALNAC1。在上调的糖蛋白中还观察到与 PI3K-AKT 通路相关的糖蛋白,包括 EPHA2、ERBB3、ITGA6、MET 和 YWHAH,以及与无机离子(如Na+/K+、H+和Mg2+)相关的转运糖蛋白(ATP1A3、ATP6V0A2、CNNM4)。这些发现表明,携带KRAS或GNAS突变的 IPMN 中的肿瘤细胞会发生离子平衡的显著调整,并代谢重编程以满足高代谢需求。
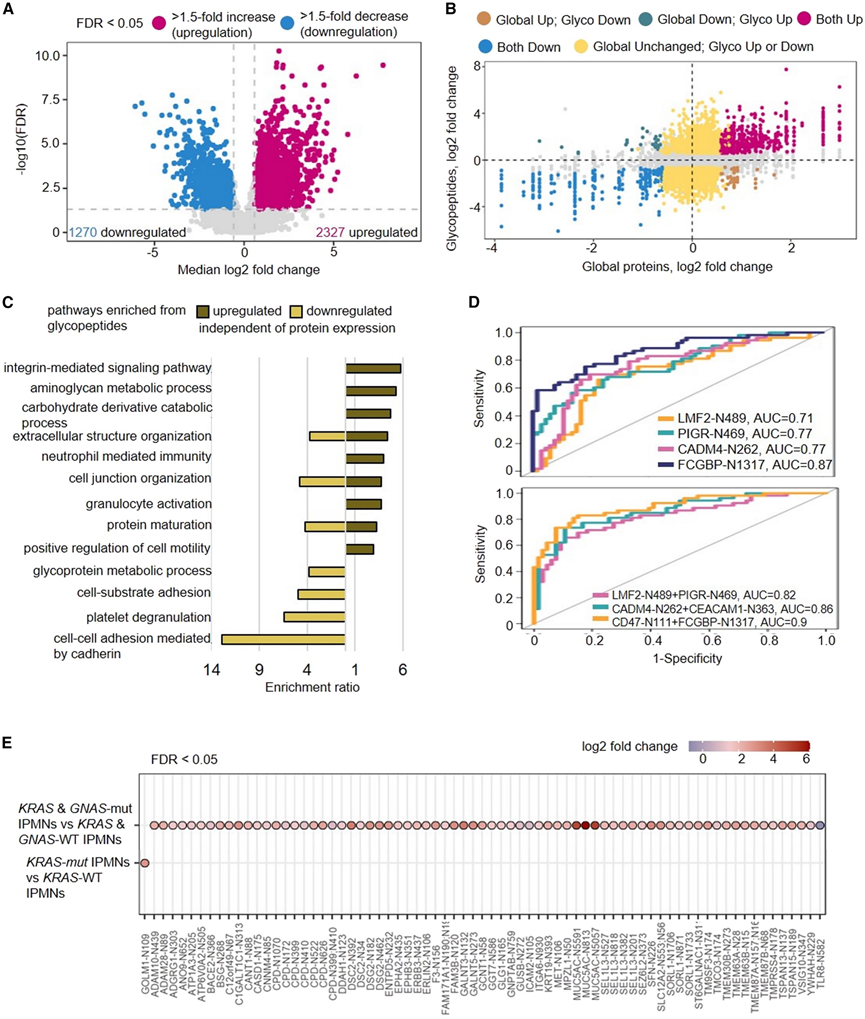
图3. IPMN 中的糖基化改变。
(A) 53例IPMN和66例ND中糖肽的比较。(B) 糖肽表达差异与整体蛋白质水平变化(IPMN 与 ND)的比较。(C) GO分析。(D) 能够区分 IPMN 和 ND 的单个糖肽和糖肽组合的示例。(E) 与KRAS 野生型 (WT) 和/或 GNAS 野生型 IPMN 相比,KRAS突变型IPMN或 KRAS和GNAS突变型 IPMN 中存在差异表达的糖肽。
04
肿瘤进展过程中 ECM 相关蛋白上调
他们从之前报道的一系列 PDAC 中选择了104个细胞最多的(肿瘤细胞 >15%)PDAC 和 43 个匹配的 NAT,并使用 DIA-MS对其进行了重新分析(图 4)。在主成分分析 (PCA) 中,PDAC、IPMN 和正常样本(ND 和 NAT)分别聚类(图 4A)。IPMN 样本聚类在 PDAC 和正常样本之间,证明IPMN 处于正常导管组织和浸润性癌症之间的过渡阶段。将104个 PDAC 中的蛋白质表达与匹配的 43 个 NAT 进行比较,发现在癌症中,1539 种蛋白质显著上调超过 1.5 倍,902 种蛋白质显著下调超过 1.5 倍(图S4A)。这些蛋白质中的绝大多数之前都已有报道,其中一些,例如 S100P、THBS2 和 SERPINB5,也在 IPMN 中过度表达(图 2A)。他们使用免疫组织化学验证了PDAC 组织中选定蛋白质(S100P、SERPINB5 和 THBS2)的表达和细胞定位(图 4B)。具体而言,S100P 和 SERPINB5 由侵袭性癌细胞表达,而 THBS2 主要由基质细胞表达。为了进一步研究哪些 IPMN 与 PDAC 更相关,他们鉴定了1670种在 PDAC 中与NAT和正常导管相比发生显著变化的蛋白质,并根据这些蛋白质计算了 PDAC 和 IPMN 之间的关联分数。八个 IPMN 与 PDAC 聚集在一起(图 4C),每个 IPMN 都具有相对较高的关联分数(≥ 0.88)。他们进一步检测了1670种蛋白质,发现 351 种蛋白质在 PDAC 中过表达,并且与其余 IPMN 相比,一些 IPMN 与 PDAC 分组在一起。这些蛋白质是 IPMN 进展的潜在标志物,因为它们在 PDAC 关联分数较高的 IPMN 中升高。在这 351 种蛋白质中,与侵袭和转移相关的蛋白质,例如细胞粘附、细胞骨架动力学、细胞运动和 ECM 蛋白值得进一步研究(图 4D)。上调的蛋白质包括 ECM 调节剂和胶原修饰酶(如 PLOD3)、成纤维细胞表达的 ECM 糖蛋白[如纤连蛋白 (FN1) 和腱蛋白 (TNC)]以及参与胶原纤维组织的蛋白聚糖[包括 lumican (LUM)],所有这些都与侵袭性肿瘤进展有关(图 4E)。大约 60 种 ECM 蛋白在从 IPMN 到 PDAC 的转变过程中表现出显著变化,包括 ECM 附属蛋白、ECM 糖蛋白、ECM 调节剂、蛋白聚糖和分泌因子(图 4F)。他们发现 106 种蛋白质在 PDAC 和 IPMN 中下调,与其他 IPMN 相比关联分数较高,并且这些蛋白质在代谢过程中富集(图 4D)。这 351 种上调蛋白质和 106 种下调蛋白质是早期检测具有高进展潜力的 IPMN 的潜在标志物。
IPMN 在形态上可分为三种亚型:胃型、肠型和胰胆型。此外,根据细胞结构异形性程度和有无相关侵袭性癌症,IPMN 可分为低度不典型增生、高度不典型增生和相关侵袭性癌症。他们将基于蛋白质组学的 NMF 亚型策略应用于 IPMN 和 PDAC,以探索肿瘤异质性并揭示进展特征。该分析显示了三个聚类(NMF1-3):NMF 1 完全由 PDAC 组成,NMF 2 包括一些 PDAC 和一些 IPMN,而 NMF 3 几乎完全由只有一个 PDAC 的 IPMN 组成(图S4B)。大多数(75%)伴有 PDAC 的 IPMN 聚集在 NMF 2 中。使用特征蛋白进行 KEGG 通路富集可区分这三个聚类(图S4C)。值得注意的是,NMF 3 在氨基糖代谢、代谢过程和胰腺分泌方面富集。NMF 3 中的几种粘蛋白糖基化相关酶,例如 UDP-半乳糖-4-差向异构酶 (GALE)、谷氨酰胺-果糖-6-磷酸氨基转移酶 1 (GFPT1)、GNE 和葡萄糖胺-磷酸 N-乙酰转移酶 1 (GNPNAT1),都参与氨基糖代谢。NMF 3 中发现的钠/钾转运 ATP 酶 (ATP1A1、ATP1B1) 和 ADP/ATP 转位酶 (SLC25A4) 是代谢过程中的关键参与者。NMF 3中发现的 Ras 相关蛋白 (RAB27B、RAB3D) 控制着分泌囊泡的成熟、运输和胞吐,在胰腺分泌中尤为突出。NMF 3 的这些独特特性表明,与粘蛋白聚糖合成增加和细胞外囊泡分泌相关的代谢过程发生了重编程。NMF 2 和 NMF 3 之间的主要差异包括 NMF 2 中胶原蛋白和基质蛋白(COL4A1、COL4A2、COL4A5、COL6A1、COL6A2、COL6A3、TNXB)升高,这些蛋白在 ECM-受体相互作用、PI3K-Akt 信号传导等途径中富集(图 4G)。这些发现强调了从 IPMN 到 PDAC 进展过程中 ECM 相互作用的重组。在 NMF1 中,明胶酶 A(MMP2)和 FN1,以及糖蛋白层粘连蛋白(LAMB3、LAMA3)和膜相关调节蛋白(ANXA2、ANXA5),突出了癌症中的细胞粘附和迁移途径以及蛋白多糖相互作用(图 4G)。
为了更好地了解不同 NMF聚类中微环境的动态和特征,他们对微环境蛋白质特征进行了分类,特别关注免疫蛋白质特征和免疫浸润程度(图 S4D)。由于各种 CD8+ T 细胞亚型的浸润,他们将 NMF 3 中的样本注释为“免疫热”肿瘤。完全由 PDAC 组成的 NMF 1 聚类表现出 CD8+幼稚 T 细胞和 CD8 + 中央记忆 T 细胞(CD8 + Tcm)的“冷”特征,这表明免疫反应耗尽,并可能导致侵袭性癌症的免疫逃避。这些免疫蛋白质特征为分子水平聚类增加了额外的价值,并有助于了解癌症进展。
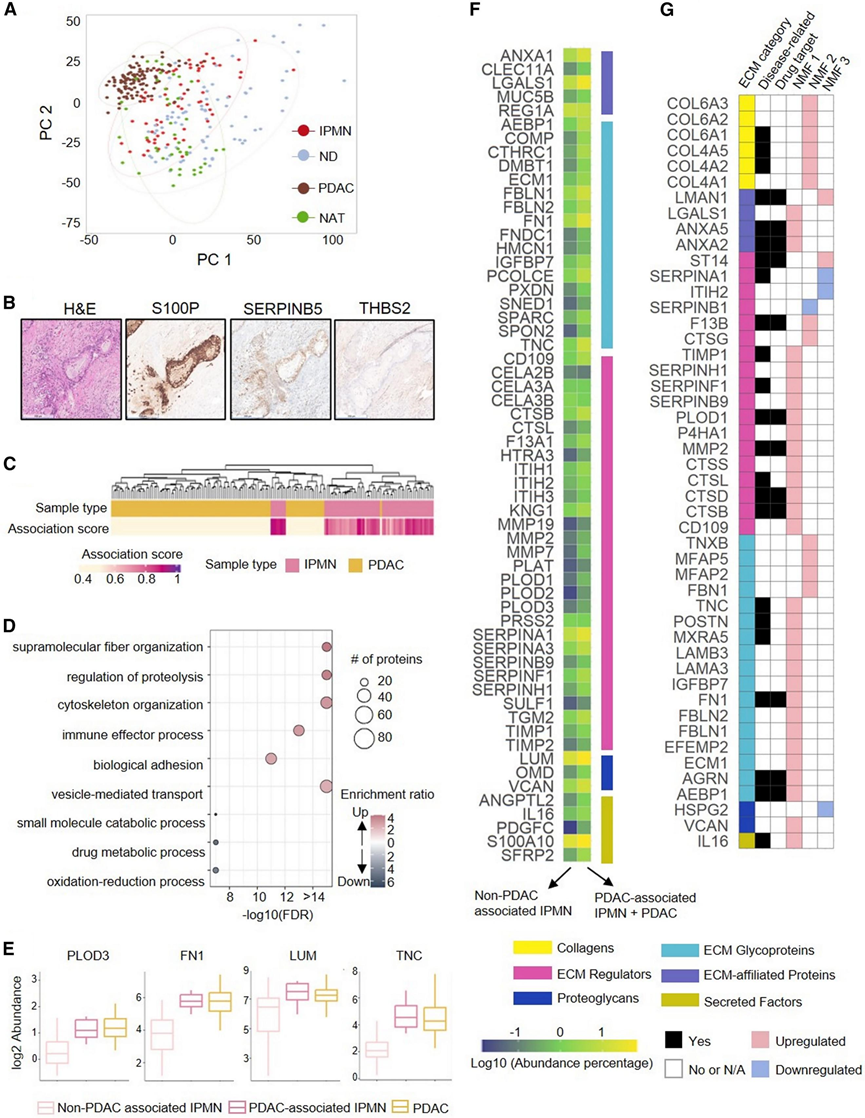
图4. IPMN与高肿瘤细胞密度PDAC的蛋白质组学比较。
(A) 整个队列的 PCA 分析。(B) 胰腺导管腺癌 (PDAC) 组织中 S100P、SERPINB5 和 THBS2 的 IHC 标记结果。(C) 104 个 PDAC 和 64 个 IPMN 的层次聚类。(D) GO分析。(E) 与 PDAC 分组的 PDAC 相关 IPMN与非 PDAC 相关 IPMN之间显示出显著变化的蛋白质示例。(F) 与非PDAC相关IPMN相比,PDAC相关的IPMN和PDAC具有丰富的ECM蛋白。(G) 根据人类蛋白质图谱,每个 NMF 聚类中与疾病相关和/或潜在药物靶点的 ECM 蛋白均有差异表达。
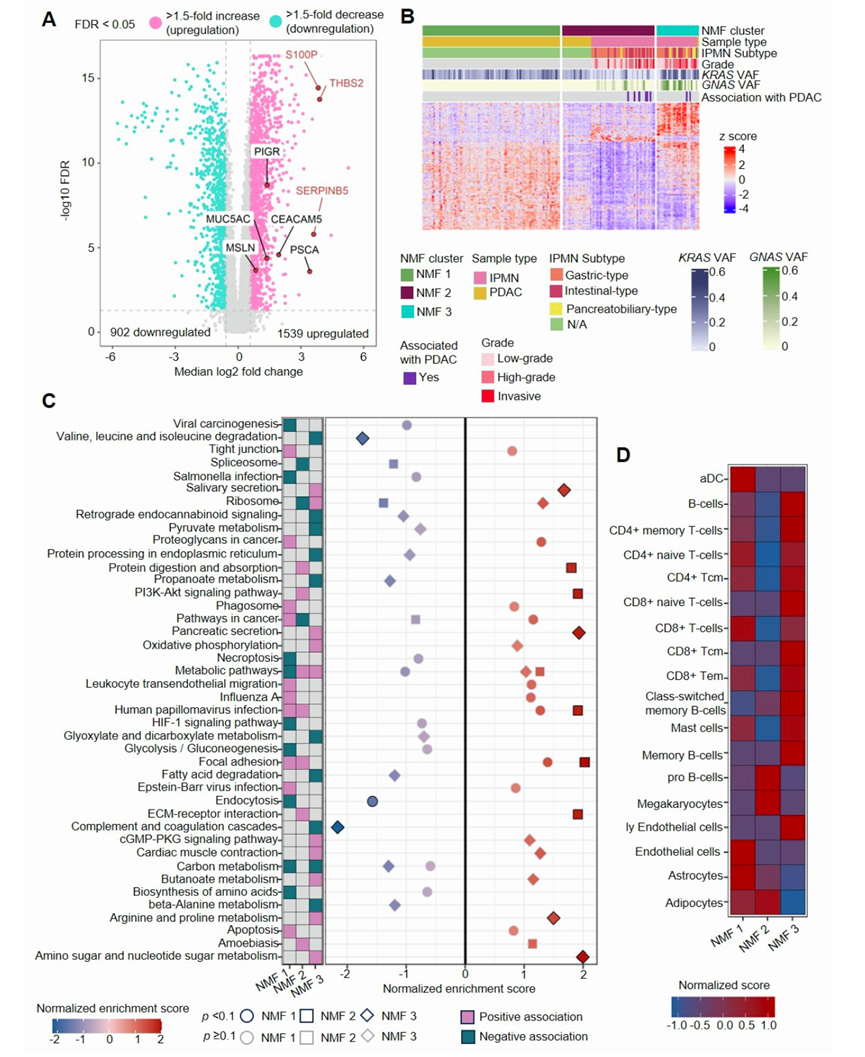
图S4. 高肿瘤细胞性IPMN和PDAC的蛋白质组学亚型分析。
(A)差异表达蛋白分析。(B)亚型聚类分析。(C) KEGG通路富集分析。(D) 基于xCell的基因特征对每个NMF聚类进行细胞类型富集。
+ + + + + + + + + + +
结 论
本研究分析了64例IPMN、55份囊液样本、104例PDAC以及各类正常样本。与低级别病变相比,高级别 IPMN 表现出糖基化和肿瘤进展通路的富集。本研究利用免疫标记和激光显微切割技术鉴定并验证了高级别 IPMN 相关蛋白,例如 PLOD3、IRS2、LGALS9 和 Trop-2,一些高级别相关蛋白也在胰腺囊液中检测到。与正常导管相比,在 IPMN 中观察到ECM蛋白的糖基化改变。此外,本研究还鉴定出一类具有PDAC样特征的IPMN,包括ECM蛋白表达升高。这些发现有助于深入了解进展相关标志物,并强调了这些蛋白在胰腺肿瘤中的诊断和治疗潜力。
+ + + + +



 English
English


