文献解读|Cancer Cell(44.5):生酮饮食通过促进肠道菌群产生的丁酸盐来抑制胶质瘤的进展
✦ +
+
论文ID
原名:Ketogenic diet inhibits glioma progression by promoting gut microbiota-derived butyrate production
译名:生酮饮食通过促进肠道菌群产生的丁酸盐来抑制胶质瘤的进展
期刊:Cancer Cell
影响因子:44.5
发表时间:2025.09.25
DOI号:10.1016/j.ccell.2025.09.002.
背 景
胶质瘤是脑部最常见的神经上皮肿瘤,约一半患者会发展为胶质母细胞瘤(GBM),这是最具破坏性的肿瘤类型。目前,GBM的治疗效果仍然有限,中位总生存期仅为15个月。鉴于预后如此糟糕,迫切需要开发新的治疗方法。近年来,以肠道菌群为靶点的疗法正逐渐成为个体化癌症治疗的新范式。研究表明,胶质瘤患者和健康对照组(HC)的肠道菌群结构存在显著差异。抗生素(ABX)诱导的肠道菌群耗竭会加剧临床前模型中胶质瘤的生长。然而,胶质瘤患者肠道菌群的确切特征,尤其是核心菌群,仍然是未知的。重要的是,肠道菌群如何影响神经胶质瘤生长的机制基础尚未阐明。
实验设计
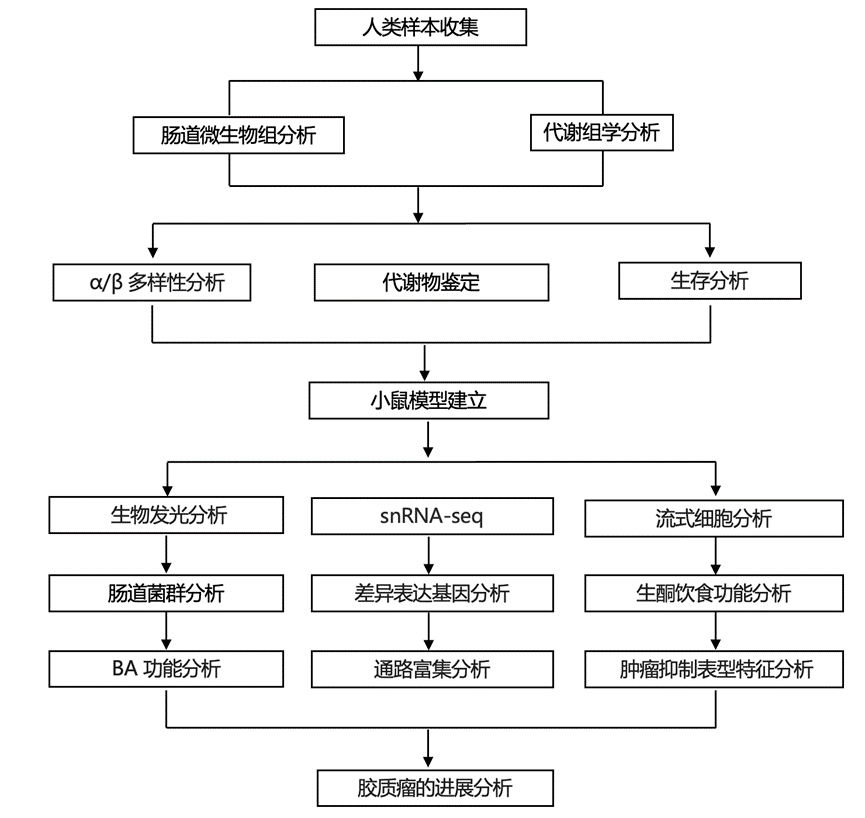
结 果
01
胶质瘤患者肠道菌群和代谢物的分析
研究团队收集了胶质瘤患者和HC样本进行了多组学分析,虽然α多样性相当,但β多样性分析显示两组人群的肠道菌群结构存在不同的聚类(图S1A-B)。相似性分析(ANOSIM)表明,胶质瘤患者和健康对照组之间的菌群组成差异大于各组内个体之间的差异(图S1C)。胶质瘤患者的芽孢杆菌门丰度降低,芽孢杆菌门/拟杆菌门(B:B)比值也降低,表明存在肠道菌群失调(图S1D-F)。值得注意的是,胶质瘤患者体内产生丁酸盐(BA)的细菌,尤其是罗斯氏菌属(Roseburia)、F. prausnitzii和R.faecis的丰度降低(图S1D-E)。其中,R.faecis的丰度下降幅度最大,且随着胶质瘤分级的升高而降低(图1A-B)。此外,随机森林模型和偏最小二乘判别分析(PLS-DA)的投影变量重要性(VIP)评分均显示,R.faecis是区分各组的最佳细菌(图1C-D)。受试者工作特征(ROC)曲线分析表明,R.faecis能够区分胶质瘤患者与HC以及低级别与高级别胶质瘤,曲线下面积(AUC)值为0.7917–0.8636(图1E)。相比之下,F. prausnitzii的丰度随胶质瘤分级的变化并不显著,且无法区分低级别和高级别胶质瘤患者,AUC值为0.5697-0.6476(图S1G-H)。此外,在科、属和种水平上,肠道菌群的变异均未受到性别、年龄或BMI的显著影响(图S1I)。因此,他们选择R. faecis作为后续实验中潜在的核心功能菌,以阐明肠道菌群在胶质瘤进展中的潜在机制。
靶向粪便代谢组学分析揭示了两组患者粪便中代谢谱的显著差异(图S1 J)。在粪便中共鉴定出145种代谢物,包括33种氨基酸(46.16%)、10种短链脂肪酸(SCFA)和11种碳水化合物(10.51%)(图S1 K)。胶质瘤患者粪便中52种代谢物的含量显著低于对照组(图1 F)。BA、乙酸和烟酸作为关键的鉴别指标,其中粪便中BA的含量差异最为显著(图1 G,图S1 L-N)。代谢物集富集分析(MSEA)表明,差异代谢物在粪便中显著富集于BA代谢相关通路(图S1O)。粪便BA含量下降最为显著,且与胶质瘤分级呈负相关(图1H-I)。ROC曲线分析显示,粪便BA能够区分胶质瘤患者与HC,以及区分低级别和高级别胶质瘤(AUC:0.8381-1)(图1J)。同时,粪便BA含量与R. faecis丰度呈正相关(图1K)。R. faecis和粪便BA联合检测能够更好地区分胶质瘤患者与健康对照组,AUC为0.9012,显著高于单独检测R. faecis或粪便BA(图S1P)。此外,血清BA水平的变化模式与粪便BA水平相似,均随肿瘤分级的升高而逐渐降低,并能够区分胶质瘤患者与健康对照组,以及区分低级别和高级别胶质瘤(AUC:0.8750–1)(图S1Q-S)。血清BA含量与R. faecis丰度呈正相关(图1L)。此外,他们发现R. faecis丰度、粪便或血清BA水平均与胶质瘤患者的生存时间呈正相关(图1M)。R.faecis丰度较高(≥0.44%)、粪便BA水平较高(≥8.2 μmol/g)或血清BA水平较高(≥0.2 μM)的患者生存期显著更长(图1N)。这些结果共同表明,BA产生菌(尤其是R. faeci)丰度的降低以及BA水平的下降是胶质瘤患者肠道菌群和代谢组的特征,这可能在胶质瘤的进展中发挥重要作用。
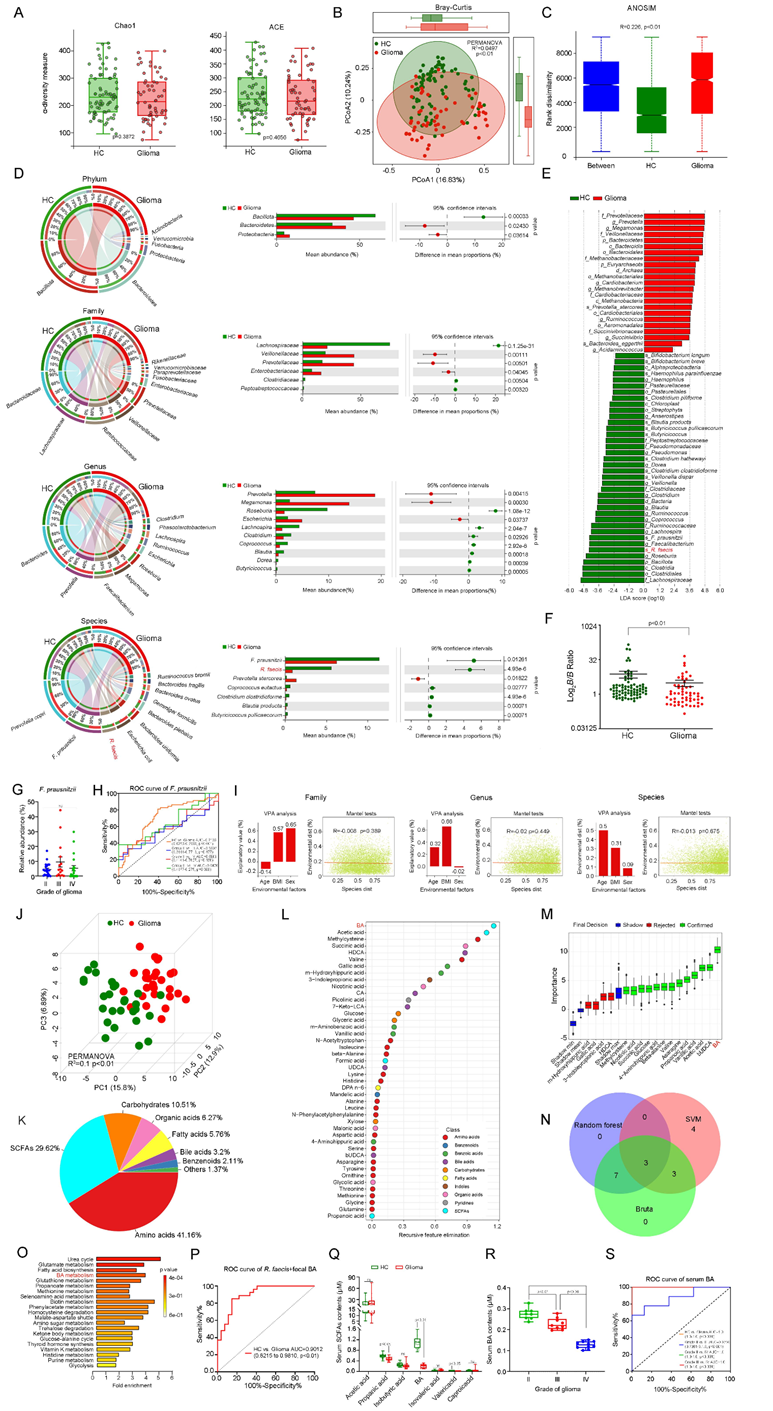
图S1. 胶质瘤患者的肠道微生物群和代谢组分析。
(A) α多样性分析。(B) β多样性的PCoA。(C) ANOSIM分析。(D) 主要肠道菌群的分布。(E) LDA分数。(F) B/B ratio 分析。(G) F. prausnitzii在不同级别胶质瘤患者中的丰度。(H) F.Prausnitzii在胶质瘤患者中的鉴别价值。(I) VPA分析和Mantel测试。(J) 粪便代谢物的OPLS-DA分析。(K) 不同种类粪便代谢产物的比例。(L-M) 通过粪便代谢组的SVM和Boruta识别出对区分胶质瘤患者和健康对照者贡献最大的生化数据。(N)维恩图。(O) 胶质瘤患者相关代谢物的MSEA。(P) ROC分析BA和R. faecis联合鉴别胶质瘤患者和HC的效能。(Q) 检测胶质瘤患者和HC血清SCFA含量。(R) 血清BA含量。(S)生存分析。
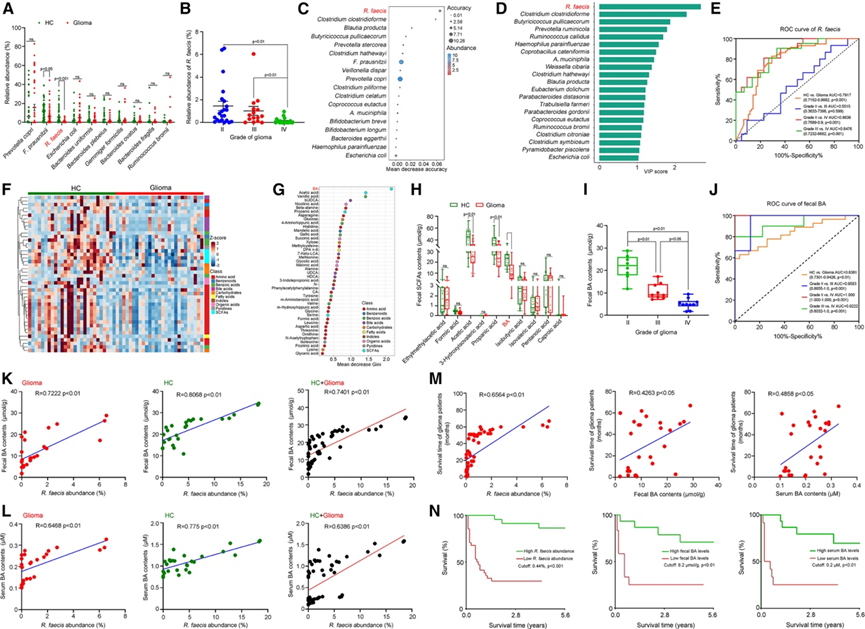
图1. 胶质瘤患者肠道菌群和代谢物分析。
(A) 健康对照组和胶质瘤患者中不同物种的丰度。(B) 不同级别胶质瘤中R. faecis的丰度。(C) 通过随机森林分类法鉴定的肠道微生物群物种。(D) PLS-DA 的 VIP 评分。(E) ROC 分析R. faecis在区分神经胶质瘤患者(N = 58)与健康对照组(N = 79)以及低级别与高级别病例(Ⅱ/Ⅲ/Ⅳ级)方面的表现。(F) 粪便中鉴定的代谢物(VIP ≥ 1,p < 0.05)的热图。(G) 粪便代谢组的随机森林分类。(H) 粪便代谢组的随机森林分类。(I) 不同级别胶质瘤患者的粪便BA含量。(J) ROC 分析粪便 BA 在区分胶质瘤患者与健康对照组(N = 27/组)以及低级别与高级别病例(Ⅱ/Ⅲ/Ⅳ级)方面的差异。(K) R.faecis丰度与粪便 BA之间的 Pearson 相关性。(L) R. faecis丰度和血清BA含量之间的Pearson 相关性。(M) 质瘤患者的生存时间分别与R. faecis丰度、粪便和血清 BA 水平之间的 Pearson 相关性。(N) 生存分析。
02
肠道菌群影响胶质瘤的发生发展
本研究使用了GL261小鼠胶质瘤模型、人1016B胶质瘤细胞来源的异种移植瘤模型,以及之前报道的通过颅内注射pTomo HRasV12-shp53慢病毒(LVRshp53)诱导GFAP-Cre小鼠胶质瘤发生的小鼠模型(称为LVRshp53小鼠)。同时,这些小鼠分别接受广谱抗生素治疗(称为ABX小鼠)或进行无菌饲养(称为GF小鼠)。ABX治疗显著降低了荷瘤C57BL/6J小鼠的细菌负荷,尤其是R. faecis的丰度。与仅接受对照饮食(CD)的C57BL/6J小鼠相比,ABX处理组的肿瘤体积和Ki67水平显著升高,生存期显著缩短;而ABX本身对小鼠生存期无影响(图2A-C)。在ABX处理的NOD-SCID小鼠和GF小鼠中也观察到了类似的结果(图2D-F),这些结果清楚地证实了肠道菌群在胶质瘤进展中发挥着重要作用。
此外,将GBM患者的粪便样本(GBM-FMT)和HC的粪便样本(HC-FMT)或R. faecis移植到GF小鼠体内(图2G)。灌胃后14天,GBM-FMT和HC-FMT GF小鼠的肠道菌群聚类模式不同,HC-FMT GF小鼠中Lachnospiraceae和R. faecis的丰度显著增加。这些结果表明,灌胃后4天,接受粪菌移植的小鼠能够重现胶质瘤患者和健康对照者的肠道菌群特征。HC-FMT和R. faecis移植均显著增加了R. faecis的丰度;然而,GBM-FMT没有显著影响。同时,HC-FMT或R. faecis显著降低了GF或ABX处理的C57BL/6J小鼠的肿瘤体积和Ki67水平,并延长了生存期;相比之下,GBM-FMT可能由于R.faecis水平未发生改变而未产生显著效果(图2G-L)。在ABX处理的NOD-SCID和LVRshp53小鼠中也观察到了类似的结果(图2 M-Q)。此外,R. faecis的丰度能够抑制C57BL/6J、NOD-SCID和LVRshp53小鼠的肿瘤进展(图2 J-Q)。这些数据表明,肠道菌群是调控胶质瘤进展的关键因素,其中R. faecis是一种核心功能菌。
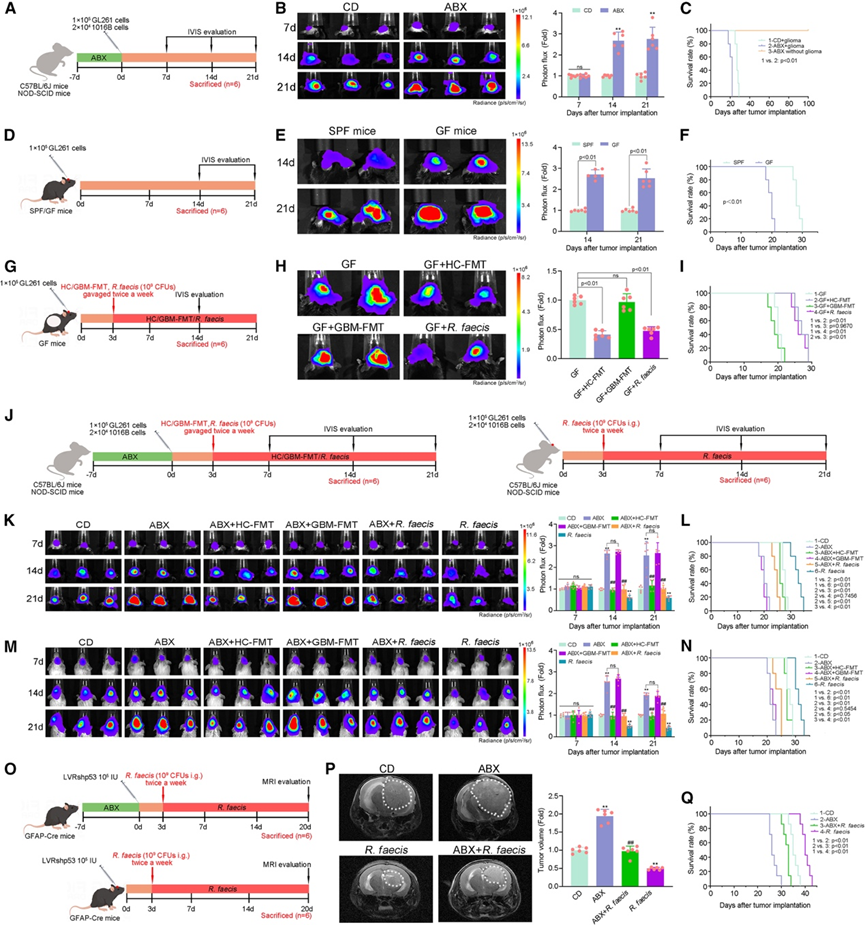
图2. 肠道菌群影响胶质瘤的发生发展。
(A, D, G, J, O)小鼠模型建立。(B, E, H, K, M) 生物发光图像及肿瘤定量分析。(C, F, I, L, N)生存分析。(P) 肿瘤的定量分析。(Q)生存分析。
03
BA是肠道菌群产生的具有抑癌功能性的代谢产物
GBM-FMT 和 HC-FMT GF 小鼠的粪便、血清和肿瘤组织代谢谱存在差异(图 3A)。GBM-FMT GF 小鼠的粪便、血清和肿瘤组织中分别有 8、9 和 16 种代谢物发生显著改变,其中BA是粪便中的关键鉴别代谢物(图3B)。同时,在 GBM-FMT GF 小鼠的粪便、血清和肿瘤组织中,BA代谢通路分别位列改变程度的前 2、1 和 4 位。此外,GBM-FMT GF 小鼠粪便、血清和肿瘤组织中的BA含量显著降低,且与R. faecis的丰度呈正相关(图3C-D)。HC -FMT 或R. faecis显著提高了GF或ABX小鼠粪便、血清和肿瘤中的BA水平(图3E)。SCFA混合物(67.5 mM乙酸、25.9 mM丙酸和40 mM BA)或100 mM BA均能以同等疗效逆转ABX诱导的肿瘤进展(图3F-H) 。BA还能改善ABX处理的LVRshp53或GF小鼠的胶质瘤进展(图3I-K)。最后,R. faecis移植显著提高了BA含量,而ABX可消除这种作用,停用ABX后补充BA可逆转ABX诱导的胶质瘤进展。此外, BA显著抑制了C57BL/6J、NOD-SCID和LVRshp53小鼠的肿瘤生长(图3F-K)。这些结果表明,BA可能是肠道菌群,特别是R. faecis产生的潜在功能性胶质瘤抑制代谢物。
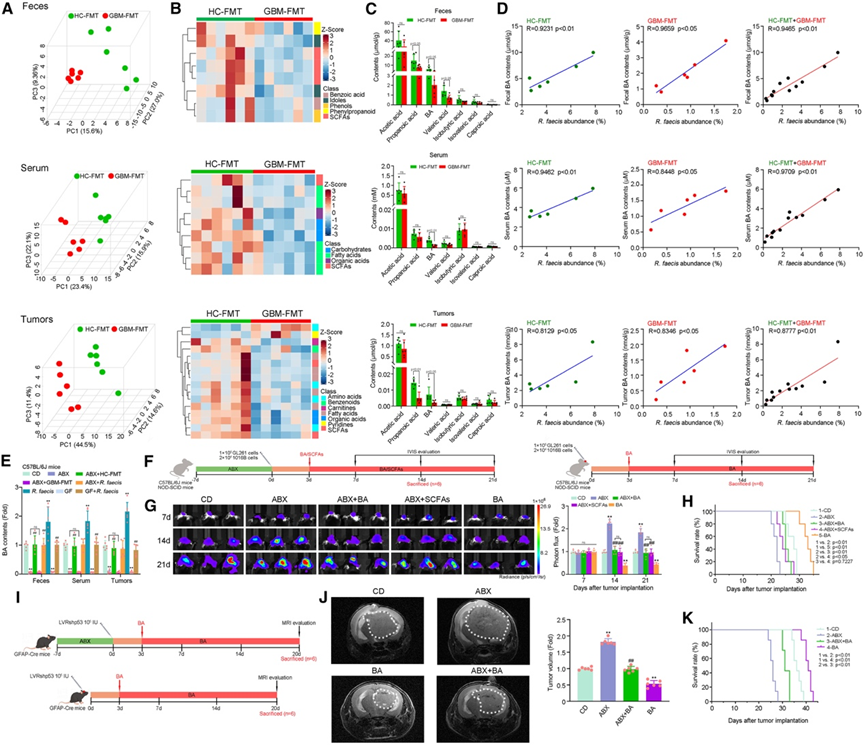
图3. BA是肠道菌群产生的具有抑癌功能性的代谢物。
(A) GBM-FMT 和 HC-FMT GF 小鼠粪便/血清/肿瘤中代谢物的 OPLS-DA。(B) GBM-FMT 和 HC-FMT GF 小鼠的粪便/血清/肿瘤中鉴定的代谢物的热图。(C)在 GBM-FMT 和 HC-FMT GF 小鼠的粪便/血清/肿瘤中检测到 SCFA水平。(D) HC-FMT、GBM-FMT 和 HC-FMT + GBM-FMT GF 小鼠的粪便/血清/肿瘤中 R. faecis丰度与 BA 含量之间的 Pearson 相关性。(E) 经指定处理的 C57BL/6J 小鼠的粪便/血清/肿瘤中的BA含量。(F) C57BL/6J 和 NOD-SCID 小鼠接受 SCFA 或 BA 治疗的方案。(G) 生物发光图像和肿瘤定量。(H) 生存分析。(I) LVRshp53 小鼠的治疗方案。(J) LVRshp53 小鼠的 T2 加权成像和肿瘤定量。(K) LVRshp53 小鼠的生存分析。
04
肠道菌群来源的BA促进了胶质瘤中小胶质细胞的抑癌表型
对GBM-FMT和HC-FMT GF小鼠的胶质瘤组织进行单细胞核转录组分析(snRNA-seq),共鉴定出52986个细胞核,将这些细胞核分为29个聚类,根据公开描述的标记物,将这些聚类注释为11种细胞类型,其中肿瘤相关巨噬细胞(TAM)是主要的免疫亚群(图4 A)。拷贝数变异(CNV)分析证实,聚类0为恶性细胞,具有大规模扩增和缺失,且CNV评分最高(图4 B)。在两组小鼠的肿瘤微环境中,除上皮细胞外,各细胞亚群的基因表达存在显著差异(图 S4 E),其中 GBM-FMT GF 小鼠的 TAM 表现出肿瘤促进基因(Spp1、Ccl12、Lgals1、Fkbp5和Il6rA)的上调(图 4 C)和促肿瘤通路(NOTCH 信号通路、G2M 检查点和IL-6-JAK-STAT3 信号通路)的富集(图 4 D),表明TAM可能在肠道菌群对胶质瘤进展的调控中发挥重要作用。
TAM 的重新聚类鉴定出 6 个亚群:小胶质细胞来源的 TAM(TAM-MG:MG1、MG2)、单核细胞来源的巨噬细胞(TAM-MDM:MDM1-3)和树突状细胞(DC)(图 4E)。MG1 表达稳态小胶质细胞标志物(P2ry12、Pros1和Tmem119),而 MG2 则表现出促肿瘤特征,包括恶性肿瘤相关基因(Ctsb、Spp1和Gpnmb)的上调以及促肿瘤通路(NOTCH 信号通路、G2/M 期检查点和 IL-6-JAK-STAT3 信号通路)的富集(图4F-G)。此外,两组小鼠中TAM-MG和TAM-MDM的比例相似。然而,在GBM-FMT GF小鼠中,MG2的比例增加,而MG1的比例则相应减少(图4 H)。两组小鼠中MG1、MG2、MDM1、MDM2和MDM3的基因表达存在显著差异。TAM-MG中差异表达基因(DEG)的数量远高于TAM-MDM;这些DEG在GBM-FMT GF小鼠中富集于促肿瘤通路。据报道,小胶质细胞中caspase-3 (CASP3) 的抑制会诱导一种肿瘤支持表型,其特征是IL-6增加和诱导型一氧化氮合酶 (iNOS) 减少,从而促进胶质瘤生长。在GBM-FMT GF小鼠的TAM-MG1和TAM-MG2中,IL-6分泌和产生的正调控通路富集,而一氧化氮合酶 (NOS) 生物合成过程的正调控和CASP3信号通路受到抑制。这些结果表明,肠道菌群可能通过改变TAM-MG的表型来调控胶质瘤的进展。
流式细胞分析进一步显示,GF或ABX小鼠中TAM-MG或TAM-MDM的数量保持不变,且不受HC-FMT、GBM-FMT、R. faecis或BA的影响。在GF或ABX小鼠的TAM-MG中检测到IL-6上调和iNOS下调,但在TAM-MDM中未检测到;这些变化可由HC-FMT、R. faecis或BA逆转(图4 I-L)。与CD组相比,R. faecis或BA降低了TAM-MG中IL-6的表达并增加了iNOS的表达(图4J-L)。此外,BA显著减弱了胶质瘤细胞系(GL261/C6/U251/1016B细胞)条件培养基(CM)诱导的BV2和HMC3细胞中IL-6升高和iNOS降低,且不影响细胞活力(图4M-N)。然而,BA未能逆转CM诱导的THP-1来源巨噬细胞(THP-1m)或RAW264.7细胞中IL-6升高或iNOS降低。最后,当在CX3CR1 CreERT2/+:R26iDTR /+小鼠中用他莫昔芬(TMX)和白喉毒素(DTX)特异性清除小胶质细胞时,ABX对胶质瘤生长和R. faecis的保护作用没有显著影响。R. faecis或BA对胶质瘤进展的抑制作用显著消失(图4 O-Q)。综上所述,这些数据表明肠道菌群,尤其是R. faecis,诱导胶质瘤中小胶质细胞而非TAM-MDM产生抑癌表型,而这种抑制作用是由BA介导的。
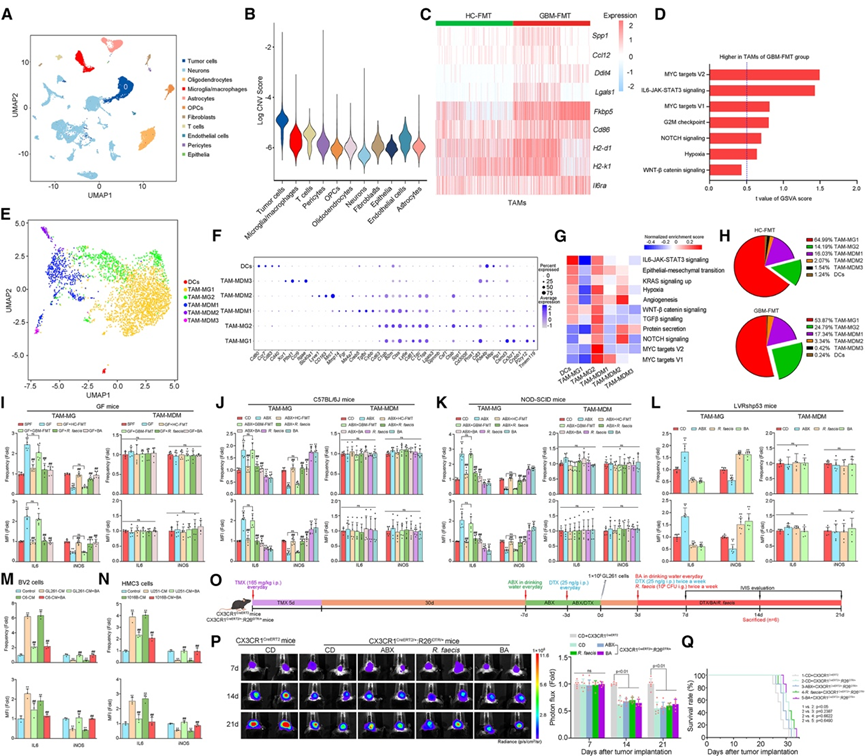
图4. 肠道菌群来源的 BA 促进胶质瘤中小胶质细胞的抑癌表型。
(A)SnRNA-seq 均匀流形近似和投影(UMAP)图,按在患有胶质瘤的 GBM-FMT 和 HC-FMT GF 小鼠的肿瘤中观察到的细胞类型着色。(B) 小提琴图显示不同细胞类型中 CNV 得分的分布。(C) 热图显示了 HC-FMT 和 GBM-FMT GF 小鼠 TAM 中所示恶性肿瘤相关基因的表达。(D) 根据 GBM-FMT GF 小鼠 TAM 中的基因集变异分析(GSVA)进行差异通路富集分析。(E) UMAP 图显示了 TAM 的聚类情况。(F) 散点图显示了用于识别细胞聚类类型的“特征”基因的表达情况。(G) 热图展示了 TAM-MG1/TAM-MG2/TAM-MDM1/TAM-MDM2/TAM-MDM3/DC 中的 GSVA 富集途径。(H) 热图展示了 TAM-MG1/TAM-MG2/TAM-MDM1/TAM-MDM2/TAM-MDM3/DC 中的 GSVA 富集途径。(I-L)流式细胞分析。(M-N) 检测BV2 细胞和HMC3 细胞中 IL-6/iNOS 的频率和 MFI。(P) 生物发光图像和肿瘤定量。(Q)生存分析。
05
BA通过激活胶质瘤中的CASP3促进小胶质细胞的肿瘤抑制表型
接下来,在无菌(GF)或抗生素切除(ABX)小鼠的TAM-MG(而非TAM-MDM)中,裂解型CASP3(C-CASP3)的表达显著降低,而HC-FMT、R. faecis或BA均可逆转这一现象(图5A-D)。同时,BA可恢复CM诱导的BV2和HMC3细胞中CASP3的失活,但对THP-1m或RAW264.7细胞无效。Casp3 /CASP3的小干扰RNA (siCasp3/CASP3)可降低CASP3的表达,从而消除BA诱导的CM处理的小胶质细胞中IL-6的降低和iNOS的升高(图5E-F)。BA抑制了小胶质细胞介导的胶质瘤细胞侵袭性、迁移性和存活率的增加,而siCasp3/CASP3则逆转了这种抑制作用(图5G-H)。此外,为了进一步明确小胶质细胞CASP3在肠道菌群中的作用或BA对体内TAM-MG的影响,他们使用了携带小胶质细胞特异性启动子Tmem119和Casp3短发夹RNA的腺相关病毒(AAV- Casp3)、AAV- Tmem119 -shRNA对照(AAV-CT)或CX3CR1CreERT2/+:CASP3flox/flox小鼠。在经 AAV-Casp3处理的 C57BL/6J 或经 TMX 处理的 CX3CR1CreERT2/+:CASP3flox/flox小鼠的 TAM-MG 中, Casp3表达发生特异性沉默(≥75%)。流式细胞分析显示,AAV- Casp3或 TMX 特异性地降低了 TAM-MG 中的 C-CASP3 表达,但在 TAM-MDM 中未观察到此现象(图5-L)。此外,ABX 未能促进 TAM-MG 中 IL-6 的表达,也未能抑制 iNOS 的表达,并且没有增强小胶质细胞 CASP3 缺陷小鼠的肿瘤生长或降低其存活率(图5I-R)。重要的是,在TAM-MG中,R. faecis或BA诱导的IL-6降低和iNOS升高以及肿瘤生长抑制作用,在小胶质细胞CASP3缺陷小鼠中均发生逆转,无论是否接受ABX治疗(图5 I-R)。这些结果表明,R. faecis或BA通过激活CASP3诱导小胶质细胞产生抑癌表型,从而抑制胶质瘤的进展。
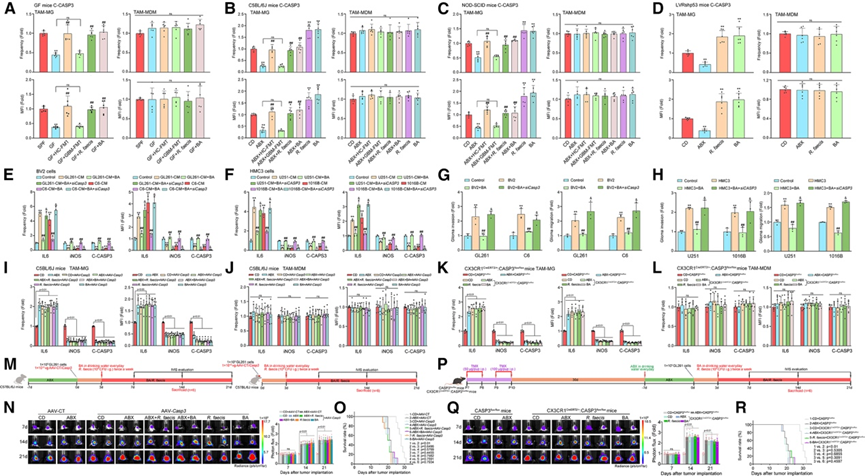
图5. BA通过激活胶质瘤中的CASP3促进小胶质细胞的肿瘤抑制表型。
(A-F)流式细胞分析。(I-J) 流式细胞分析 AAV- Casp3治疗的 C57BL/6J 小鼠(n = 6/组)中(I)TAM-MG 和(J)TAM-MDM 中 IL-6/iNOS/C-CASP3 的频率和 MFI。(K-L)流式细胞分析。(M, P)小鼠模型建立。(N, Q) 生物发光成像和肿瘤定量分析。(Q-R) 生存分析。
06
肠道菌群产生的胆汁酸介导了生酮饮食的抗胶质瘤作用
生酮饮食(KD)显著抑制了C57BL/6J和NOD-SCID小鼠的胶质瘤进展(图6A-C)。KD治疗的C57BL/6J胶质瘤小鼠的α多样性降低,β多样性分析显示两组小鼠肠道菌群组成存在分离的聚类。ANOSIM分析表明,CD组和KD组小鼠之间的菌群差异大于各组小鼠之间的差异。KD显著增加了C57BL/6J胶质瘤小鼠中Akkermansiaceae和A.muciniphila的丰度。在KD治疗的NOD-SCID胶质瘤小鼠中也观察到了类似的结果。此外,ABX消除了KD对C57BL/6J小鼠胶质瘤进展的有益作用(图6D-F)。ABX显著降低了A.muciniphila的丰度,而A.muciniphila或A. muciniphila + R. faecis可逆转这一现象;同时,R.faecis或A. muciniphila + R. faecis可增加KD + ABX处理的C57BL/6J小鼠中R. faecis的丰度。A. muciniphila、R.faecis或A. muciniphila + R. faecis可减弱ABX对KD在C57BL / 6J小鼠中抗胶质瘤作用的抑制作用(图6D-F)。与CD组相比,A.muciniphila + R. faecis可显著降低KD + ABX处理组小鼠的胶质瘤细胞密度。A. muciniphila+R. faecis同时提高了粘液杆菌和粪根瘤菌的丰度,从而抑制了C57BL/6J小鼠的神经胶质瘤生长(图6G-I)。在NOD-SCID小鼠中也观察到了类似的结果(图6J-K)。此外,KD 还能够抑制胶质瘤的进展,而这种抑制作用可由于ABX 消除;在 LVRshp53 小鼠中,A. muciniphila+R. faecis可减弱 ABX 诱导的 KD 抗胶质瘤作用的抑制(图6L-N)。在 KD 处理的 GF 小鼠中也获得了类似的结果(图6O-Q)。这些结果表明,KD 重塑了小鼠的肠道菌群,从而抑制了胶质瘤的进展,其中A. muciniphila似乎是核心功能菌。
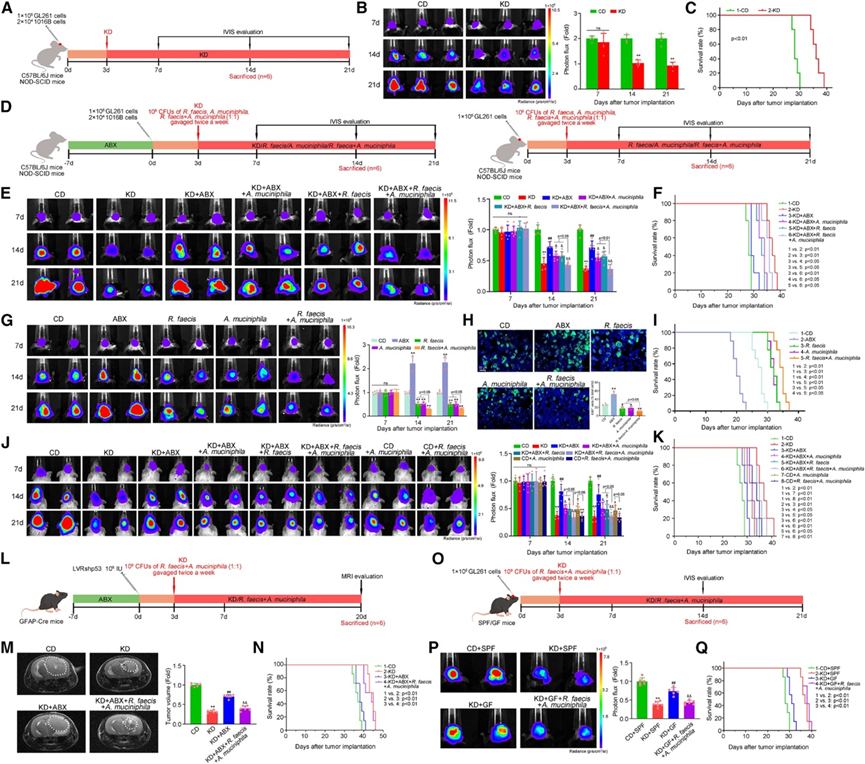
图6. KD 通过重塑肠道菌群抑制胶质瘤进展。
(A, D)小鼠模型建立。(B, E, G, J) 生物发光成像和肿瘤定量分析。(C, F, I, K) 对接受指定治疗的 C57BL/6J 和 NOD-SCID 小鼠进行生存分析。(H) 免疫荧光染色和定量分析。(L-O) LVRshp53 和 SPF/GF 小鼠的治疗方案。(M) 肿瘤的定量分析。(N, Q) 生存分析。(P) 生物发光图像和肿瘤定量。
07
肠道菌群产生的胆汁酸介导了生酮饮食的抗胶质瘤作用
β-羟基丁酸 (βHB) 在KD的抗胶质瘤作用中发挥重要作用,KD 显著提高了小鼠血清和肿瘤中的 βHB 含量,并降低了葡萄糖水平,而肠道或肝脏中的 βHB 水平无明显差异。重要的是,肠道菌群的缺失并不影响接受或未接受 KD 治疗的小鼠的 βHB 和葡萄糖含量。这些数据证实,肠道菌群对 KD 的抗胶质瘤作用的调节独立于 βHB 水平的改变。值得注意的是,CD 组、KD 组和 KD + ABX 组的粪便、血清和肿瘤组织的代谢谱存在差异(图 7 A-B),其中,BA是区分 KD 组和 CD 组粪便的主要指标。同时,在KD处理的C57BL/6J小鼠的粪便、血清和肿瘤样本中,BA含量显著升高,且与A. muciniphila的丰度呈正相关(图7C-D)。A.muciniphila、R . faecis或A.muciniphila + R. faecis均可提高KD + ABX联合治疗或未治疗小鼠粪便、血清和肿瘤组织中的BA水平(图7E-F)。此外,BA或SCFA混合物均能以相同的效率减弱ABX对KD抗胶质瘤作用的抑制(图7G-K)。BA也能减弱ABX对LVRshp53小鼠KD抗胶质瘤作用的抑制(图7L-N)。在KD处理的GF小鼠中也获得了类似的结果(图7 O-Q)。这些发现表明,BA可能是肠道菌群(尤其是A. muciniphila)产生的潜在功能性胶质瘤抑制代谢物,介导了KD对胶质瘤的保护作用。
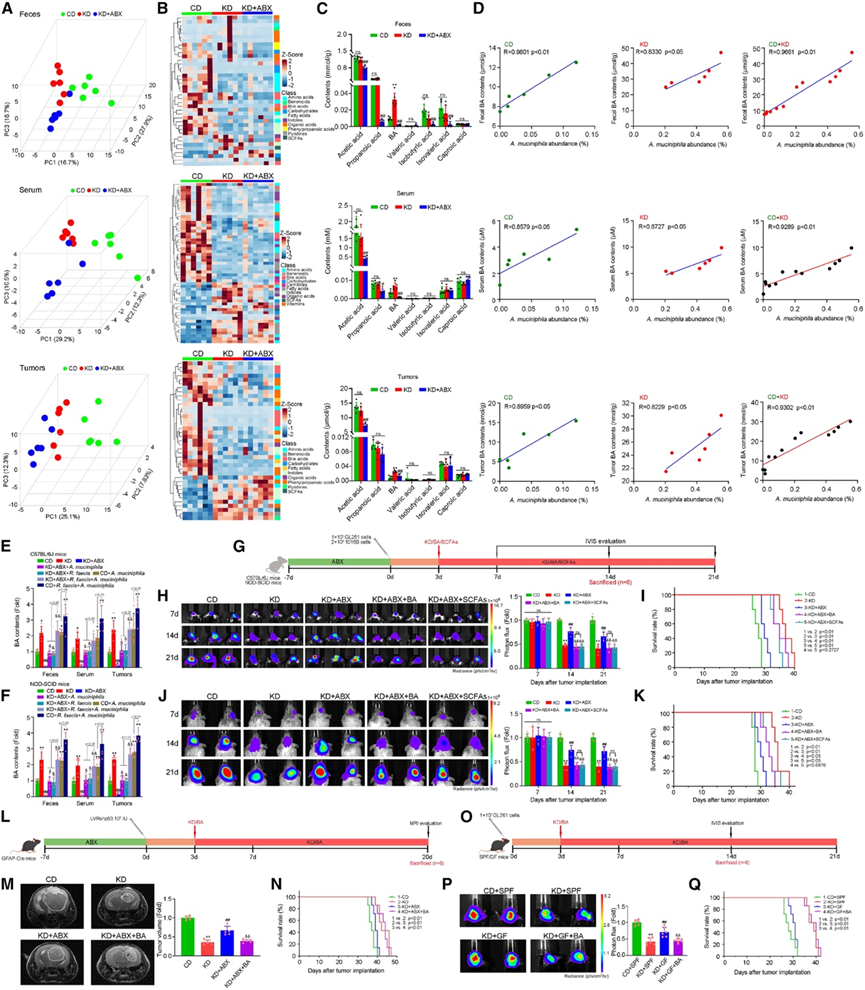
图7. 肠道菌群产生的胆汁酸介导了生酮饮食的抗胶质瘤作用。
(A) C57BL/6J 小鼠粪便/血清/肿瘤中代谢物的 OPLS-DA 分析。(B) C57BL/6J 小鼠粪便/血清/肿瘤中鉴定的代谢物。(C) 粪便/血清/肿瘤中检测到了 SCFA含量。(D) A. muciniphila丰度与 BA 含量之间的 Pearson 相关性。(E-F) 小鼠的粪便/血清/肿瘤中的BA含量。(G) C57BL/6J 和 NOD-SCID 小鼠的治疗方案。(H,J) 生物发光图像和肿瘤定量分析。(I-K) 生存分析。(L,O) 小鼠的治疗方案。(M) 肿瘤定量。(N, Q) 生存分析。(P) 生物发光图像和肿瘤定量。
08
KD通过激活CASP3促进小胶质细胞的肿瘤抑制表型
KD 可增加 TAM-MG 中 IL-6 的表达并降低 iNOS 的表达,而 ABX 或 GF 可消除这些作用。在 ABX 或 GF 小鼠中,A . muciniphila、R . faecis、A . muciniphila + R. faecis或BA 可恢复 KD 对 TAM-MG 的疗效。与 CD 组相比,A . muciniphila、R . faecis、A . muciniphila + R. faecis或BA仍能显著降低 TAM-MG 中 IL-6 的表达并增加 iNOS 的表达(图8A-B)。此外,当在 CX3CR1CreERT2/+:R26iDTR/+小鼠中特异性敲除小胶质细胞时,KD 无法抑制胶质瘤的进展(图8E-G)。同时,ABX对KD处理的小鼠的胶质瘤生长没有显著影响;A . muciniphila + R. faecis或BA也未能抑制ABX + KD处理的CX3CR1CreERT2/+:R26iDTR/+小鼠的胶质瘤生长(图8E-G)。这些数据表明,小胶质细胞在KD对胶质瘤进展的保护作用中发挥了重要作用。
最后,KD恢复了C-CASP3的表达,而ABX或GF则逆转了这一恢复,A . muciniphila、R . faecis、A . muciniphila + R. faecis或BA显著减弱了ABX引起的KD诱导的CASP3激活的抑制作用(图8H-K)。与CD组相比,A . muciniphila、R . faecis、A . muciniphila + R. faecis在TAM-MG中仍然显著激活了CASP3(图8H-I)。此外,KD对胶质瘤的保护作用显著减弱,ABX未能进一步抑制KD在小胶质细胞CASP3缺陷小鼠中的抗胶质瘤作用;同时,A . muciniphila + R. faecis或BA对KD+ABX处理的CASP3缺陷型小胶质细胞小鼠的胶质瘤生长也无任何有益作用(图8 L-U)。这些数据表明,KD通过CASP3依赖的方式诱导小胶质细胞产生抑瘤表型,从而抑制胶质瘤生长。
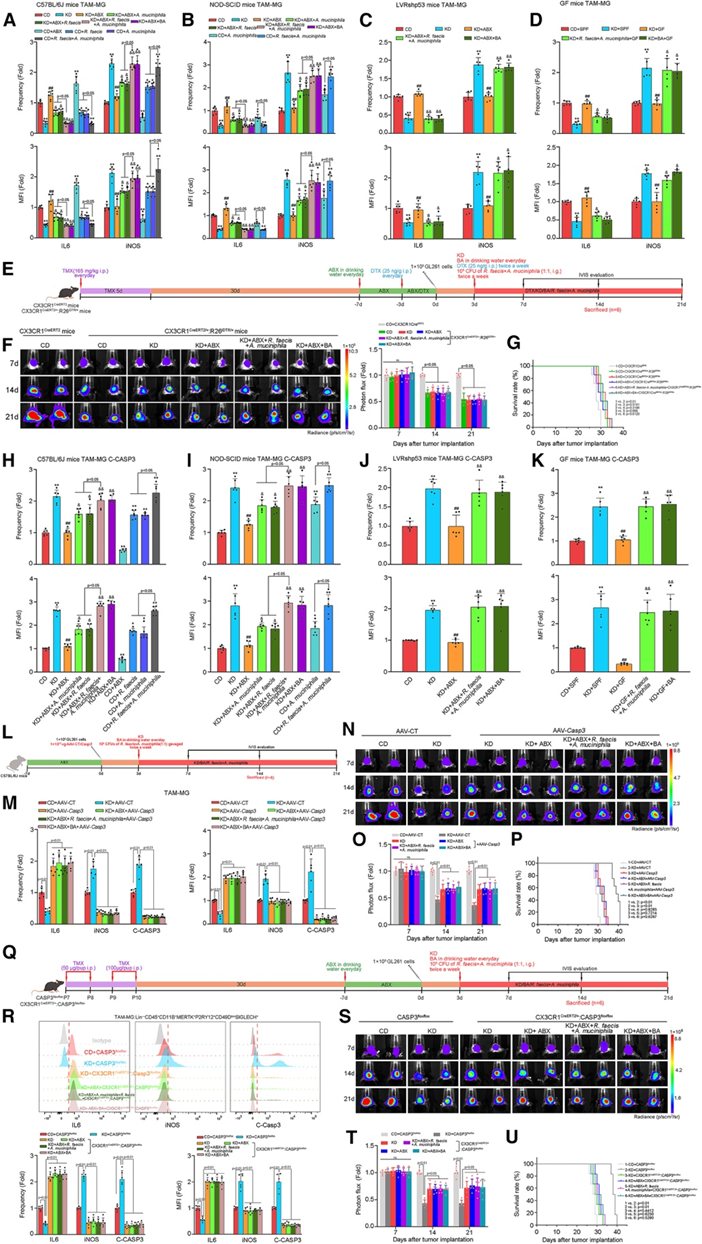
图8. KD通过激活CASP3促进小胶质细胞的肿瘤抑制表型,从而抑制胶质瘤进展。
(A-D)流式细胞分析。(E) 小鼠的治疗方案。(F) 肿瘤生物发光图像和定量分析。(G) 小鼠的生存分析。(H-K) 流式细胞分析。(L,Q) C57BL/6J 小鼠注射 AAV- Casp3 的治疗方案。(M, R)流式细胞分析。(N, O, S, T) 生物发光图像和肿瘤定量。(P, U) 生存分析。
+ + + + + + + + + + +
结 论
本研究发现胶质瘤患者表现出独特的肠道菌群特征,其丁酸产生菌(尤其是R. faecis)丰度降低,同时丁酸水平也降低。值得注意的是,KD能够重塑肠道菌群,特别是以黏蛋白-2依赖的方式富集A. muciniphila,提高丁酸生成,并激活小胶质细胞中的caspase-3。这些变化促进了抗肿瘤小胶质细胞表型的形成,最终抑制小鼠胶质瘤的进展。A . muciniphila + R. faecis能够恢复生酮饮食诱导的小胶质细胞caspase-3激活,并恢复经抗生素治疗或无菌小鼠的小胶质细胞的抗肿瘤表型。这些发现表明,通过KD或补充丁酸盐来靶向肠道菌群可能是治疗胶质瘤的有效策略
+ + + + +



 English
English


