文献解读 |Signal Transduct Target Ther ( 52.8 ):时空多组学分析揭示了 NAD 依赖性免疫抑制微环境如何触发早期胃癌
✦ +
+
论文ID
原名:Spatiotemporal multi-omics analysis uncovers NAD-dependent immunosuppressive niche triggering early gastric cancer
译名:时空多组学分析揭示了NAD依赖性免疫抑制微环境如何触发早期胃癌
期刊:Signal Transduction and Targeted Therapy
影响因子:52.8
发表时间:2025.09.22
DOI号:DOI: 10.1038/s41392-025-02390-w
背 景
胃癌(GC)是全球第五大常见恶性肿瘤,也是全球癌症相关死亡的第三大主要原因,其特点是病程复杂,涉及多个阶段和多种病因。根据Correa级联模型(正常→慢性胃炎→萎缩性胃炎→肠化生→异型增生→癌),约占所有胃癌病例80%的肠型胃癌的发生发展遵循一定的顺序。肠化生(IM)是早期胃癌(EGC)癌变过程中的关键前体,代表着从良性到恶性状态的转折点。已知诊断为慢性萎缩性胃炎或肠化生的患者每年进展为胃癌的风险较高,估计分别为0.1%和0.25%。虽然在理解这些癌前病变的组织病理学特征和分子机制方面取得了显著进展,但目前仍严重缺乏预防或逆转这些病变的临床有效策略,这凸显了早期干预和预防方面存在的关键且持续的差距。
实验设计
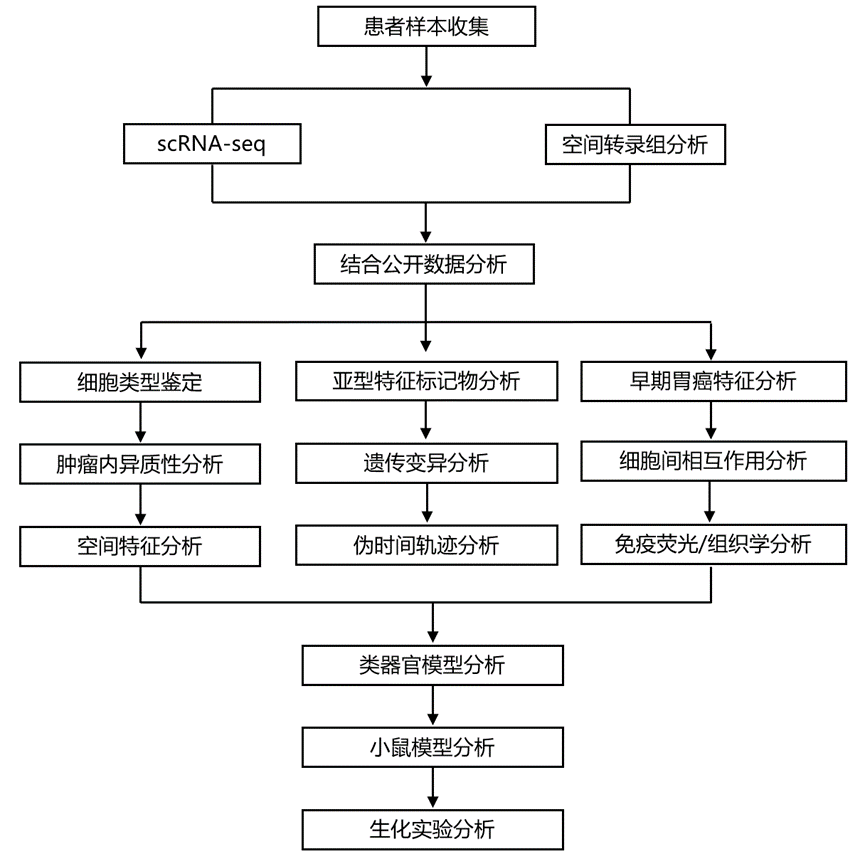
结 果
01
ESD标本中EGC的时空图谱
为了全面阐明EGC的发生发展过程,尤其关注癌前状态的细胞组成和空间组织及其在人类EGC发生中的作用,研究团队收集了内镜黏膜下剥离术(ESD)标本。这些标本包括T1期EGC(T)、癌前状态(包括间变性、轻度至中度不典型增生)以及匹配的正常组织(N)(图1a)。共有9例未经任何治疗的个体的9个组织样本符合纳入标准,其中8个标本(P1-P8)采用空间转录组(ST)技术进行分析,3对组织(P4-P6)和1个非配对标本(P9)采用单细胞转录组(scRNA-seq)技术进行分析。
为了阐明感兴趣的细胞微环境内的异质性细胞群,他们分析了四位患者相邻位点匹配区域的scRNA-seq谱,共获得16839个细胞。为了确定EGC肿瘤微环境(TME)的细胞组成,他们对这些细胞进行了基于图的聚类分析,根据已知的标记基因或特定细胞类型特有的表达基因,鉴定出12种不同的细胞类型。这些细胞类型包括上皮细胞、B细胞、CD4+ T细胞、CD8+ T细胞、NK细胞、NKT细胞、髓系细胞、内皮细胞、肥大细胞、成纤维细胞、浆细胞和MKI67 +祖细胞(图1b-c)。此外,经典标记物的免疫荧光染色证实了这些细胞类型在整个 EGC 发育过程中的异质性浸润,突显了 TME 的复杂性和动态性。
在ST分析中,每个包含两个连续切片的切片平均包含约2500个斑点。每个斑点直径为55 μm,在捕获区域内包含约8-20个细胞,便于观察从正常组织到肿瘤的连续病理过程(6.5 mm × 6.5 mm)。共对来自8名患者的20063个斑点进行了测序,中位数为约6500个独特的分子标识符和2600个基因。病理学家对每个ST数据的H&E图像区域进行了标记,共识别出20个不同的组织学区域(图1d)。为了探索肿瘤内异质性,他们应用了先前开发的AI模型stMVC,该模型整合了基因表达、空间位置、H&E图像和组织学注释。stMVC采用多视图学习来导出空间域嵌入,从而捕捉疾病进展的结构和时间特征。分析表明,stMVC可以描绘出不同空间域的发展轨迹。例如,在P1中,他们观察到从正常组织到癌变的轨迹:聚类12/8⟶聚类11⟶聚类6⟶聚类16⟶聚类1,聚类11代表 IM 和 EGC 组织之间的过渡状态。在其他七名患者中也观察到了类似的模式(图1d-f)。
所有患者N、IM和T区域中各种细胞类型经典标记基因的空间分布表明细胞微环境的异质性(图1g)。使用GraphST 分析每个斑点中12种不同细胞类型的比例,他们发现所有主要细胞类型均存在于8例患者的肿瘤、邻近IM和正常区域中。然而,这些细胞类型的浸润程度在不同区域间差异显著,提示这些细胞类型在早期胃癌(EGC)进展的不同阶段发挥着不同的作用(图1h)。
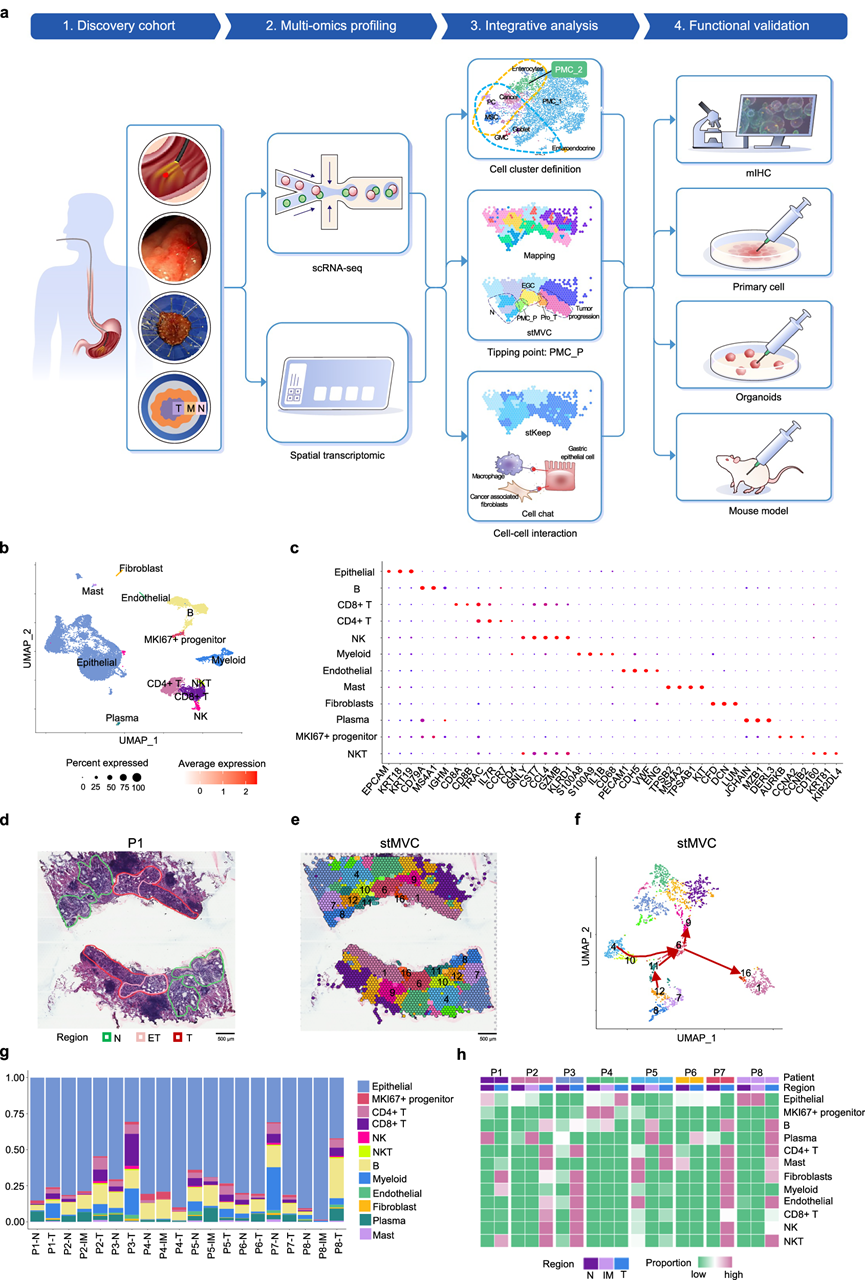
图1. 早期胃病变的时空异质性,涵盖正常、肠化生 (IM) 和肿瘤 (T) 区域。
(a) 实验流程示意图。(b) UMAP 可视化,显示 12 种主要细胞类型。(c) 散点图展示了已识别细胞类型中经典标记基因的表达情况。(d) 患者 P1 的H &E 染色空间转录组学 (ST) 切片,并标注了组织学注释的正常 (N)、早期肿瘤 (ET) 和肿瘤 (T) 区域。(e) 基于患者 P1 的ST数据,通过 stMVC 算法识别的空间域。(f) 患者 P1 的 ST 数据中,通过 stMVC 识别的空间域的 UMAP 可视化。(g) 柱状图显示了来自 8 例患者的 ST 数据中,通过 scRNA-seq 鉴定的 12 种细胞类型在各组织学区域中的比例。(h) 热图显示了来自 8 例患者的 ST 数据中,通过 scRNA-seq 鉴定的 12 种细胞类型在 20 个组织学注释区域中的富集情况。
02
早期胃癌进展过程中上皮细胞亚型的变化
对全部 10474 个上皮细胞进行亚聚类分析后,他们鉴定了九种不同的亚型,其中大多数亚型都具有已知的标记物(图2a-b)。这些亚型包括:胃窦基底腺黏液细胞(GMC,表达MUC6、PGC和LIPF)、小窝黏液细胞(PMC_1,以GKN1和TFF1为标记)、肠内分泌细胞(CHGA、GAST和SST)、肠细胞(FABP1 / 2和APOA1)、杯状细胞(ILTN1、TFF3和SPINK4)以及增殖细胞(PC,表达PRR11和MKI67)。其他细胞聚类鉴定为癌细胞(CCK和CLIC3)、化生干细胞样细胞(MSC,由OLFM4和GAL定义)以及 PMC_2 细胞。与 PMC_1 细胞相比,PMC_2 细胞的独特之处在于其炎症信号IL1B表达水平升高,同时ITGA2和干细胞相关标志物(如PHLDA1)的表达水平也较高。
每种亚型都与特定的功能通路相关。GMC与肠道免疫网络相关,参与IgA的产生;PMC_1细胞参与TGF-β信号通路和类固醇代谢;肠内分泌细胞参与花生四烯酸代谢和GPCR配体结合;肠上皮细胞与PI3K-AKT信号通路相关,杯状细胞则受PTEN信号通路调控。值得注意的是,PMC_2细胞在白细胞介素-10信号通路、TP53转录网络、MAPK信号通路、IL2-STAT5信号通路以及通过NFκB介导的TNF-α信号通路中均表现出活性;PC细胞与MHC II类抗原呈递、细胞周期以及TP53活性的调控相关;MSCs则表现出多种功能,包括糖酵解和糖异生、RUNX1介导的转录调控、对化学应激的反应以及RUNX3表达的调控。癌细胞参与先天免疫反应、白细胞介素信号传导、B2 类分泌家族受体、中性粒细胞脱颗粒以及碳水化合物和嘌呤的代谢(图2c)。
为了探究不同上皮亚型是否表现出不同的遗传变异,他们利用 inferCNV 软件对九种细胞类型的大规模染色体拷贝数变异 (CNV) 进行了分析。分析结果揭示了几个关键发现:(1) PMC_2 细胞的 CNV 水平高于 PMC_1 细胞,表明 PMC_2 与癌症的关联性更强;(2) 与癌细胞和 MSC 细胞相比,GMC 细胞和肠内分泌细胞的 CNV 水平相对较低。这一模式与其在不同病理区域的空间分布相符,其中 GMC 细胞和肠内分泌细胞主要位于正常区域,而癌细胞和 MSC 细胞则位于癌变区域(图2d-e)。基于正常、肠化生 (IM) 和癌变区域中上皮细胞亚型比例的聚类分析表明,具有相同组织学类型的区域往往具有相似的细胞类型组成。值得注意的是,与正常组织相比,IM 和癌症区域均表现出更高的异质性,并且 IM 中的上皮亚型比例与癌症中的上皮亚型比例比与正常区域中的上皮亚型比例更相似(图2f)。
此外,他们利用DPT算法来估计这九种细胞类型的伪时间,轨迹分析揭示了三个分支谱系:PMC_1⟶PMC_2⟶癌细胞,PC⟶癌细胞,MSC⟶RNA速度验证了癌细胞的存在(图2g)。与PMC_1相比,PMC_2表现出多种生物学功能,包括细胞迁移、伤口愈合、细胞间黏附、EMT相关通路以及多种信号通路,例如NFκB-TNFα、KRAS、ERBB、IL2-STAT5、IL1、INFγ、INFα和整合素介导的信号通路。这些通路可能在早期胃癌(EGC)的发生发展中发挥关键作用(图2h)。
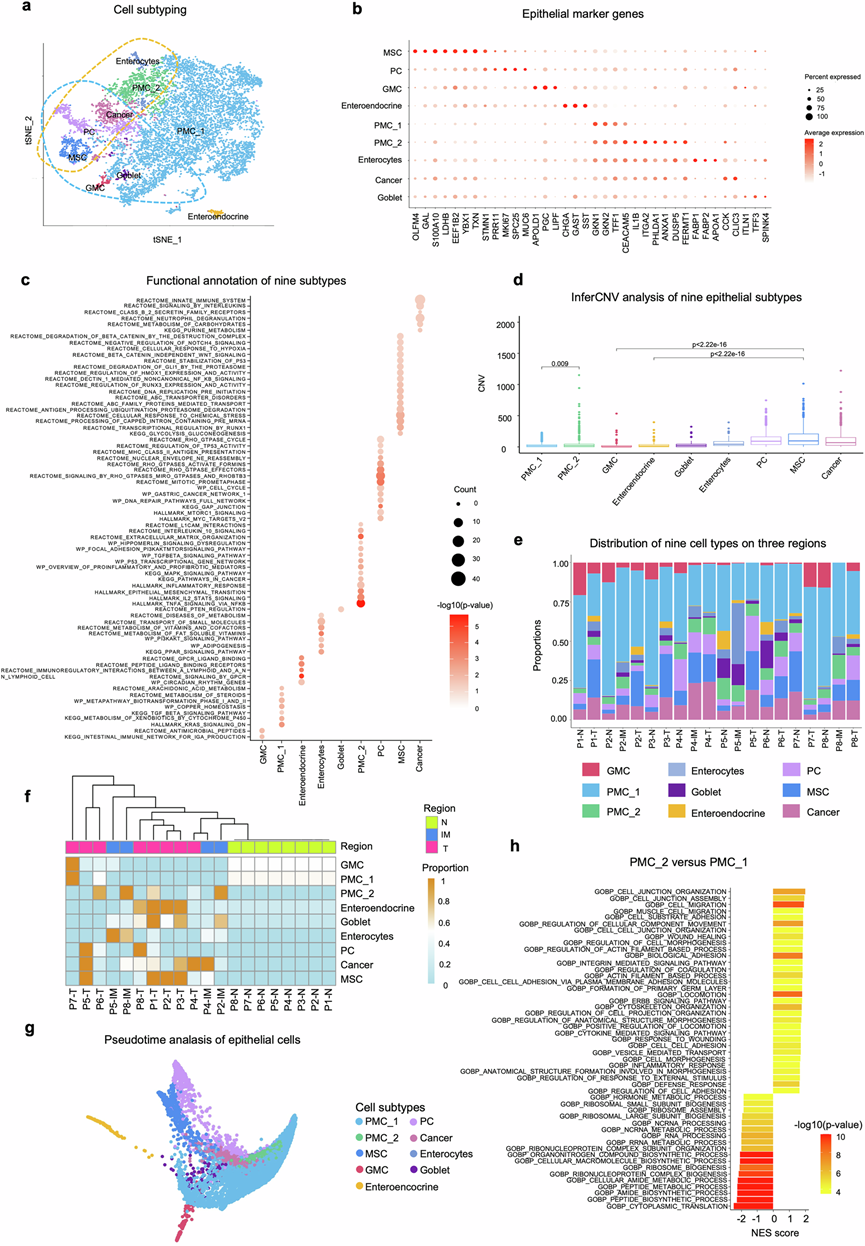
图2. 上皮细胞亚型的异质性。
(a) tSNE图展示了从scRNA-seq数据中鉴定的九种上皮细胞亚型。(b) 散点图显示了每种亚型中标记基因的表达水平。(c) 九种亚型的功能注释。(d) 箱线图显示了六种亚型(杯状细胞、肠细胞、PMC_2、PC、MSC和癌细胞)与PMC_1、GMC和肠内分泌亚型相比的大规模拷贝数变异(CNV)。(e) 每位患者的ST数据中九种细胞亚型在N、IM和T区域的分布。(f) 基于上皮亚型在正常、IM和癌变区域中的比例进行的无监督聚类分析。(g) 基于所有单细胞样本的scRNA-seq数据,对上皮细胞进行伪时间轨迹分析。(h) 功能分析比较 PMC_2 和 PMC_1。
03
PMC_P,即 EGC 启动期间的临界状态
为了识别在早期胃癌 (EGC) 起始阶段过度富集的上皮细胞,他们使用 stMVC 将来自三个上皮区域(即正常组织 (N)、肠化生 (IM) 和肿瘤组织 (T))的空间域分类为与疾病进展相关的六个类别。这些类别包括正常组织、GMC_P、IM、PMC_P、Pro_T 和肿瘤,每个类别都具有独特的基因表达谱(图3a)。PMC_P 和 GMC_P 分别在癌变前和从正常组织到肿瘤的过渡区域观察到,代表癌前状态。在癌变区域发现的30个Pro_T细胞,表现出与肿瘤进展相关的多种功能,例如炎症反应(通过NF-κB和IL-6/JAK/STAT3信号通路激活TNF-α信号通路)、纤维化/重塑通路(上皮-间质转化和TGF-β信号通路)、代谢重编程(胆固醇稳态和糖酵解)以及细胞命运控制(细胞凋亡、TP53通路)的激活,表明其处于复杂的促肿瘤状态。这一分类与推断的拷贝数变异(CNV)结果一致,CNV水平从正常组织到GMC_P和肿瘤组织,以及从正常/IM到PMC_P和肿瘤组织逐渐升高(图3b)。值得注意的是,在证实了已知的从GMC到肿瘤的分化通路的同时,他们也发现了一条潜在的从PMC到肿瘤的新通路(图3c)。
为了阐明 PMC_P 在驱动早期胃癌 (EGC) 发生中的潜在作用,他们采用了多种互补的方法:(i) PMC_P 细胞表现出COL3A1、SLC5A5、AKR1B10、LCN2、LGR4、CAPN8和RNASE1等基因的过表达,这些基因此前已报道与胃癌的发生发展相关(图3a);(ii) PMC_P 中七个代表性“起始促进”基因的平均表达水平与较短的总生存期显著相关,这已在来自 TCGA 胃癌数据库的独立队列中得到验证(图3d);(iii)通路分析表明,PMC_P 细胞积极参与关键的致癌信号级联反应,包括细胞凋亡、EMT、JAK-STAT 和 MAPK 通路(图3e);(iv)使用 GraphST 对六个组中的上皮亚型进行比较分析,揭示了不同的模式:PMC_1 细胞主要富集于正常/IM 区域,而 PMC_2 细胞在 PMC_P 区域中显著增多(图3f),这一模式已通过 mIHC 证实(图4a-b)。这种分布与 ST 数据和临床标本(图4d)中 PMC_P 区域中 PMC_2 基因特征评分升高相一致;(v) PMC_P 区域的特征是免疫抑制性微环境,这体现在癌前上皮区域内存在免疫检查点分子(PDCD1、CD274和HAVCR2)、共刺激/共抑制分子(CD86)、免疫抑制酶(IDO1、HLA-G)、髓系细胞标志物(CD33、MRC1)以及 T 细胞调节分子(IL2RA)(图4e)。此外,与其他五组相比,PMC_P 中免疫抑制性免疫细胞的比例显著更高(图4f)。此外,他们观察到癌前上皮区域中PD-L1表达升高,这在ST数据(图4g)和早期临床癌症样本中均有体现(图4h)。综上所述,这些发现表明PMC_2是连接IM和肿瘤发生的关键过渡上皮细胞群,而PMC_P是关键的癌前微环境,其特征是免疫抑制性微环境,先于EGC的发生。
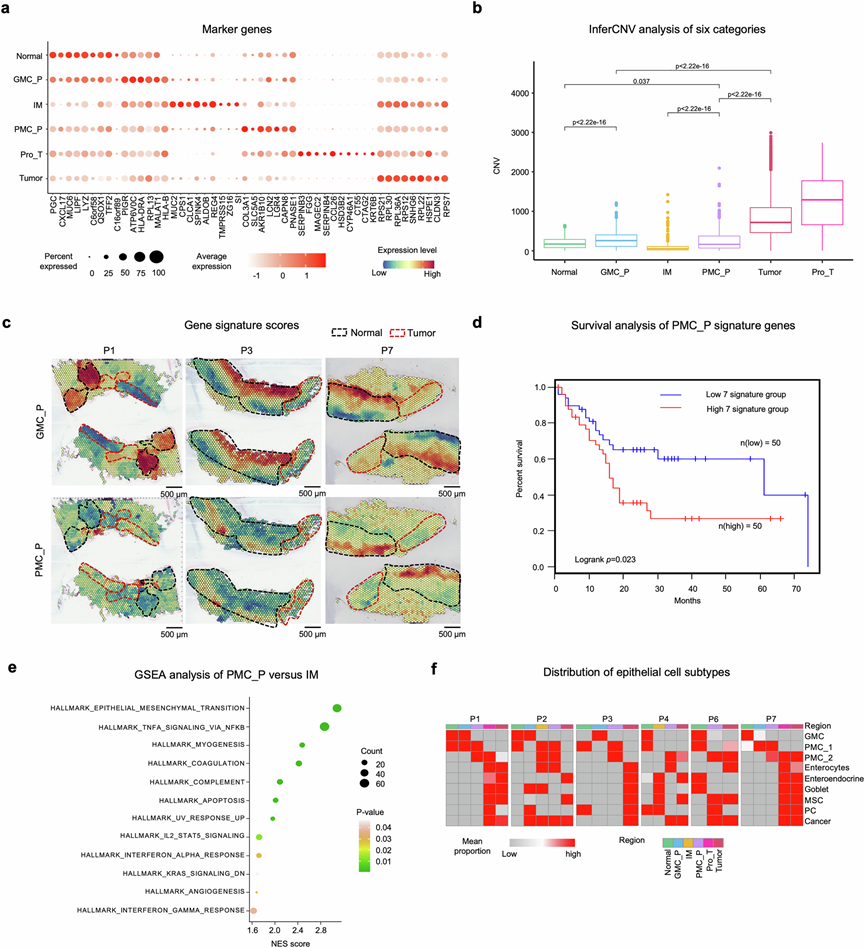
图3. 鉴定驱动早期胃癌 (EGC) 发生的关键上皮细胞状态。
(a) 散点图显示了在 ST 数据中识别出的六个空间上皮组中代表性标记基因的表达情况。(b) 箱线图显示了六个空间组中大规模CNV水平。(c) 三个代表性患者(P1、P2 和 P3)中 ST 区域内 GMC_P(上图)和 PMC_P(下图)标记基因的基因特征评分。(d)生存分析。(e) 基因集富集分析 (GSEA) 。(f) 热图显示了六个 ST 组中九种上皮亚型的比例。
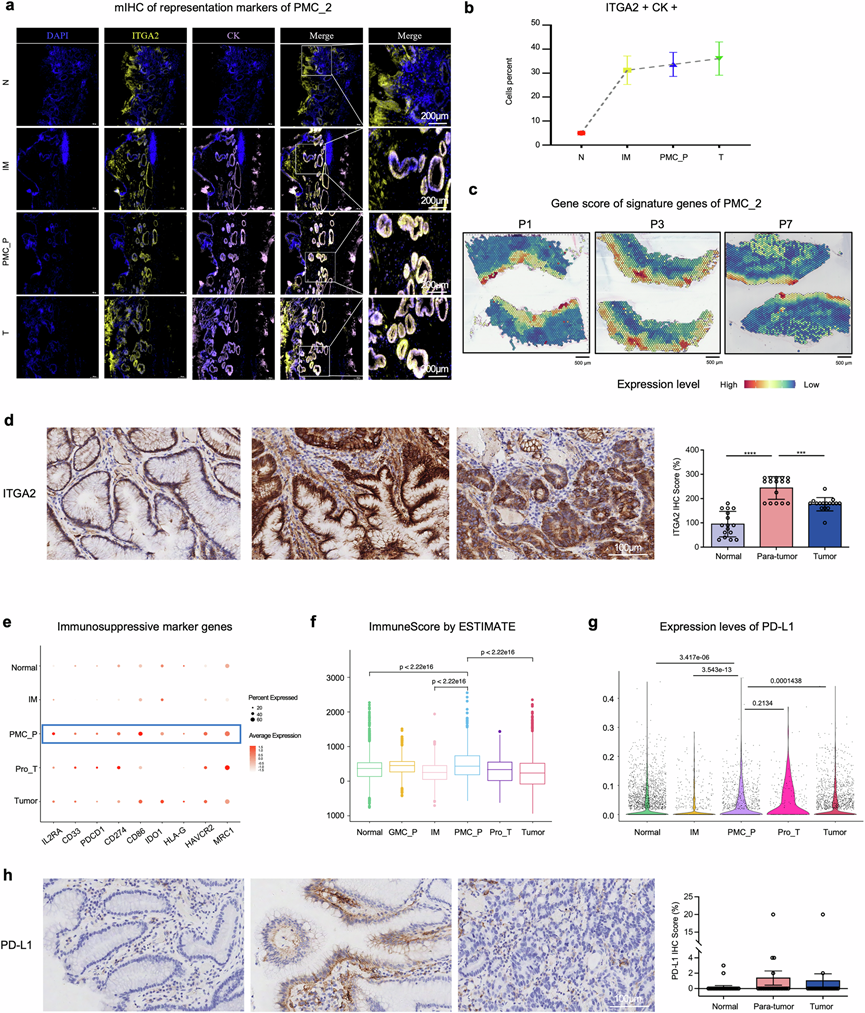
图4. 癌前PMC_P微环境协调PMC_2的积累和PD-L1介导的免疫抑制。
(a) 通过免疫荧光双标记(DAPI/CK/ ITGA2)分析各组中PMC_2标记物(CK /ITGA2)的空间分布。(b) 定量分析进一步证实PMC_2比例随进展阶段(N < IM < PMC_P < T)呈梯度增加。(c) PMC_2基因特征评分的空间表达。(d) 21例早期胃癌(EGC)患者的ITGA2表达显示,肿瘤旁区域的ITGA2表达水平显著高于其他区域。(e) 点图显示经典免疫抑制标志基因的表达。(f) 箱线图显示六个组中免疫评分的分布。(g) 小提琴图显示六个组中 PD-L1 的表达水平。(h) 21 例早期胃癌 (EGC) 患者的 PD-L1 表达情况。
04
PMC_2 与巨噬细胞/成纤维细胞之间的相互作用
为了研究潜在的细胞间通讯(CCC)机制(涉及多种信号通路,这些通路调控与早期胃癌(EGC)起始相关的不同细胞类型之间的相互作用),他们分析了PMC_P与其他五组上皮细胞之间的遗传差异。利用基尼系数程序,他们鉴定出几个候选分泌蛋白,包括AREG、IL1B、NAMPT、KLK7和IGFBP3,这些蛋白在PMC_P中的表达水平显著高于其他组(图5a)。为了进一步探究PMC_P内参与细胞通讯的关键蛋白,他们利用CellChat软件,发现AREG的配体-受体对(LRP)参与其中。 EGFR / ERBB2和NAMPT 在六名患者的PMC_P区域中,ITGA5 / ITGB1主要驱动细胞间相互作用(图5b)。该工具应用对比异质图学习技术在斑点水平上推断CCC,从而实现跨空间域的稳健且可比的模式识别(图5c-d)。此外,mIHC分析证实,AREG和EGFR / ERBB2以及NAMPT和ITGA5 / ITGB1在PMC_P区域过表达(图5e-f),并在临床标本中得到验证,表明这些LRP在肿瘤起始阶段的临界点发挥着关键作用。他们还分析了Pro_T区域与其他区域之间的基因差异,这些区域也显示出NAMPT表达。ITGA5 / ITGB1在 2 例患者的 Pro_T 区域中具有活性。
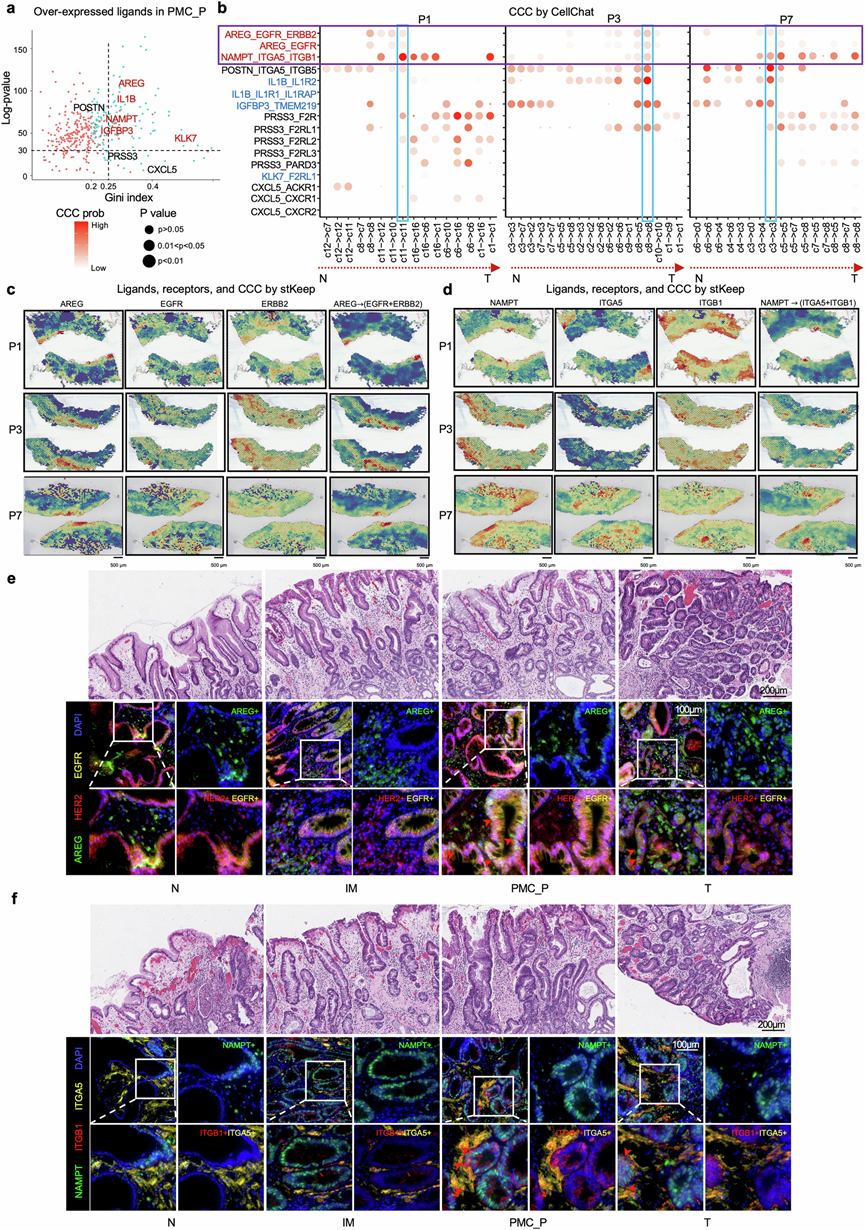
图5. 鉴定早期胃癌 (EGC) 起始阶段的关键细胞群和 CCC 机制。
(a) 散点图显示PMC_P 组中过表达配体基因的特异性(基尼系数)和差异水平。(b) 气泡热图显示 CellChat 检测的AREG、IL1B、NAMPT、KLK7、IGFBP3、PRSS3、CXCL5和POSTN相互作用对在不同区域的平均 CCC 强度。(c-d)空间表达分布分析。(e-f) H&E染色图和免疫组化图。
05
成纤维细胞和巨噬细胞相互作用
为了进一步探究哪些细胞类型利用这些LRP,他们对scRNA-seq数据进行了CellChat分析。结果显示,髓系细胞(例如M1巨噬细胞、M2巨噬细胞、mDC、CD14+单核细胞、肥大细胞)/NKT细胞与PMC_2/GMC之间存在与AREG相关的强相互作用。EGFR / ERBB2轴,以及髓系细胞/PMC_2与基质细胞(例如成纤维细胞和内皮细胞)之间通过NAMPT途径进行的连接。ITGA5 / ITGB1轴(图6a-b)。对标记物分布的进一步分析以及基因表达与特征评分之间的分析,阐明了关键信号分子的细胞来源。这些结果证实AREG主要来源于髓系细胞,NAMPT来源于PMC_2,而ITGA5/ITGB1来源于基质细胞(图6c),表明髓系细胞和PMC_2之间通过AREG存在密切的通讯。EGFR / ERBB2,以及PMC_2和成纤维细胞之间通过NAMPT的相互作用 在PMC_P区域内检测到ITGA5 / ITGB1,并通过mIHC进一步验证(图6d-f)。此外,mIHC结果显示:(i)PMC_P区域内ITGA2、NAMPT、ITGB1、ITGA5和DCN的表达水平较高,表明PMC_2来源的NAMPT与PMC_P中的成纤维细胞相互作用;(ii)PMC_P区域内S100A8、AREG、EGFR、ERBB2和ITGA2的表达水平较高,提示髓系细胞来源的AREG与PMC_P中的PMC_2相互作用。他们检测了四种髓系细胞亚型的分布,以进一步鉴定与PMC_P区域内PMC_2相互作用的细胞群,并分析了AREG表达与髓系细胞亚型基因特征评分之间的相关性。他们发现巨噬细胞是 PMC_P 区域中富集的主要髓系细胞群,并且它们的存在与患者中的AREG表达显著相关(图6g-h)。
随后,他们对患者 P4 的四个代表性区域(N、IM、PMC_P 和 T)进行了细胞群富集分析,结果显示 PMC_2 细胞数量从 IM 到 PMC_P 逐渐增加,同时成纤维细胞和巨噬细胞从 PMC_P 到 T 显著浸润(图6i)。这些发现凸显了 PMC_2、巨噬细胞和成纤维细胞之间的细胞间相互作用在驱动早期胃癌发生发展中的关键作用。
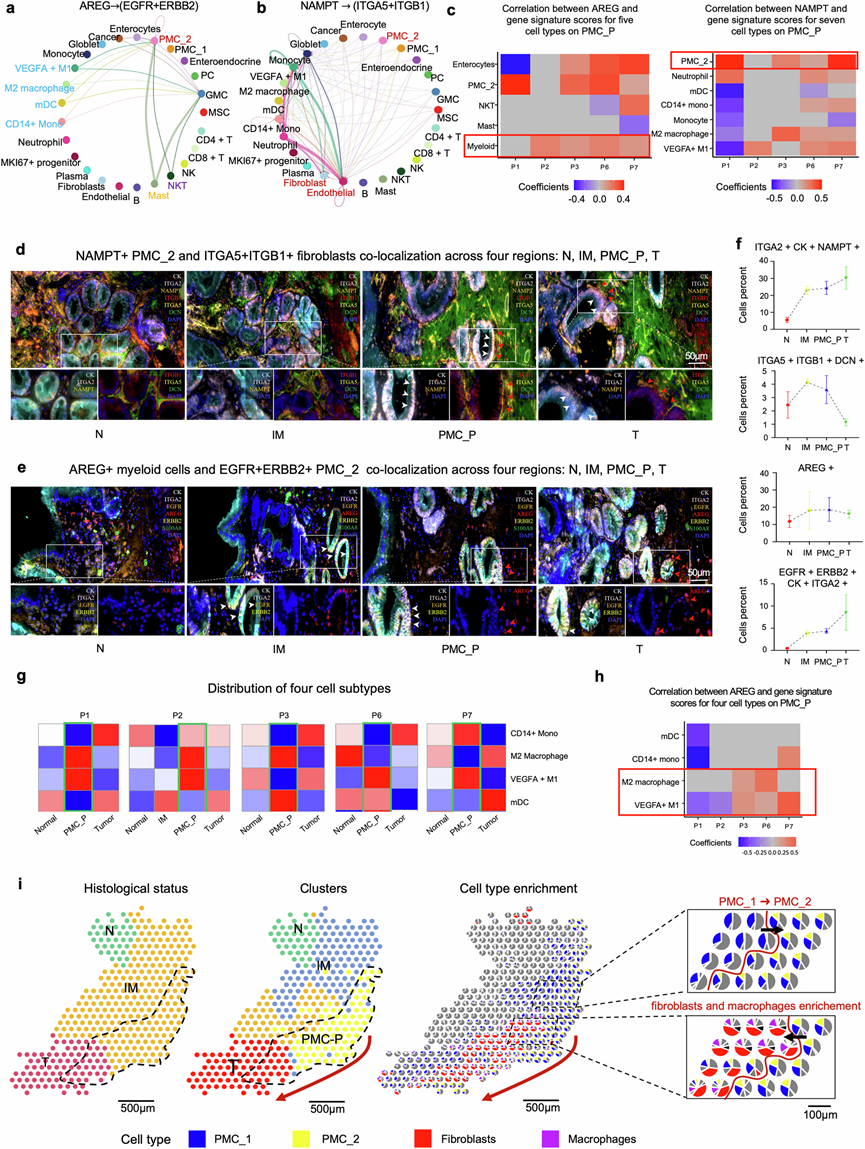
图6. PMC_2 与 PMC_P 内的成纤维细胞和巨噬细胞有很强的相互作用。
(a-b) 细胞间通讯分析。(c)基因表达与基因特征评分之间的Spearman相关性。(d-e) mIHC染色。(f)细胞比例分析。(g) 四种髓系细胞亚型的分布,显示巨噬细胞是 PMC_P 区域的主要髓系细胞类型。(h) AREG与髓系亚群之间的 Spearman 相关性。(i) 三种组织学状态(即 N、IM 和 T)的空间分布。
06
AREG/NAMPT促进癌前细胞系和类器官的恶性转化
为了阐明AREG和NAMPT在胃癌前病变恶性转化中的作用,他们成功建立了源自胃癌前病变(Pre-EGC)的原代细胞系和相应的类器官模型(图7a)。在成功将巨噬细胞极化为M1和M2表型后,他们在上皮细胞和巨噬细胞的上清液中均检测到了AREG的分泌,结果表明M1巨噬细胞分泌的AREG水平高于M2巨噬细胞。将癌前细胞与M1巨噬细胞共培养后进行增殖实验,结果显示,72小时后所有AREG处理的Pre-EGC组的细胞活力均显著增加,其中200 ng/ml处理组的效果最为显著(图7b)。对与M1巨噬细胞共培养的癌前细胞进行qPCR分析,检测初始基因集以及HER2、EGFR和PD-L1的表达。结果显示,100 ng/ml AREG处理后,RNASE1、AKR1B10、CAPN8、COL3A1、LCN2和LGR4等基因表达显著上调;200 ng/ml AREG处理后,EGFR和PD-L1表达显著上调; 400 ng/ml AREG处理后,HER2表达显著上调(图7c-d)。
在癌前上皮细胞系(Pre-EGC)的条件培养基中检测到了NAMPT的分泌,表明这些细胞能够主动释放NAMPT。为了进一步研究NAMPT的功能作用,他们建立了Pre-EGC和成纤维细胞的共培养体系,结果发现:(1)NAMPT处理可剂量依赖性地增强Pre-EGC的增殖,在100 ng/ml浓度下观察到显著的增殖(图7e);(2) NAMPT刺激可剂量依赖性地上调成纤维细胞表面受体ITGA5和ITGB1的表达,分别在25 ng/ml和50 ng/ml浓度下观察到最显著的上调(图7f)。 (3)对正常成纤维细胞(NF)、与 Pre-EGC 共培养的未处理 NF 以及暴露于 100 ng/ml NAMPT 的NF 进行比较分析,结果显示NAMPT处理组中CAF 标志物(FAP、纤连蛋白、α-SMA 和VIM)的荧光强度显著增强(图7g),这表明NAMPT驱动成纤维细胞活化并促进恶性转化,与先前报道的机制一致;(4)对初始基因集进行 qPCR 分析,结果显示,25 ng/ml NAMPT处理后COL3A1和PD-L1显著上调,50 ng/ml NAMPT处理后AKR1B10、CAPN8和LGR4显著上调, 100 ng/ml NAMPT处理后RNASE1和LCN2表达显著上调(图7h-i)。总的来说,这些结果表明,NAMPT不仅能增强癌前上皮细胞的增殖,还能促进成纤维细胞活化和恶性转化,从而促进早期胃癌的发生。
类器官模型重现了类似的趋势(图7j)。经5天处理后,ATP检测显示,在200 ng/ml和400 ng/ml AREG处理组中,类器官的活力显著增加,其中200 ng/ml的效果最为显著,这与细胞系的结果一致。对于NAMPT处理的类器官,100 ng/ml组的活力显著增加(图7k)。此外,200 ng/ml处理组中直径超过100 µm的类器官比例显著更高(图7l)。免疫荧光染色显示, NAMPT处理的类器官中E-钙黏蛋白表达显著降低,表明发生了EMT,而纤连蛋白表达保持不变(图7m)。总的来说,这些发现强调了AREG和NAMPT在促进细胞增殖、调节基因表达和驱动癌前状态表型变化方面的关键作用,从而促进恶性转化。
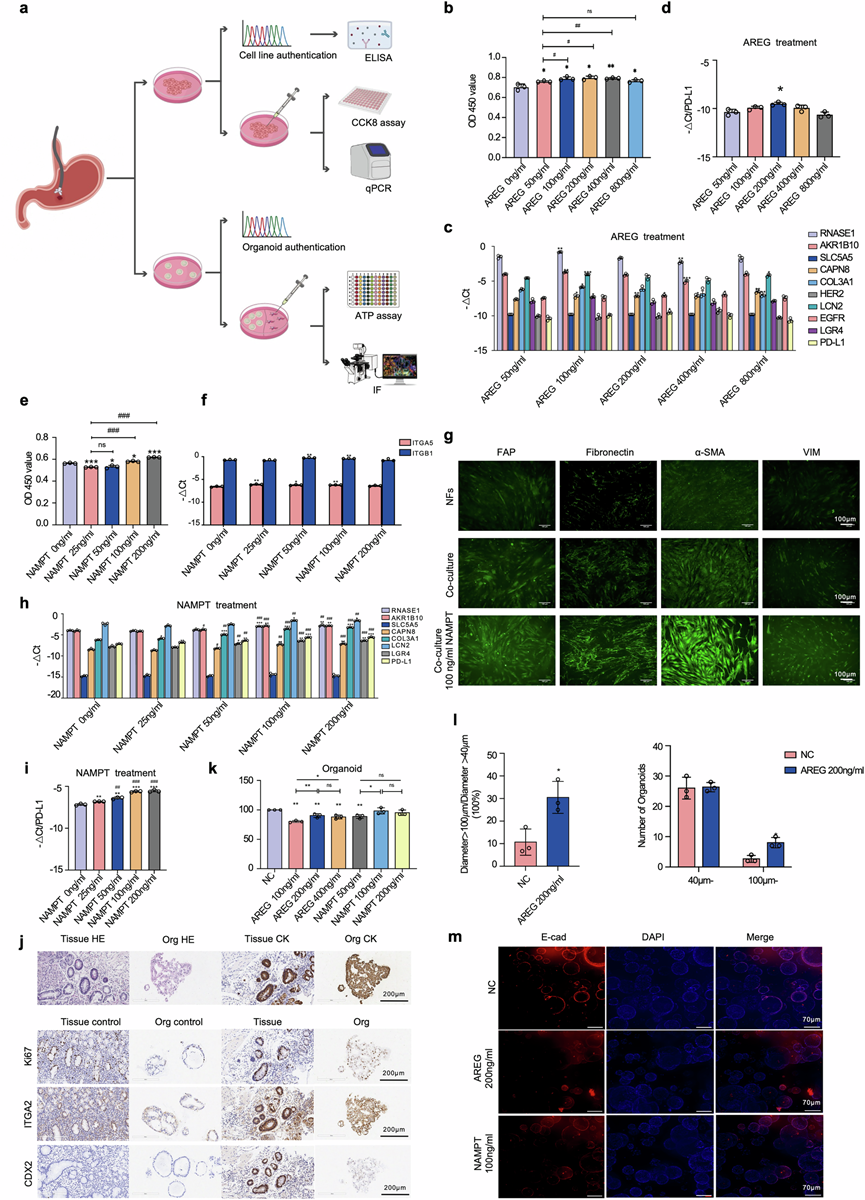
图7. AREG和NAMPT可增强癌前胃细胞系和类器官的增殖并调控基因表达。
(a) 从早期胃癌(EGC) 患者的活检组织中成功建立了癌前细胞系 (Pre-EGC) 和类器官,并用AREG和/或NAMPT进行处理。(b) CCK-8 检测显示AREG处理72 小时后对 Pre-EGC 细胞活力的影响。(c) qPCR 分析显示,AREG处理 72 小时后 Pre-EGC 中“起始促进”基因HER2、EGFR和 PD-L1 的表达发生了变化。(d) qPCR 分析显示,AREG处理后 Pre-EGC 中 PD-L1 的表达呈剂量依赖性变化。(e) CCK-8检测结果表明,NAMPT(0、25、50、100、200 ng/ml)处理 72 小时后对 Pre-EGC 细胞活力有显著影响。(f) 成纤维细胞表面受体ITGA5和ITGB1的表达呈剂量依赖性上调。(g) 与正常成纤维细胞 (NF) 和未处理组相比,用 100 ng/ml NAMPT处理的 Pre-EGC 与 NF 共培养后, CAF 标志物(FAP、纤连蛋白、α-SMA 和 VIM)的荧光强度显著增强。(h) PCR分析显示,用NAMPT处理的 NF 与 Pre-EGC 共培养72 小时后,“起始促进”基因和 PD-L1 的表达发生改变。(i) qPCR 分析显示, NAMPT处理后 Pre-EGC 中 PD-L1 表达呈剂量依赖性调节。(j) 癌前胃类器官的验证和形态学表征。(k) ATP检测显示AREG处理 5 天后对癌前类器官的增殖作用。(l) 分析用 200 ng/ml AREG处理5 天的类器官的大小和基因表达。(m) 用200 ng/ml AREG或100 ng/ml NAMPT处理5天后,免疫荧光分析E-cadherin在类器官中的表达差异。
07
评估抗NAMPT / AREG治疗在早期胃癌预防中的作用
他们利用转基因CEA-SV40小鼠模型研究了靶向AREG和NAMPT在EGC进展中的治疗效果。治疗方法如下:小鼠每周两次饮用含20 μg抗AREG抗体的水,和/或连续4天每天两次饮用含30 mg/kg FK866的水,持续2周,如前所述(图8a)。第7周,处死小鼠,并对其胃进行宏观(图8b)和组织学评估(图8c)。病理诊断结果显示,野生型(WT)、CEA-SV40未治疗组、抗AREG组、FK866组和抗AREG +FK866组的癌症发生率分别为16.7%、100%、66.7%、50%和50%(图8d)。与未治疗组相比,所有治疗组的病变程度均较轻,这凸显了这些干预措施在延缓早期胃癌发生方面的潜力。
分子分析显示,各组间PD-L1、pSTAT、pp38、pp65以及“起始促进基因”的表达存在差异(图8)。PD-L1在PMC_P和Pro_T组织中高表达(图4g),其表达可由NAMPT抑制剂(FK866)抑制。尽管STAT1、p38和p65的总水平保持不变,但所有处理组的pSTAT1核转位和pp38核活性均显著降低,且FK866处理后NF-κB激活(核内pp65表达升高)也显著降低(图8f)。“起始促进基因”表现出不同的敏感性。RNASE1对NAMPT抑制剂有选择性反应,CAPN8对联合治疗有反应,而LGR4在所有治疗组中均下调。PMC_2标志物(ITGA2)和成纤维细胞标志物(VIM)在所有治疗组中也显著降低,表明PMC_2和成纤维细胞浸润减少,并且它们在破坏促肿瘤微环境方面具有协同作用(图8f)。他们进一步通过Western blot检测了Pre-EGC、Pre-EGC + 200 ng/ml AREG和Pre-EGC + 100 ng/ml NAMPT处理的成纤维细胞经72小时处理后PD-L1、STAT、p-STAT1、p38、p-p38、p65和p-p65的表达。 WB结果证实,两种治疗方法均导致这些通路的上调,与体内实验结果一致(图8g)。综上所述,这些结果表明抗AREG和FK866治疗可降低早期胃癌发生和发展的分子驱动因素,凸显了它们作为胃癌前病变治疗策略的潜力。
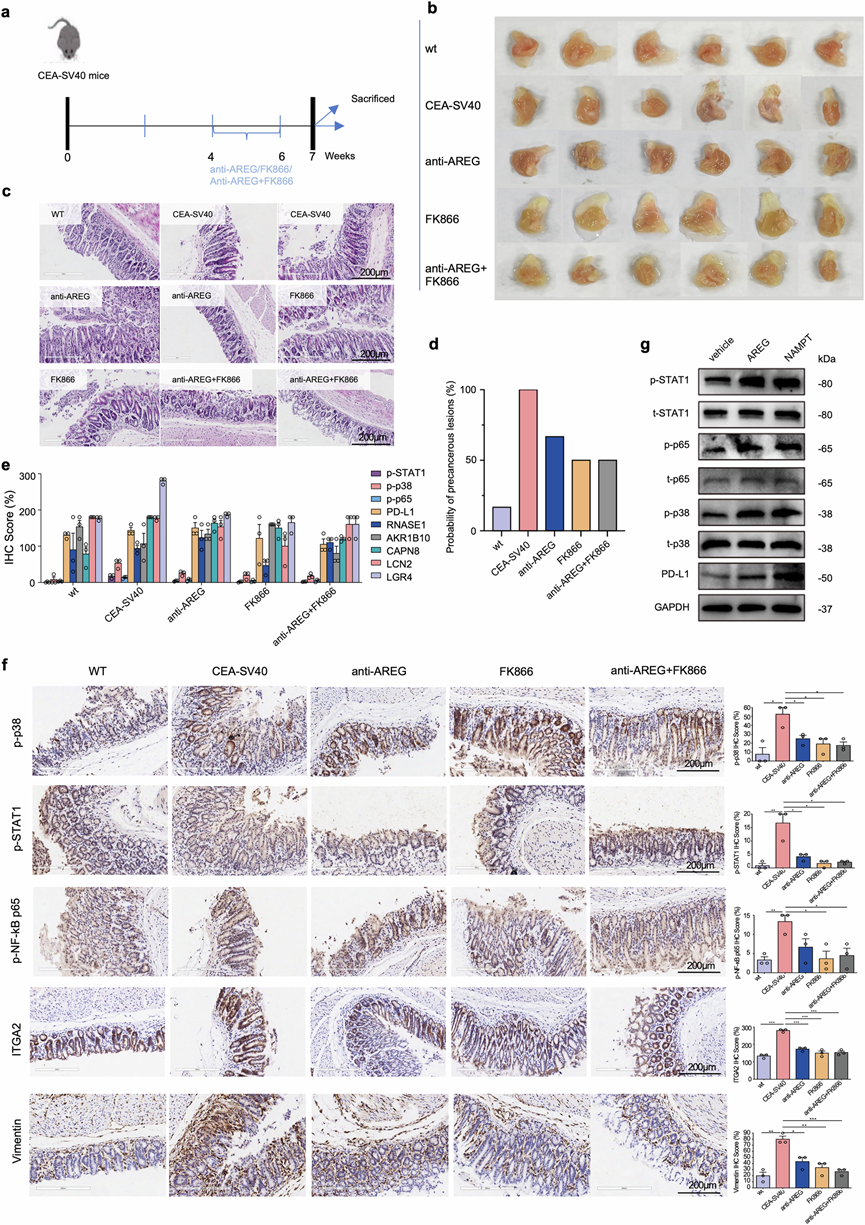
图8. 抗AREG抗体和FK866在CEA-SV40小鼠早期胃癌模型中的治疗效果。
(a) 示意图概述了CEA-SV40小鼠早期胃癌的诱导以及抗AREG抗体、FK866抗体和联合治疗(抗AREG抗体 +FK866)的口服给药方案。(b) 纵向解剖小鼠胃部以暴露胃黏膜进行肉眼观察的代表性图像。(c) 早期病变的肉眼观察显示各组均未见明显异常。(d) 各组癌前病变形成的概率。(e) 免疫组化染色评分显示各组之间存在不同的表达模式。(f) 代表性免疫组化染色图像显示各组之间存在显著差异。(g)免疫印迹分析。
+ + + + + + + + + + +
结 论
本研究利用人工智能模型整合了来自9例EGC样本(涵盖从正常到癌变的连续阶段)的空间多模态数据,构建了疾病进展的时空图谱,并识别出一个关键临界点(PMC_P),该临界点以早期癌症发展过程中的免疫抑制微环境为特征。在该阶段,具有干性的炎症性腺泡黏液细胞(PMC_2)通过NAMPT与成纤维细胞相互作用。ITGA5/ITGB1和巨噬细胞通过AREG相互作用⟶EGFR/ERBB2信号通路促进癌症的发生。本研究建立了胃癌前细胞系和类器官,证实NAMPT和AREG在体外促进细胞增殖。此外,在CEA-SV40转基因小鼠模型中,靶向AREG和/或NAMPT可破坏关键的细胞间相互作用,抑制JAK-STAT、MAPK和NFκB通路,并降低PD-L1的表达,体外Western blot实验也证实了这一点。这些干预措施延缓了疾病进展,逆转了免疫抑制性微环境,并阻止了恶性转化。本研究使用内镜切除的EGC标本进行了临床验证,精确描绘了EGC发展的时空特征,并发现了新的诊断标志物和早期干预的治疗靶点。
+ + + + +



 English
English


