文献解读|Nature(48.5):深度可视化蛋白质组学绘制遗传性肝病中的蛋白质毒性图谱
✦ +
+
论文ID
原名:Deep Visual Proteomics maps proteotoxicity in a genetic liver disease
译名:深度可视化蛋白质组学绘制遗传性肝病中的蛋白质毒性图谱
期刊:Nature
影响因子:48.5
发表时间:2025.04.16
DOI号:10.1038/s41586-025-08885-4
背 景
蛋白质错误折叠疾病,包括α1-抗胰蛋白酶缺乏症(AATD),构成了严重的健康挑战,但其细胞进展机制仍知之甚少。近期推出了深度可视化蛋白质组学(DVP)技术,它整合了染色、人工智能引导的细胞分割和分类、单细胞形态的激光显微切割以及高灵敏度质谱。DVP凭借其显著的空间和可视化特性,在数字病理学应用中表现卓越,能够同时对数千种蛋白质进行深度蛋白质组学表征。
实验设计
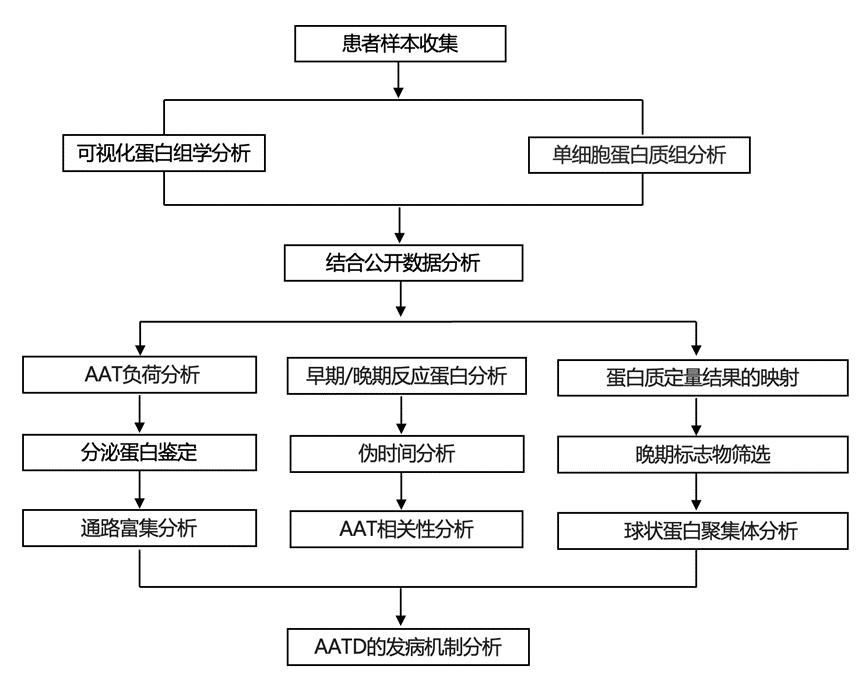
结 果
01
蛋白质毒性反应的蛋白质组图谱
研究团队收集了一组来自致病性Z变异纯合子患者的福尔马林固定石蜡包埋(FFPE)活检组织和肝脏移植标本,涵盖所有纤维化阶段(n = 34)。虽然患者携带相同的致病突变,中位年龄(58 ± 10岁)和BMI(25.2 ± 4.0)也相近,但纤维化阶段却差异显著,这表明可能存在尚未探索的分子抵抗力或风险特征。
为了阐明AATD患者临床异质性的分子基础,他们采用了一种全面的蛋白质组学分析方法来表征肝细胞对蛋白毒性应激的反应。首先,使用激光显微切割技术从患者活检组织中切割出3 μm厚的FFPE切片,并按照开发的DVP工作流程进行质谱分析。在对细胞轮廓和AAT进行染色后,他们根据显微镜图像将细胞分割并分层为低、中、高聚集负荷组(图1a-b)。然后,他们使用最新引进的Orbitrap Astral质谱仪采集了100个样本(相当于10-15个完整肝细胞的体积)的蛋白质,获得了高质量的数据集,平均每个样本的蛋白质组深度超过5000个。他们观察到低负荷细胞和高负荷细胞之间AAT水平存在显著的23倍差异。α1-抗胰蛋白酶(AAT)负荷在第二主成分上捕获,仅次于第一和第二主成分上的纤维化分期。鉴于活检材料中AAT+细胞的稀疏性,这验证了激光显微切割方法,因为它能够更清晰地展现生物学表型。与高纤维化分期相比,低纤维化分期的活检样本在蛋白质组学和成像数据上均表现出较低的AAT基线负荷,这与之前的研究结果一致,而最大负荷在所有分期中基本保持不变。三个负荷类别的蛋白质组差异显著(图1c)。除了AAT之外,AATD 肝脏病理的几个已知标志物在聚集体阳性细胞中高度富集,例如内质网(ER)分子伴侣 HSPA5增加 1.6 倍,ER-高尔基体cargo受体 LMAN1 增加 2.9倍(图1d)。
在表达失调最显著的蛋白中,他们鉴定出其他分泌蛋白,包括许多明确的丝氨酸蛋白酶抑制剂(SERPIN)、凝血因子和补体因子(图1c,图S2a-d)。这与近期关于SERPIN在AAT包涵体中聚集的研究结果相符,并支持内质网空间拥挤的观点,由于受累肝细胞中已注释的血浆蛋白的积累,可能具有潜在的全身性病理意义(图S2e)。半乳糖凝集素-3结合蛋白LGALS3BP和凋亡诱导因子TNFSF10的表达变化最为显著(图1c-d)。LGALS3BP是一种肝细胞产生的、靶向分泌的蛋白,在肝病患者的血浆中表达升高。描述 LGALS3BP 免疫调节活性的报告可以解释免疫细胞参与 AATD 肝脏病理。
通路富集分析显示,与未折叠蛋白反应(UPR)三个分支相关的蛋白显著升高,这些蛋白分别由ATF6、PERK和IRE1介导,同时分子伴侣普遍上调,而转录和翻译机制则有所下降。这导致胆汁分泌等生理功能受损(图1e)。许多反应最终汇聚成对活性氧的保护性反应,表现为硫氧还蛋白和谷氧还蛋白的上调,包括过氧化物酶体异常增多和线粒体复合物I减少(图1d,图S2b-j)。蛋白酶体和自噬蛋白基本保持不变,也未检测到钙稳态紊乱(图1e,图S2k)。
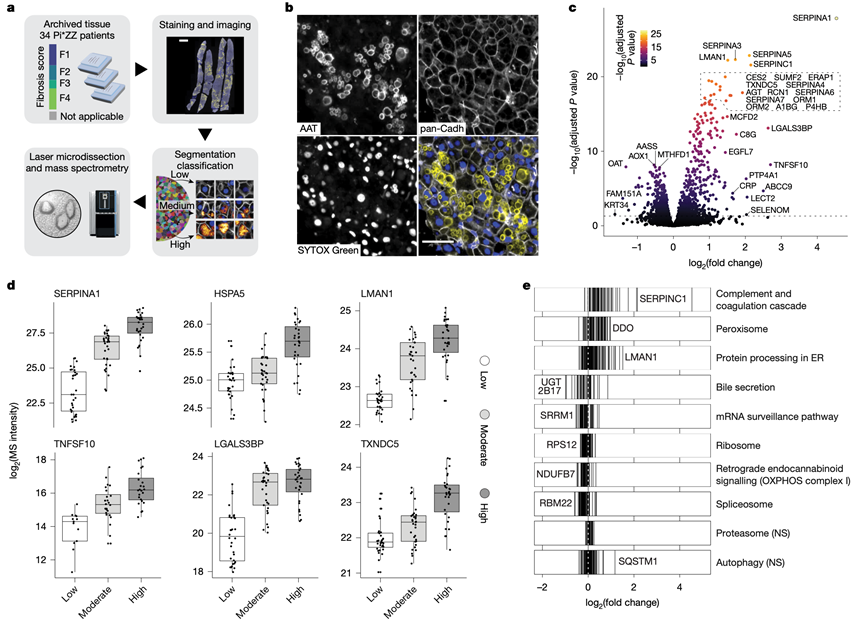
图1. 肝细胞应激反应的蛋白质组学图谱。
(a) 深度可视化蛋白质组学工作流程概述。(b) 免疫荧光染色以及三色叠加图。(c) 高、中、低 AAT 积累细胞的蛋白质组学变化。(d) 三个类别中选定蛋白质的质谱强度。(e)通路富集分析。
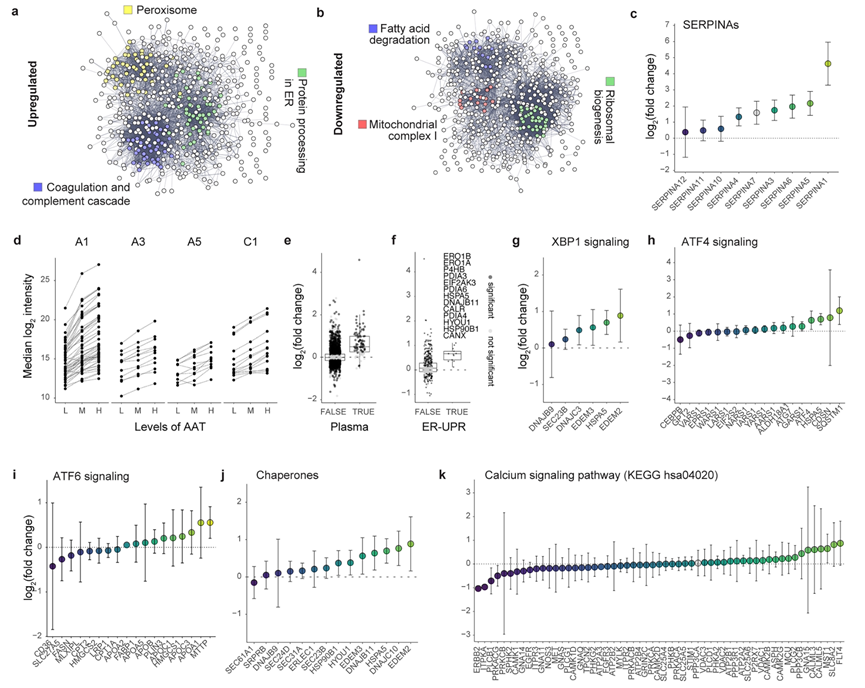
图S2. 分析蛋白质毒性应激的反应。
(a) STRING相互作用网络。(b) 细胞中显著下调蛋白。(c) 相对于基线肝细胞组,SERPINA蛋白家族成员的变化。(d) 三种肝细胞类型中SERPIN蛋白家族前体的变化。(e) 相对于基线肝细胞组,靶向血浆分泌的蛋白的变化。(f) 蛋白变化分析。(g-k) 图中显示了有无聚集体细胞中指定通路蛋白水平的比较。
02
早期和晚期应激反应
本研究的实验设计涵盖了三种不同的负荷等级,应该能够解析分子事件的逐步发展过程。为了确定AAT积累过程中分子反应发生的顺序,首先将AAT与其他蛋白质水平进行关联分析,以识别与AAT水平密切相关的“跟随者”。内质网蛋白位列前十,其中许多蛋白最终会分泌(图2a)。这其中包括许多结构相似的丝氨酸蛋白酶抑制剂(SERPIN),而这些蛋白与AAT水平的密切关联表明,它们与AAT同步积累,而非共同调控。
随后,他们将蛋白质分为对AAT积累引起的蛋白毒性应激的早期反应蛋白和晚期反应蛋白(图2b)。在共升高的蛋白质中,与AAT负荷的相关性最为显著,其中大多数(77.7%)表现为晚期反应蛋白,而早期反应蛋白的比例较小。免疫调节标志物LGALS3BP在早期反应蛋白中最为突出,其次是内质网cargo受体MCFD2及其共结合蛋白LMAN1(图2c)。早期出现了强烈的过氧化物酶体生物合成反应,其特征是过氧化物酶体增殖因子PEX11B和其他膜整合蛋白,以及脂质代谢和超氧化物解毒蛋白(图2d-e)。相比之下,虽然在早期阶段即可观察到蛋白质积累(图2d),但UPR核心机制的大多数蛋白质在AAT积累后期才出现。UPR与过氧化物酶体活性之间的相互作用仍知之甚少,但脂质代谢、胆固醇代谢和活性氧解毒均与这两个通路相关。总之,数据表明内质网氧化还原酶-1α (ERO1A)——一种主要的过氧化物产生酶——显著增加(图1c)。
随后,他们分析了不同纤维化阶段的样本,结果显示,随着纤维化程度的加重,蛋白毒性反应通路中的主要功能失调逐渐显现(图2f)。值得注意的是,这包括过氧化物酶体反应,其起始时间相对于AAT负荷逐渐延长(图2g)。过氧化物酶体分子伴侣或类伴侣蛋白未发生改变,表明过氧化物酶体不太可能参与未折叠蛋白的清除。
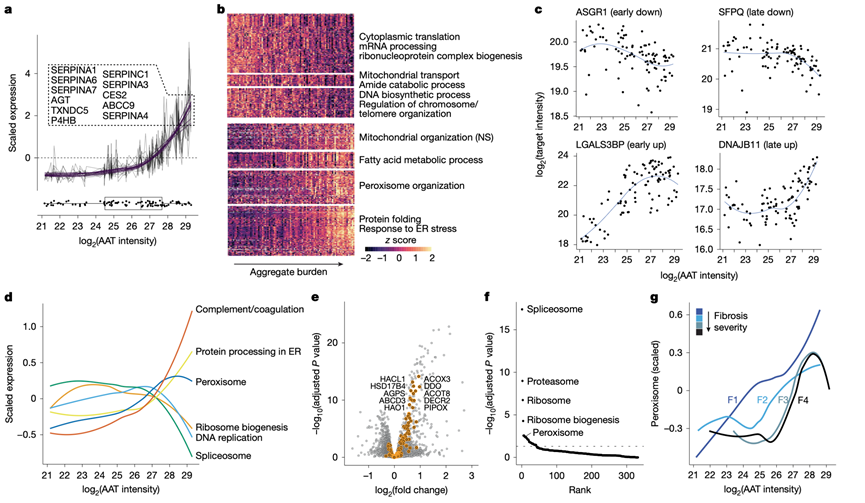
图2. 对蛋白质毒性应激的早期和晚期反应。
(a) 与AAT相关性最高的十个蛋白质的表达谱。(b) 将显著变化的蛋白质聚类为对蛋白毒性应激的早期和晚期反应基因, 并按AAT水平在x轴上排序。y 轴分为七组,以充分覆盖所有反应类型。(c) 按方向性分析的早期和晚期反应基因的伪时间表达。(d) 以z分数表示的所示KEGG通路累积变化 。(e) 三个AAT区间内蛋白质水平的变化,突出显示了过氧化物酶体蛋白。(f) 早期AAT积累期间F1和F4纤维化样本之间差异最大的功能类别。(g) 过氧化物酶体蛋白在四个纤维化阶段的累积表达。
03
完整组织中的单细胞映射
完整组织中AAT的积累表现出显著的空间分布特征。既往研究表明,在Pi*ZZ基因型的AATD患者中,AAT沿门静脉至中央静脉轴的区域梯度分布不均。然而,AAT+和AAT -细胞之间清晰的边界以及缺乏渐变,以及单个阳性细胞的存在,表明情况更为复杂(图3a)。为了绘制这些区域的空间蛋白质组图谱,基于之前开发的单细胞DVP工作流程,他们从6例F1期肝活检标本的10 μm厚FFPE切片(相当于完整肝细胞的三分之一到二分之一)的特定区域分离出单个细胞。选择早期(F1期)肝活检标本是为了在纤维化程度较低的环境下研究应激过程,从而减少晚期疾病可能造成的混淆效应。
他们对三个活检样本中259个单一形态的蛋白质组进行了定量分析,蛋白质层数中位数为2785个,最高可达 4299 个(图3b)。激光捕获技术展现出极高的精确度,相邻的 AAT+ 和AAT- 细胞能够完全分离(图3a)。比较边界区域的AAT+ 和AAT- 细胞,他们发现了与之前类似的蛋白毒性应激标志物。有趣的是,边界区域内第一行或第二行的细胞,以及各自AAT类别的细胞,其蛋白质组非常相似(图3c)。与此一致的是,AAT 积累标志物 LGALS3BP 和 ERO1A 在AAT+ 和AAT- 细胞之间存在显著差异,但在第一行和第二行相邻细胞之间则无显著差异。因此,数据支持相邻细胞之间不存在专门的应激传播,表明 AAT 诱导的蛋白毒性应激是一种细胞内在反应。
将早期和晚期反应标记物重新映射到组织后,他们发现SERPINC1和LGALS3BP在边界区域呈现预期模式,这与早期AAT水平相吻合。晚期标记物DNAJB11在六个样本中的四个样本中保持不变,表明他们捕捉到了早期至中期的积累事件(图3d)。然而,他们在两个样本的边界细胞中检测到了凋亡诱导因子TNFSF10的上调。进一步观察发现,聚集体的形态显著不同,呈现出球状表型,而另外两个样本中则呈现无定形AAT积累。
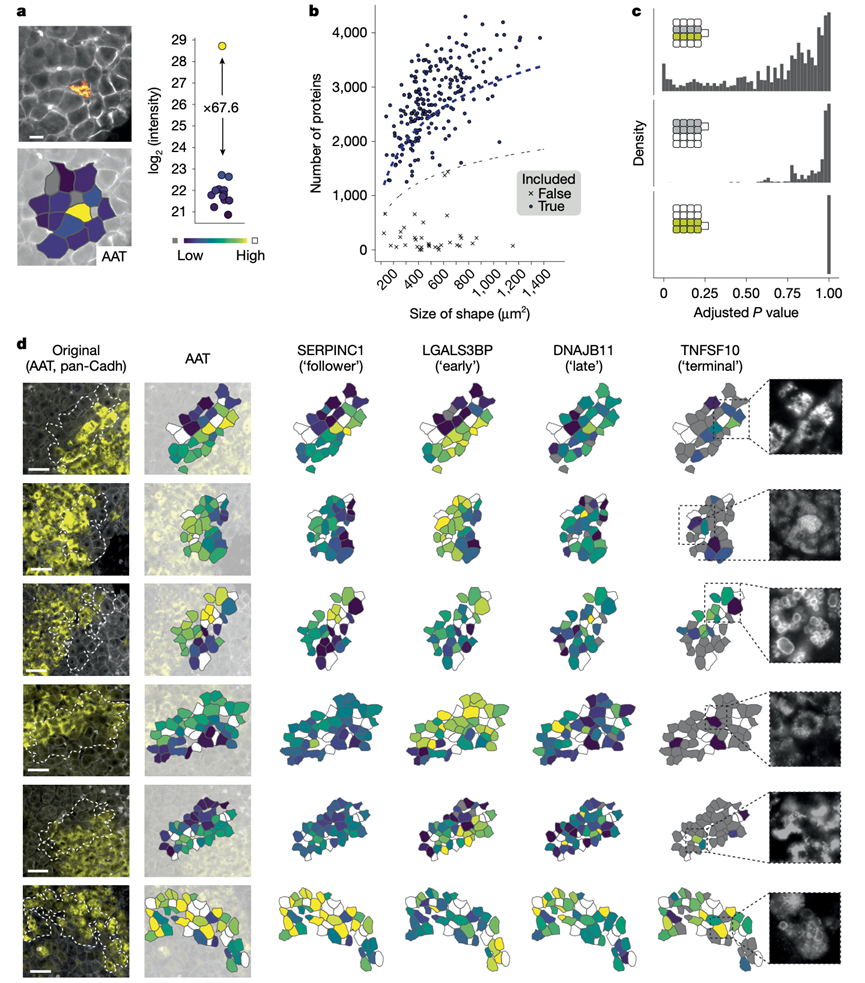
图3. 在单细胞水平上绘制完整组织图。
(a) 通过从FFPE组织中分离相邻细胞来展示工作流程的富集效率。(b) 在所有259次运行中,每个形状检测到的蛋白质数量与显微切割形状的面积的关系。(c) 比较P值的分布。(d) 将蛋白质组信息映射到原始显微图像上。
04
球状聚集体是凋亡细胞的标志
受此启发,他们改进了DVP工作流程,将形态学信息与蛋白质组学数据采集相结合。他们获得了肝切除样本,其中包含数千个具有不同AAT聚集体形态的细胞,这些细胞分布在同一张载玻片上。对三个生物学样本和四个技术样本的3 µm厚切片进行染色和共聚焦成像后,他们使用ConvNeXt卷积神经网络分割细胞,并将细胞边界内的AAT通道信号转换为2048个代表AAT形态的特征。他们使用均匀流形逼近和投影(UMAP)将这些特征投影到二维空间,并在图像信息层上确定了50个均匀分布的中心点,从中选择了距离中心点最近的50个细胞。这些细胞通过激光显微切割分离,并通过质谱(MS)进行检测,最终得到250个形态类别,代表总共12500个细胞(图4a)。
利用UMAP将这些显微切割细胞的表征投影到二维空间,验证了所使用的卷积神经网络确实能够根据聚集体形态对细胞进行分层,其中无聚集体的细胞聚集在一端,而球状和无定形形态的细胞则位于另一端,彼此之间清晰分离(图4b)。他们从相当于5到10个完整肝细胞的样本中获得了 5970 种蛋白质的中位蛋白质组学深度。蛋白质组学数据的主要驱动因素是分别在主成分1和2上角蛋白和 AAT 水平的动态变化(图4c)。当按蛋白质组将样本分组时,患者样本在蛋白质聚类中分布均匀,没有明显的基因型或技术偏差(图4d)。作为反向原理验证,他们将蛋白质聚类映射回 UMAP 图像空间,并实现了清晰的维度分离。同样地,同一蛋白质聚类的样本在蛋白质组 UMAP 和t分布随机邻域嵌入图中也表现出彼此之间最短的距离。
为了更好地理解形态类型背后的分子反应,他们对具有清晰球状聚集体和无定形聚集体的样本进行了比较分析(图4e)。与预期相反,通常与 AAT 水平相关的标记物,例如CES2和ERO1A,在球状聚集体中表达降低。相反,凋亡诱导因子 TNFSF10 和炎症标记物C反应蛋白(CRP)的表达显著升高,表明这是一种晚期表型。随后,他们将标记蛋白的表达水平映射回 UMAP 衍生的图像空间。有趣的是,ERO1A和TNFSF10定位于两个不同的细胞群中(图4f)。ERO1A指示正在进行的 UPR 反应,在无定形聚集体中高度富集,而 TNFSF10 主要存在于具有球状聚集体的细胞中,并与先天免疫系统激活因子共存。与此一致,基因集富集分析 (GSEA) 进一步发现,与细胞死亡相关的过程在球状类型中上调。
鉴于 CRP 在图像 UMAP 空间中呈现较为线性的响应率(图4f),他们随后根据 CRP 表达水平对所有样本进行了伪时间排序。在所有四个生物学样本中,虽然CRP 信号仍然存在,但仍存在小的颗粒状聚集体。随后,在细胞死亡和清除之前,细胞经历了快速的无定形聚集,最终凝聚成球状聚集体,这是细胞晚期的一个特征(图4g)。除了 TNFSF10 之外,他们还鉴定出 EGF 样结构域蛋白 7 (EGFL7) 是该阶段的一个有效标志物,它在 AATD 表型中出现较晚。值得注意的是,EGFL7 在肝细胞癌中也高表达,且高表达水平与不良预后相关。然而,球状表型与 AATD 中肝细胞癌发生率之间的潜在联系仍有待探索。该晚期表型进一步表现为晚期 UPR 停滞甚至下降,钙网蛋白和 ERO1A 水平验证了这一点,而 UGT2B17 等蛋白质水平的下降表明该肝细胞亚型的生理功能终止(图4h)。
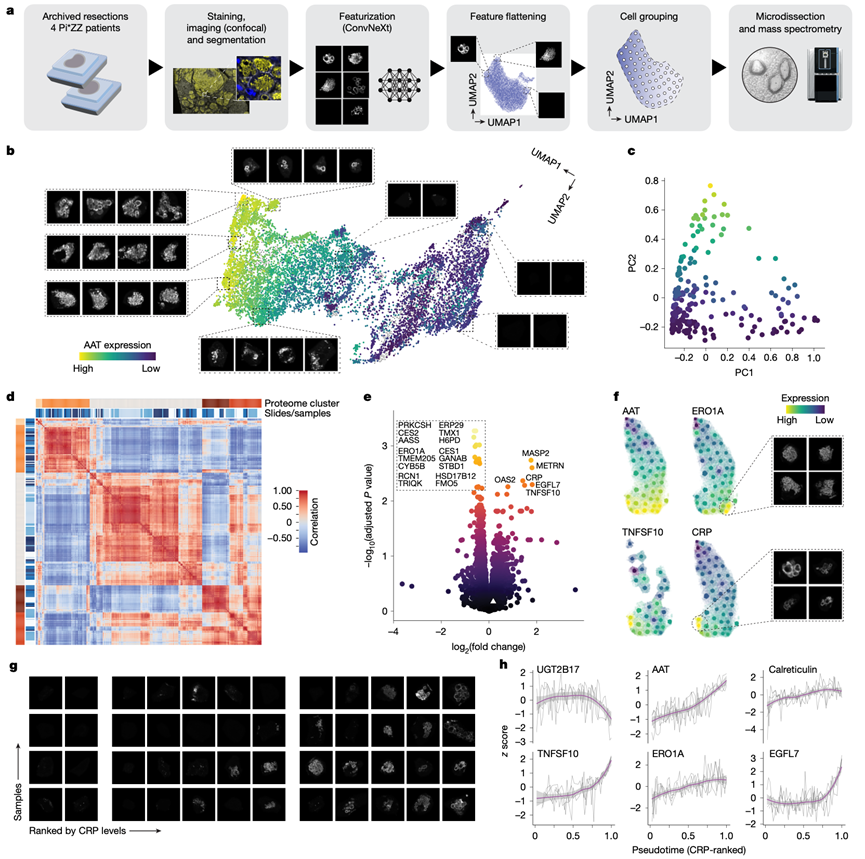
图4. 形态学引导的 DVP。
(a)流程概览。(b) 所有激光显微切割细胞(12500个)的投影以及指定区域的代表性AAT图像。(c) 蛋白质组学数据。(d) 蛋白质组学样本相关性热图。(e) 选择AAT水平相似的细胞(白色三角形)后,比较具有球状聚集体和无定形聚集体的细胞的蛋白质组。(f) 将蛋白质组学数据投影到一个代表性样本的基于图像的UMAP空间,并显示指定聚类的代表性图像。(g) 所有四个生物学重复的伪时间排序图像。(h) CRP排序伪时间中指定蛋白的表达水平。
+ + + + + + + + + + +
结 论
本研究从福尔马林固定、石蜡包埋的组织中单个细胞的三分之一处获得了高达4300种蛋白质的蛋白质组深度。该数据集揭示了一种潜在的临床可操作的过氧化物酶体上调,该上调先于经典的UPR。单细胞蛋白质组学数据表明,AAT的积累主要由细胞内因素引起,肝细胞间的应激传播极少。本研究将蛋白质组学数据与人工智能引导的基于图像的表型分析相结合,研究了多种疾病阶段,揭示了一种晚期肝细胞表型,其特征是球状蛋白聚集体和独特的蛋白质组学特征,尤其包括TNFSF10(也称为TRAIL)含量升高。这种表型可能代表疾病进展的关键阶段。本研究为AATD的发病机制提供了新的见解,并引入了一种强大的方法,用于对复杂组织进行高分辨率的原位蛋白质组学分析。该方法有望揭示各种蛋白质错误折叠疾病的分子机制,为在单细胞水平上理解人类组织中的疾病进展树立新的标准。
+ + + + +



 English
English


