文献解读|Cell(42.5):人类 50 年寿命的综合蛋白质组图谱揭示衰老轨迹和特征
✦ +
+
论文ID
原名:Comprehensive human proteome profiles across a 50-year lifespan reveal aging trajectories and signatures
译名:人类 50 年寿命的综合蛋白质组图谱揭示衰老轨迹和特征
期刊:Cell
影响因子:42.5
发表时间:2025.07.25
DOI号:10.1016/j.cell.2025.06.047.
背 景
在哺乳动物中,人类以寿命长而著称,然而这也伴随着系统性衰老的负担。衰老伴随着器官功能的下降和慢性疾病风险的升高,尤其是心血管系统疾病。许多慢性疾病的发生都与器官衰老有关,这凸显了该领域的研究在制定延缓衰老和相关病理的策略方面具有巨大潜力。然而,目前的研究对单个人体器官衰老模式的理解仍然不充分,而控制多器官衰老复杂相互作用的分子机制在很大程度上是未知的。蛋白质是生命的基石。然而,人体组织衰老的蛋白质组学图谱仍未构建。
实验设计
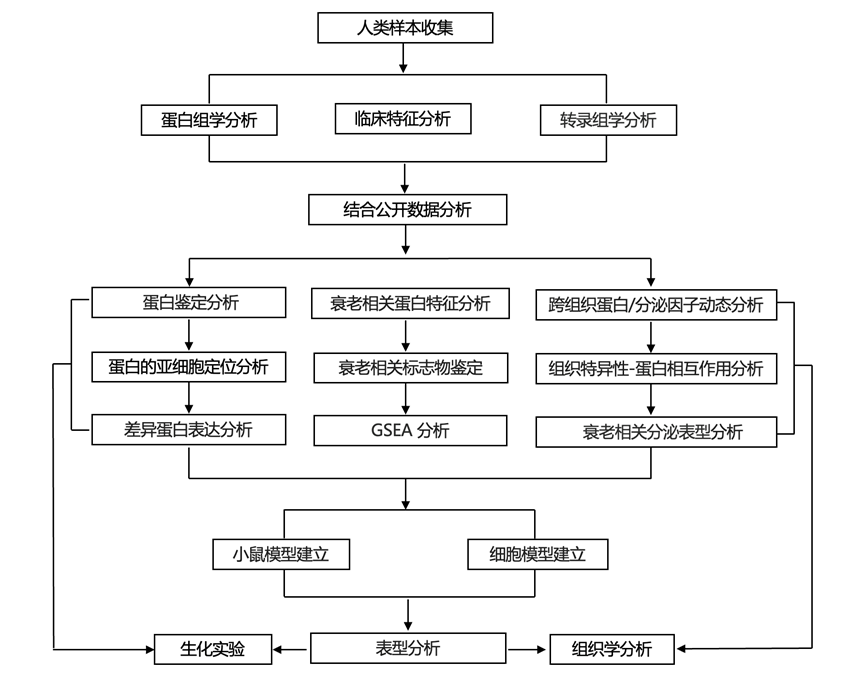
结 果
01
半个世纪以来人类器官衰老的蛋白质组学概要
为了阐明人类衰老的复杂机制,研究团队着手编撰一部蛋白质组百科全书,涵盖14至68岁个体(包括两种性别)的组织样本(图1 A)。他们精心挑选的样本反映了功能多样性及其与衰老的相关性,涵盖了七个身体系统的组织:心血管系统(心脏和主动脉)、消化系统(肝脏、胰腺和肠道)、免疫系统(脾脏和淋巴结)、内分泌系统(肾上腺和白色脂肪)、呼吸系统(肺)、外皮系统(皮肤)和肌肉骨骼系统(肌肉),以及血液样本。
他们使用最先进的质谱技术对每个样本进行了定量蛋白质组学分析,并同时进行了转录组学分析。这种严格的方法产生了超过 12771 种不同蛋白质的综合目录,涵盖了所有染色体上的人类蛋白质编码基因组(图1B-C)。除了对翻译和代谢功能至关重要的高丰度蛋白质之外,他们还鉴定出了大量跨组织的低丰度蛋白质,包括转运蛋白和激素调节剂(图 1D)。他们还根据检测到的蛋白质的亚细胞定位、细胞成分和分子功能分析了它们的特征。大多数蛋白质位于细胞内,同时还检测到了膜结合蛋白和分泌蛋白。大量蛋白质定位于细胞核和细胞器区室,尤其是线粒体。功能上,这些蛋白质涵盖多种作用,包括转录和表观遗传调控以及受体-配体信号传导,并且在组织间具有显著的异质性(图 1 E)。均匀流形近似和投影(UMAP)揭示了高度组织特异性的蛋白质组学特征,心脏和骨骼肌之间以及脾脏和淋巴结组织之间存在明显的相似性。他们鉴定了组织富集和组织增强的蛋白质,以及跨组织常见的蛋白质。组织富集的蛋白质具有不同的表达谱,强调了每种组织的特定生理作用。即使在类似的器官内,本研究也能精确地鉴定出差异表达蛋白(DEP),并通过免疫印迹法验证了特定表达,包括 SULT1B1,一种肝脏外来化合物代谢酶;PNLIPRP2 是一种水解半乳糖脂的胰脂肪酶;水通道蛋白 4 (AQP4) 是一种肌肉中的肌膜蛋白;以及桥粒蛋白 2 (DSG2) 是一种心脏中的桥粒蛋白。此外,他们还研究了生物性别对组织中蛋白质表达的影响,发现只有少数蛋白质表现出性别差异的丰度,例如女性心脏中的表观遗传调节因子 SGF29 和男性白色脂肪组织中的基质金属蛋白酶 3 (MMP3)。
蛋白质稳态是一个包含控制蛋白质合成、折叠、修饰、转运和降解的细胞机制的系统,是细胞健康的一个关键方面。为了评估蛋白质组学模式的转录调控,他们将蛋白质组学谱与转录组数据进行了比较。超过 95%的已鉴定蛋白质显示出可检测到的转录信号,但 mRNA 和蛋白质水平之间的相关性仅为中等程度(图1F-G)。正相关性随着年龄的增长而减小,在脾脏、肌肉和淋巴结中尤为明显,强调了蛋白质和转录之间存在与年龄相关的脱钩(图 1 H)。值得注意的是,这些解偶联蛋白对于组织功能维持至关重要,例如调节脾脏中的B细胞活化。这些发现强调了衰老器官中mRNA和蛋白质水平之间日益增大的差异,强调了了解衰老蛋白质组学方面的重要性。
接下来,他们研究了整个蛋白质代谢生命周期中的关键通路,这些通路可能会影响蛋白质质量控制能力,并随后导致衰老过程中 mRNA-蛋白质解偶联(图 1 I)。在翻译水平上,他们观察到大多数组织中参与蛋白质合成的关键蛋白质的丰度下降,包括细胞质和线粒体核糖体蛋白以及氨酰-tRNA 合成酶和肽基-tRNA 水解酶(图 1 I)。这表明翻译能力可能会随着年龄的增长而下降。翻译后,发现参与折叠、组装和运输的蛋白质,例如含分子伴侣的 T 复合体蛋白 1 亚基 α (TCP1)、Sec1/Munc18 家族、内质网膜复合体和核孔复合体中的蛋白质,会随着衰老而减少(图 1 I)。例如,组氨酰-tRNA 合成酶 1 (HARS1),一种组氨酰-tRNA 合成酶;含 TCP1 亚基 5 的伴侣蛋白 (CCT5) 和含 TCP1 亚基 7 的伴侣蛋白 (CCT7),环状伴侣蛋白 T 复合物蛋白环复合物 (TRiC) 的亚基;以及蛋白酶体亚基 β 型 1 (PSMB1),一种 20S 蛋白酶体的非催化亚基,在衰老组织中的蛋白质水平均降低。与蛋白质质量控制的下降一致,淀粉样蛋白与免疫球蛋白和补体一起积累(图 1 I)。蛋白质组学数据分析和组织免疫荧光分析证实了淀粉样蛋白的积累,例如血清淀粉样蛋白A1(SAA1)和血清淀粉样蛋白A2(SAA2),以及免疫途径的过度激活(例如免疫球蛋白λ常数1 [IGLC]、免疫球蛋白重常数α1 [IGHA]和补体C4A)(图1 I-J)。考虑到异常淀粉样蛋白沉积可触发免疫球蛋白激活,从而导致补体途径参与,淀粉样蛋白-免疫球蛋白-补体轴可能构成衰老组织微环境的重要组成部分。

图1. 多组织蛋白质组图谱概述了年龄和组织相关蛋白质的特征。
(A) 研究示意图。(B) 左图:每种组织中鉴定出的蛋白质数量。右图:蛋白质大小的密度分布,颜色越深表示数量越多。(C) 检测到的蛋白质在组织中的染色体分布,红色表示密度较高。(D) 左图:跨组织蛋白质丰度热图。右图:高/低丰度蛋白质的富集情况。(E) 按亚细胞定位、细胞成分和跨组织功能划分的检测蛋白质点图。(F) 每种组织的蛋白质环形图。(G) 每种组织的 mRNA-蛋白质 Spearman 相关性的密度图。(H) 按年龄分层的 mRNA 和蛋白质水平的 Spearman 相关性的小提琴图。(I) 左图:蛋白质稳态中与衰老呈负相关的蛋白质。右图:与衰老呈正相关的蛋白质。(J) 淋巴、心脏和肠道中SAA1/2、IGLC、IGHA和C4A的免疫荧光(IF)染色。
02
人体器官衰老的蛋白质组学动力学和生物标志物
为了揭示人类蛋白质组的终生动态,他们重点研究了与衰老相关的具有差异丰度的蛋白质,鉴定出大量在人类衰老过程中至少一个器官中表现出表达改变的年龄依赖性蛋白质。在各种组织中都观察到了年龄依赖性的 DEP,其中一些组织表现出明显的衰老敏感性(图 2 A)。通过深入表征所有 DEP 在各个器官中的表达模式,他们鉴定出上调和下调 DEP 的不同模块。该分析揭示了器官特异性蛋白质特征,反映了与衰老相关的动态变化(图 2 B-C)。上调的 DEP 模块 1 在组织中普遍存在且随着年龄增长而持续上升,它包含参与补体激活、免疫反应和淀粉样蛋白原纤维形成的蛋白质(图 2 C),强调这些蛋白质形成了一个“蛋白质群落”,并随着组织衰老而协同增加。其他模块主要由随年龄增长而增加的组织特异性DEP组成,相应的通路分别在主动脉、肺、心脏、脾脏和淋巴结中显著富集(图 2 C)。关于下调的DEP,他们检测到与高尔基囊泡转运和蛋白质成熟相关的蛋白质在不同组织中持续减少。其他模块由随年龄增长而逐渐下降的组织特异性DEP组成,不同组织中下调的通路部分反映了衰老引起的组织功能衰退(图 2 C)。
虽然大多数 DEP 是组织特异性的,但发现大约 40% 在至少两种组织之间共存(图 2D-E)。值得注意的是,31 种蛋白质在超过六种组织中一致下调,而在任何器官中均未上调,这些称为随衰老普遍下调的蛋白质 (UDPA),包括参与前 mRNA 剪接的PRPF4(图 2E-F)。相反,29 种蛋白质在超过六种组织中持续上调,而没有相互冲突的趋势(图 2E-F),这些指定为随衰老普遍上调的蛋白质 (UUPA),与补体激活、炎症反应和细胞粘附有关。其中,血清淀粉样蛋白 P 成分(SAP,由APCS编码)是最突出的 UUPA,它是一种典型的淀粉样因子,也是肝脏中 mRNA-蛋白质解偶联的主要蛋白(图 2 E-G),组织学染色证实了它在多种老年组织中的升高(图 2 H)。这种蛋白质随着衰老而上调可能会促进血管老化、损伤和炎症,因为用重组 SAP 蛋白治疗人主动脉内皮细胞 (hAEC) 会增加 SA-β-Gal 阳性,损害管腔形成,增强免疫细胞粘附,并增加白细胞介素 6 (IL-6) 的分泌。

图2. 年龄依赖性DEP的分子表征。
(A) 上图:LOESS 拟合的各组织上调 (左) 和下调 (右) DEP 的缩放表达轨迹(显示数量和比例)。下图:各组织和年龄段上调和下调 DEP 的缩放表达热图,并标明了亚细胞定位分布。(B) 不同组织中上调(左)和下调(右)DEP模块的平均Spearman相关系数热图。(C) 10 个 DEP 模块的年龄轨迹,其丰度增加(上)或减少(下)。(D) 共有和组织特异性上调(左)和下调(右)DEP 的 Circos 图。(E) 不同组织中上调(左)和下调(右)的DEP热图。(F) GO分析。(G) 各组织 SAP 蛋白水平随年龄增长而增加。(H) 免疫组织化学 (IHC) 染色显示年龄相关的 SAP 在各组织中上调。
03
老年人体器官生物通路的扰动
为了阐明衰老器官的蛋白质组学变化,他们建立了一个衰老标志评估系统来追踪衰老特征。该系统包括细胞周期停滞、基因组不稳定性、异染色质缺失、炎症和纤维化的标志物(图 3 A)。与蛋白质组学数据一致,组织学染色显示 p21 Cip1表达升高、DNA 损伤信号增强、异染色质标志物 H3K9me3 减弱、促炎因子 IL-6 增加,以及老化组织中 IV 型胶原蛋白指示的组织纤维化增多,所有这些都是已确定的衰老生物标志物(图 3 B)。表观遗传不稳定性是衰老的关键驱动因素,这促使他们进一步探究与衰老相关的表观遗传调控蛋白的变化,包括调节 DNA 甲基化、组蛋白修饰、染色质重塑和 RNA 表观遗传学的蛋白(图 3 C)。值得注意的是,YTHDC1 成为跨组织最持续下调的表观遗传调节因子,其在老年肝脏和肾上腺组织中的表达降低通过组织学染色进一步得到验证。在衰老标志中,他们还观察到与线粒体生物合成、体内平衡和呼吸有关的线粒体蛋白普遍下调,强调了线粒体在衰老中的重要性(图 3 D)。
蛋白质通常在复合物内发挥作用,这促使他们对复合物组进行定量分析,以揭示与衰老相关的改变。本研究分析了总共816个蛋白质复合物,观察到转录调控复合物(例如AR-NONO-SFPQ)和RNA剪接复合物(例如剪接体)在不同组织中的下调(图3 E)。相比之下,上调的复合物在各种组织中都富集于免疫和炎症反应(例如MAVS-TRADD)以及细胞外基质和细胞粘附(例如ITGA3-ITGB5)中(图3 E)。基因集富集分析(GSEA)证实了这些发现,揭示了上调的复合物主要富集于炎症小体通路,而下调的复合物与核激素受体、核转运和剪接体相关(图3 F)。
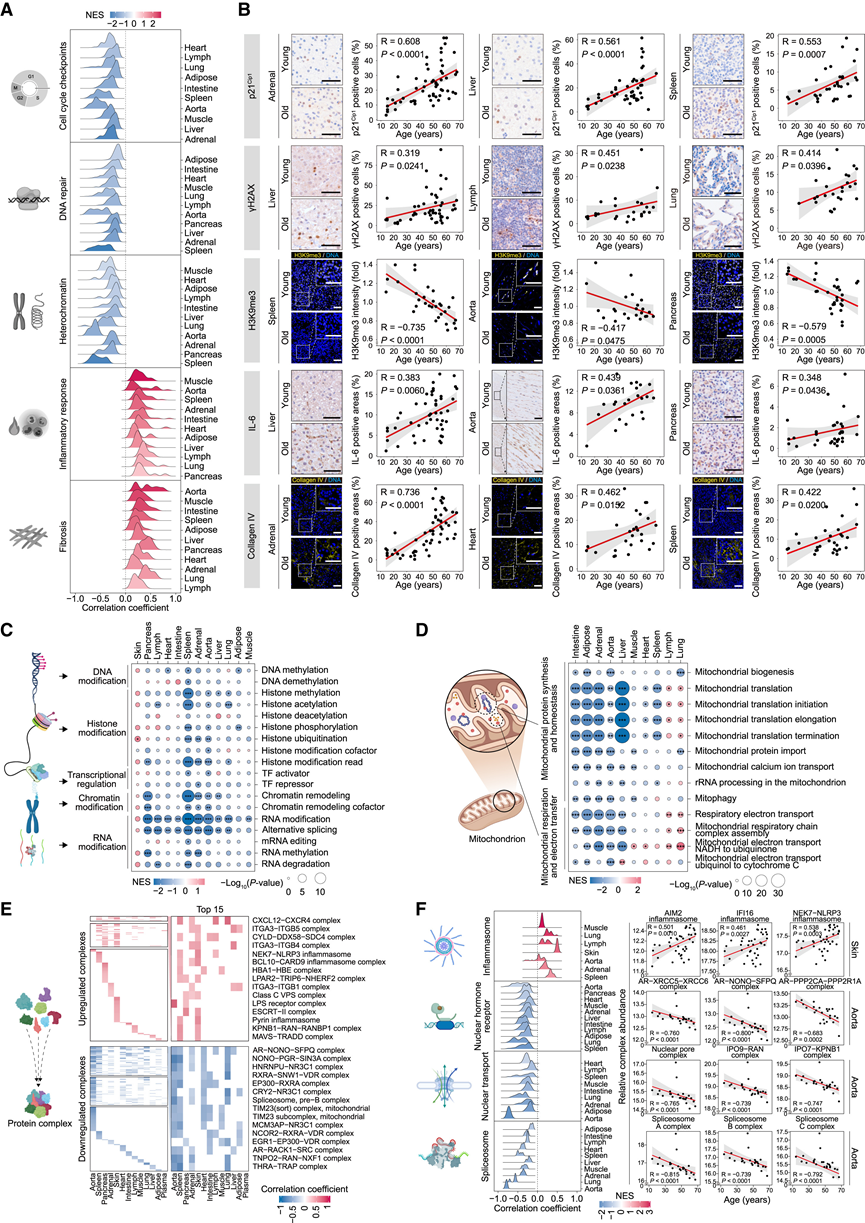
图3. 共有的衰老蛋白质组学特征汇聚在跨组织的核心通路上。
(A) GSEA 中年龄相关蛋白质的脊图。(B) 组织中衰老标志物的免疫组化 (IHC) 或免疫荧光 (IF) 染色。(C) GSEA 得分与表观遗传途径富集p值的点图。(D) 线粒体通路GSEA 得分与富集p值的点图。(E) 各组织中上调(上)和下调(下)蛋白质复合物的热图。(F) 左图:蛋白质复合物组的GSEA。右图:各组织中代表性复合物丰度及其年龄相关性。
04
人体器官异质动态的蛋白质组衰老时钟
为了定量评估人体器官衰老速度的异质性,他们设计了一种计算每种组织生物年龄的创新方法(图 4 A),为13种人体组织建立了蛋白质组年龄时钟,扩展并补充了之前仅依赖血浆蛋白成分的时钟。采用弹性网络回归算法,确定了可以精确预测每种组织实际年龄的蛋白质,Spearman 相关系数从 0.74 到 0.95 不等(图 4 B)。他们进一步剖析了驱动组织特异性时钟的关键蛋白质。特别值得注意的是,金属蛋白酶抑制剂 3(TIMP3),一种金属蛋白酶的调节剂,确定为九个不同器官的组织时钟的贡献者。随后的免疫染色证实,TIMP3 在各种组织中表现出与年龄相关的增加。
通过对人类生命周期的蛋白质组学分析,他们精确定位了跨越衰老早期、中期和晚期阶段的DEP。虽然患病率较低,但与体液免疫反应和RNA剪接相关的衰老早期DEP会导致所有年龄组的衰老DEP,尤其是在胰腺和主动脉中的影响更为显著。中年DEP在整个生命周期的衰老DEP中占了相当大的比例,这强调了体液免疫反应和补体激活在多个组织中的扩增,以及中年RNA剪接的失调。此外,基于滑动窗口的累积分析显示,许多组织在 50 岁左右,尤其是在 45 至 55 岁之间,会发生显著的蛋白质组重塑(图 4 C-D)。在所有器官中,主动脉在整个生命周期中表现出最明显和最连续的蛋白质组波动。在 30 岁时,除主动脉、脾脏和肾上腺外,大多数组织中 DEP 的总体比例仍然较低,其中肾上腺显示出更显著的蛋白质表达变化(图 4 C)。这表明内分泌稳态的改变可能是系统性衰老的起始事件之一,这与之前的研究结果一致。在45岁和55岁时,各器官中 DEP 的积累加剧,其中主动脉显示出最突出的变化,强调其对衰老的特殊敏感性。与此同时,胰腺和脾脏也表现出持续的蛋白质组重塑,这可能反映了衰老相关的代谢和免疫功能的衰退。功能上,30岁时的早期改变主要与rRNA代谢和翻译有关,而45岁和55岁时的转变则主要集中在RNA剪接和蛋白质加工相关通路上。这些数据共同凸显了器官衰老的动态性和异质性,其中脉管系统是最早和受影响最严重的系统之一。
为了阐明衰老相关分泌表型 (SASP) 的复杂性,他们通过对衰老相关分泌组和成熟的 SASP 集合进行综合分析。总体而言,他们鉴定了579种不同的 SASP 蛋白,其中约一半在至少两种组织中共存(图 S6D)。趋化因子 CXCL12 94在九种组织中积累(图 4E),并通过在衰老人体组织中进行免疫染色进行了验证(图 4F)。此后,衰老组织或细胞释放的细胞因子统称为衰老因子。
分泌蛋白是器官间通讯的关键介质,然而,他们对这些相互作用如何随着人体器官的衰老而变化的理解有限。通过 CellPhoneDB 分析了与衰老相关的分泌蛋白动态,并绘制了跨组织的配体-受体相互作用图(图 4 G)。通过这种方法,他们发现了潜在的器官间通讯网络,其中主动脉、脾脏和淋巴结等免疫组织以及肾上腺等内分泌器官与其他组织表现出广泛的相互作用。值得注意的是,这些器官间相互作用会随着年龄的增长而增强,主要由涉及炎症趋化因子 CXCL12 和 CXCL14 的受体-配体对驱动。相比之下,Ephrin 家族成员 Ephrin A1 (EFNA1)、ephrin B1 (EFNB1) 和 ephrin B2 (EFNB2) 的器官间相互作用随着年龄增长而减少,这些成员通过 Eph 受体介导双向信号传导,并参与调节细胞迁移、组织边界形成和血管发育。
鉴于蛋白质通过血液介导器官间相互作用,他们整合了血浆蛋白质组学数据,以在蛋白质水平上阐明这些长距离、血浆介导的相互作用。他们鉴定出 24 对配体-受体对,它们通过血浆介导组织通讯并表现出与年龄相关的变化,主要源自主动脉和脾脏。这凸显了血管和免疫组织在协调多器官衰老中的关键作用(图 4H-I)。鉴于动脉衰老较早且显著,这些发现进一步支持了动脉可能是系统性衰老(称为“senohub”)的主要起源。它们不仅对衰老相关的变化高度敏感,而且还是分泌性促衰老蛋白(称为衰老蛋白)的主要来源,可放大系统性衰老信号。值得注意的是,生长停滞特异性6 (GAS6)——一种在血浆及其来源组织——主动脉中均升高的senokine——与广泛表达的TAM受体(TYRO3、AXL和MERTK)的相互作用增强(图4 I)。这种相互作用可能激活促血栓信号通路,导致内皮功能障碍和动脉病。
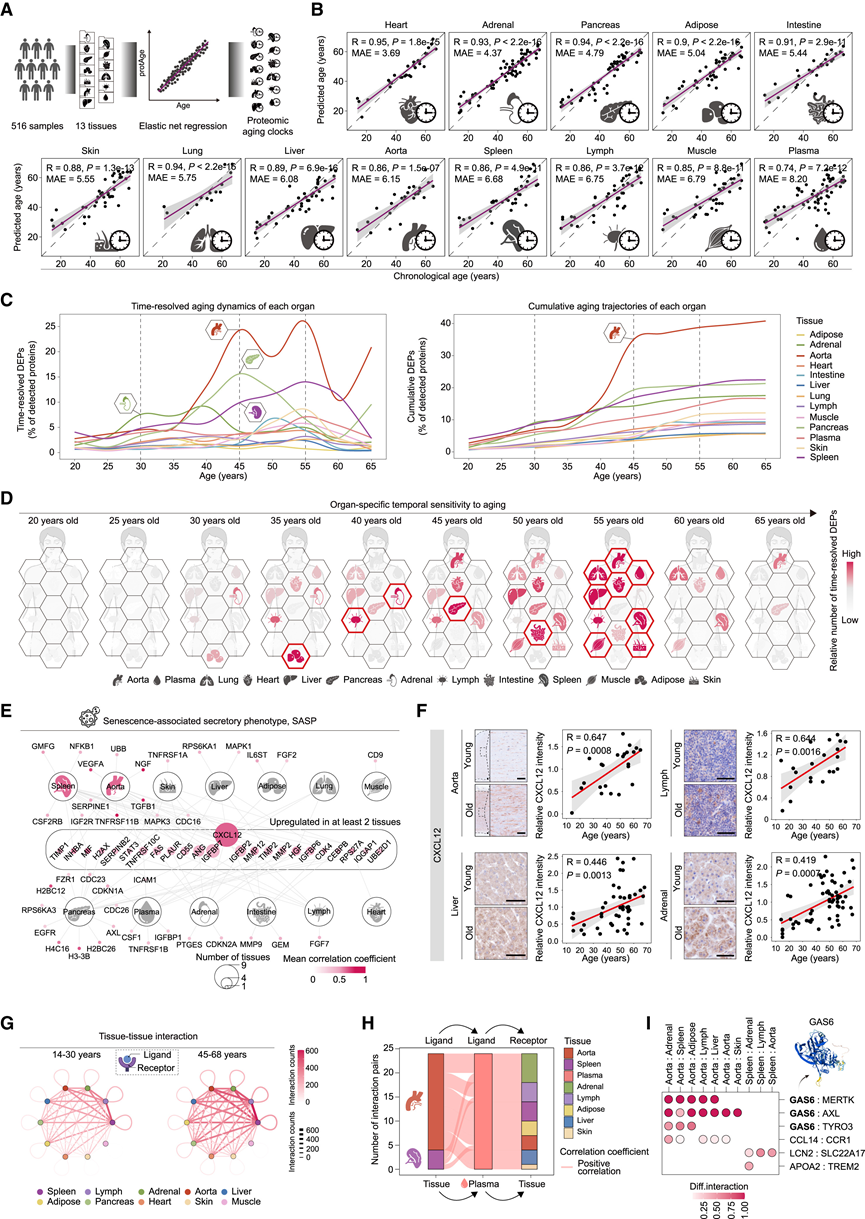
图4. 衰老相关蛋白质和分泌因子的动态分析。
(A) 使用弹性网络回归构建蛋白质组衰老时钟的示意图。(B) 衰老时钟在不同组织中的表现。(C) 不同年龄段动态DEP的滑动窗口分析。(D) 跨组织时间分辨DEP的数字体图。(E) 年龄依赖性上调分泌蛋白网络,与已知 SASP 基因集重叠。(F) 免疫组化 (IHC) 验证多种组织中年龄相关性 CXCL12 表达升高。(G) 组织相互作用网络分析。(H) 血浆介导的跨组织配体-受体相互作用的桑基图。(I) 血浆介导的配体-受体相互作用的年龄相关性变化点图。
05
细胞和小鼠模型验证
为了验证这一假设,他们首先使用免疫组织化学染色和 ELISA 验证了人类血管组织和血浆中 GAS6 的年龄相关性上调(图 5 A-B)。然后,他们用重组人 GAS6 蛋白处理人血管平滑肌细胞 (hAEC) 和人血管平滑肌细胞 (hVSMC)(图 5 C)。在 hAEC 中使用 GAS6 处理可增加 SA-β-Gal 阳性率和 p21Cip1表达,削弱血管形成和迁移能力,增加 IL-6 分泌,并增强免疫细胞粘附(图 5 D-I)。同样,在 hVSMC 中,senokine GAS6 加速细胞衰老并升高炎症细胞因子水平(图5J-L)。
为了评估循环 GAS6 的体内效应,他们每 5 天给 8 个月大的小鼠静脉注射重组小鼠 GAS6,共注射 4 次(图 5 M)。在生理水平上,GAS6 治疗的小鼠表现出身体机能受损,包括握力下降、挂线耐力下降、平衡和协调能力下降,证据是平衡木测试中的脚滑增加和穿越时间延长(图 5 N)。组织学分析显示出明显的血管老化标志,包括 p21Cip1表达升高、氧化性 DNA 损伤(8-OHdG)增加和内源性逆转录病毒(MMTV)表达增强(图 5 O)。GAS6治疗还促进脂质沉积,同时上调主动脉内炎症标志物 S100A8 和血管损伤标志物 von Willebrand 因子 (vWF) 的表达(图5O)。除血管组织外,GAS6 还促进了多个靶器官的加速衰老表型(图5P-S)。在肝脏中,GAS6 处理增加了 p21Cip1的表达,降低了 H3K9me3 水平,刺激了免疫浸润和脂质积聚(图5P)。在脾脏中,GAS6 破坏了白髓的结构完整性,并提高了 p21 Cip1和 IL-6 的表达(图5Q)。GAS6 处理增加了淋巴结和肾上腺中炎症标志物 IL-6 和 S100A8 的表达,同时增加了淋巴结中 DNA 损伤标志物 γH2AX 的表达(图 5R-S)。总之,这些研究结果表明,GAS6 升高有助于加速血管和全身衰老。
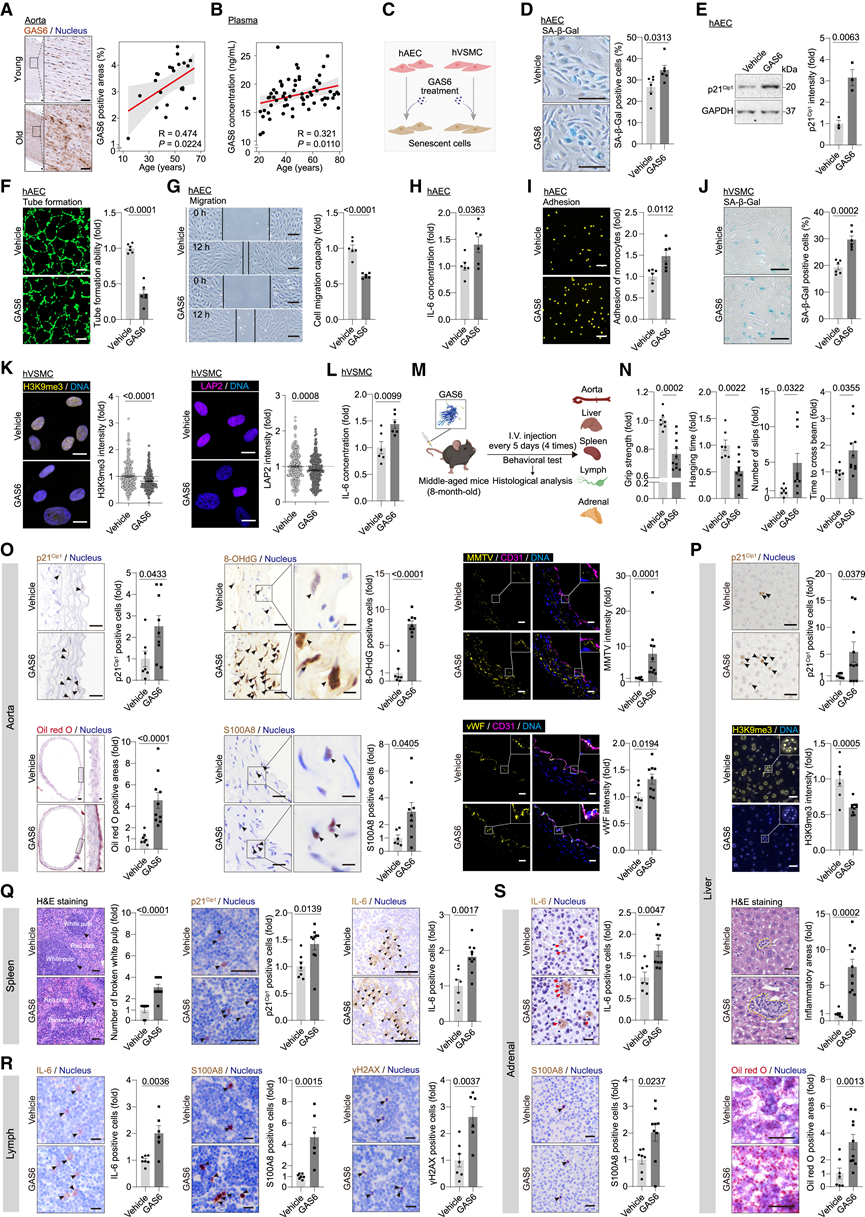
图5. GAS6促进人类内皮细胞衰老和小鼠多器官衰老。
(A) 不同年龄个体血管壁GAS6的IHC染色。(B) ELISA检测显示不同年龄段血浆GAS6水平。(C) GAS6 在 hAEC 和 hVSMC 中治疗的示意图。(D-I) SA-β-Gal 染色、免疫印迹、管形成实验、迁移实验、ELISA和单核细胞粘附实验。(J) 用载体或GAS6处理的hVSMC中的SA-β-Gal染色。(K) IF 染色。(L) ELISA 检测。(M) 实验设计。(N) 对小鼠进行功能测试。(O-S)组织学和免疫荧光染色分析。
06
预测器官衰老的循环蛋白生物标志物
揭示器官衰老的血液生物标志物对于非侵入性衰老评估至关重要。他们整合了血浆和器官蛋白质组学数据,以鉴定两者中具有一致变化的蛋白质,从而表征器官衰老的潜在液体生物标志物。采用这种方法,他们总共鉴定了 211 种血浆-组织配对 DEP,它们随血浆中的衰老而变化,并在至少一个组织中显示出与血浆中相同方向的年龄依赖性变化(图 6 A)。在主动脉、肾上腺和脾脏中观察到的血浆-组织配对 DEP 数量最多,突显了它们对与衰老相关的血浆蛋白质组成变化的影响。此外,他们主要关注上调的 DEP。约 40% 的血浆-组织配对 DEP 仅存在于单个组织中(图 6 A)。值得注意的是,他们鉴定了几种血浆-组织配对的 DEP,它们与血浆和至少一种组织相对应,并且这些蛋白质在衰老血浆中表现出显著的积累。例如,已报道的衰老相关抗原 GPNMB已证实在衰老血浆中积累。此外,他们还鉴定了一系列血浆-组织配对的衰老生物标志物,包括 COMP、CHI3L1、NOTCH3、ITLN1、EFEMP1、HTRA1 和 LTBP2,并通过 ELISA 进一步验证了它们在人血浆中的升高(图6B)。他们还通过组织学免疫染色证实了多种组织中 GPNMB、COMP、NOTCH3、HTRA1 和 LTBP2 蛋白的衰老相关上调,其中在主动脉中观察到最显著的增加(图 6C)。他们还发现了血浆-组织配对蛋白(包括 HARS1、CCT5 和 PSMB1)的年龄依赖性下调。值得注意的是,HARS1是一种与神经退行性疾病和自身免疫性疾病相关的蛋白质,在组织中表现出最广泛的下降。ELISA 和免疫组织化学进一步证实了血浆中 HARS1 的年龄相关性减少以及其在主动脉中的减少。他们假定基于血浆蛋白的时钟可以作为由实际组织蛋白基质构建的器官时钟的替代品。因此,他们使用机器学习算法开发了一种血浆蛋白代理组织衰老时钟,其实现与组织蛋白基质衍生时钟相当的年龄预测精度,并可区分不同组织的衰老。
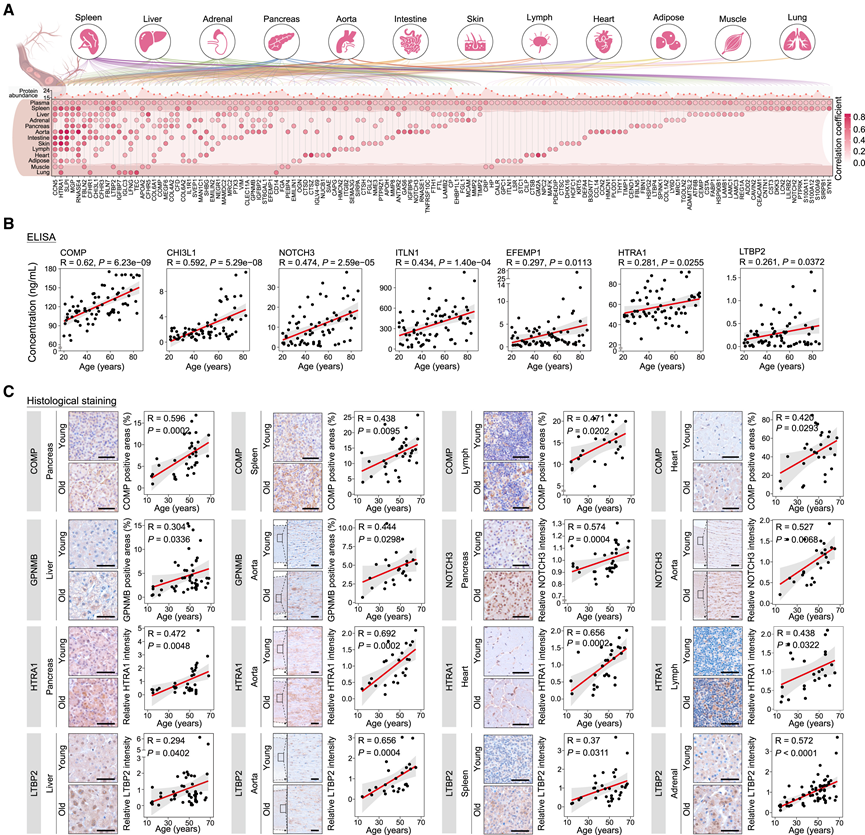
图6. 人类血浆和组织中协同上调的蛋白质。
(A) 血浆和组织中DEP随年龄共同上调的点图。(B) ELISA 分析所示 DEP 的血浆蛋白水平。(C) 对按年龄分层的组织中年龄上调蛋白进行免疫组化染色。
07
体液衰老蛋白驱动血管和系统衰老
接下来,他们探究了血浆中积累的特定衰老蛋白是否能够驱动血管老化,因为它们与血管壁,尤其是内皮细胞直接相互作用(图 7 A-B)。为了验证这一假设,他们用随年龄增长而增加的重组血浆蛋白处理 hAEC(图 7 B)。七种蛋白质——GPNMB、COMP、HTRA1、SLPI、IGFBP7、NEGR1 和 NOTCH3——诱导了血管内皮衰老的标志性特征。这些特征包括 SA-β-Gal 活性增加、p21Cip1表达升高以及 H3K9me3 和 LAP2 水平降低(图 7 C-F)。还观察到促炎细胞因子(IL-6和IL-8)和内皮功能障碍标志物(VCAM1)表达升高、迁移和管道形成受损、单核细胞粘附增强以及 IL-6 分泌增加(图 7 G-J)。
转录组分析进一步表明,用这些蛋白质治疗可激活典型的衰老相关基因并上调与细胞衰老、氧化应激和炎症相关的通路。为了确定这些影响是否超出内皮细胞的范围,他们用 GPNMB、HTRA1 和 IGFBP7 处理 hVSMC,结果同样诱导了衰老表型,包括 SA-β-Gal 活性升高、H3K9me3 降低、LAP2 受损以及 IL-6 表达增加。为了验证与衰老相关的血浆蛋白是否可驱动血管老化和随后的系统性衰退,他们通过静脉注射 GPNMB 检测了中年小鼠。GPNMB 处理的小鼠握力下降,运动协调性和平衡能力受损(图 7 K)。组织学分析显示,GPNMB 加速了血管老化,其特征包括 DNA 氧化增加、逆转录转座子再激活、血管壁细胞细胞周期停滞、内皮损伤(vWF 上调)、血管炎症和脂质积聚增加(图 7L-R)。总之,这些发现表明,衰老组织分泌的衰老蛋白可以放大促衰老信号,介导血管和多器官的退化。
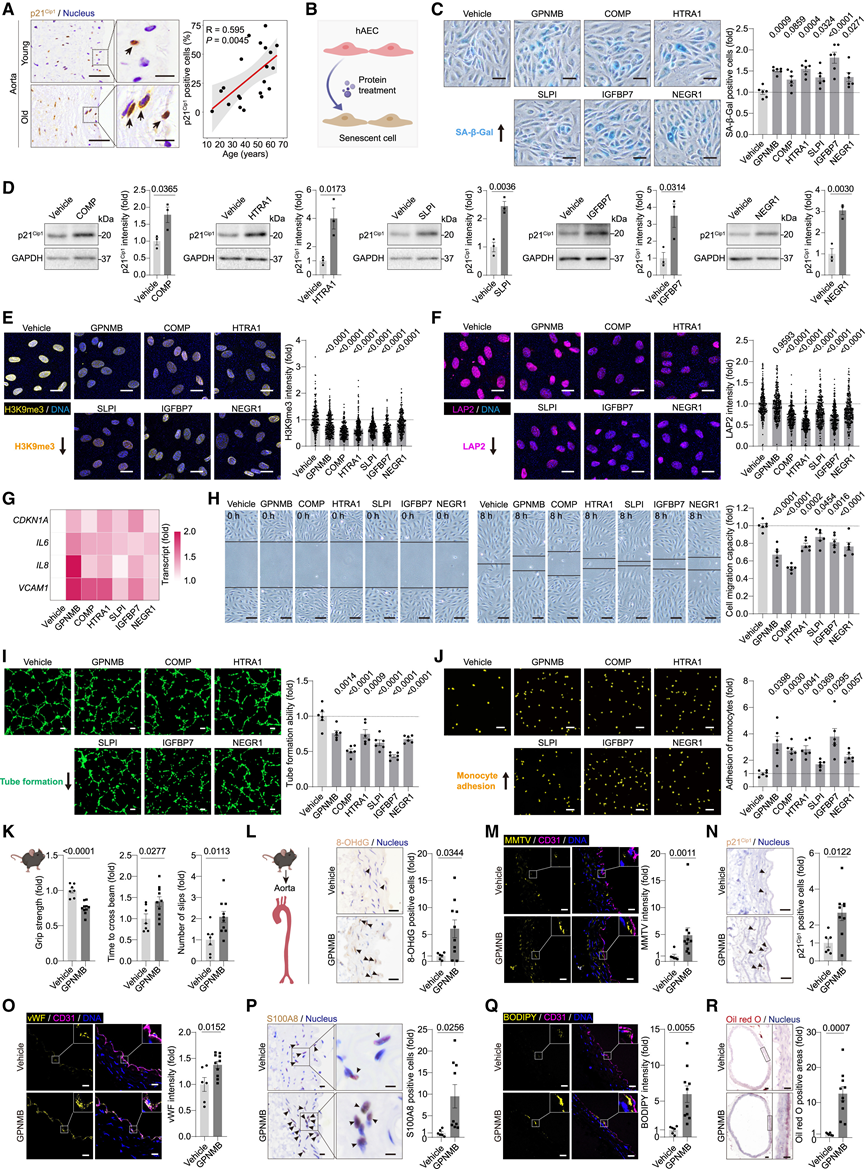
图7. 血浆衰老蛋白诱导血管和系统衰老。
(A) 左图:从年轻到衰老人类主动脉中 p21 Cip1的免疫组化染色。右图:应用 Spearman 相关性分析。(B) 实验示意图。(C) SA-β-Gal染色。(D) 免疫印迹分析。(E-F) 免疫荧光染色。(G-J) 衰老相关基因的RT-qPCR、迁移分析、管腔形成和单核细胞粘附分析。(K) 小鼠的握力、横梁穿过时间和足滑。(L-R) 小鼠主动脉的IHC和IF染色。
+ + + + + + + + + + +
结 论
本研究对来自13种人体组织的516个样本,跨越50年的时间,进行了全面的蛋白质组学和组织学分析。这份动态图谱揭示了广泛的转录组-蛋白质组脱钩和蛋白质稳态下降,其特征是淀粉样蛋白的积累。基于衰老相关的蛋白质变化,本研究开发了组织特异性的蛋白质组年龄时钟,并描述了器官水平的衰老轨迹。时间分析显示,衰老拐点出现在50岁左右,而血管是一种较早衰老且极易受衰老影响的组织。本研究进一步定义了与其组织来源相匹配的衰老血浆蛋白质组学特征,并鉴定了包括GAS6在内的驱动血管和全身衰老的候选衰老蛋白。总之,这项研究成果为从蛋白质的视角系统性地理解人类衰老提供了新的理论依据。
+ + + + +



 English
English


