文献解读|Cancer Cell(44.5):全面的肿瘤免疫分析揭示了肉瘤样肾细胞癌中矛盾免疫敏感性的介质
✦ +
+
论文ID
原名:Comprehensive tumor-immune profiling reveals mediators of paradoxical immune sensitivity in sarcomatoid renal cell carcinoma
译名:全面的肿瘤免疫分析揭示了肉瘤样肾细胞癌中矛盾免疫敏感性的介质
期刊:Cancer Cell
影响因子:44.5
发表时间:2025.07.23
DOI号:10.1016/j.ccell.2025.07.010
背 景
肾细胞癌 (RCC) 肿瘤包含多种组织学上不同的上皮亚型。最常见的是透明细胞肾细胞癌 (ccRCC),占 RCC 的 75%。伴肉瘤样去分化的 RCC (sRCC) 是一种罕见的组织型,其特征是梭形细胞形态。虽然 sRCC 仅占 RCC 诊断的 5%,但高达 80% 的 sRCC 患者病情进展至晚期,且 sRCC 患者的生存期很少超过一年,使其成为最具侵袭性的泌尿系统恶性肿瘤之一。sRCC的独特之处在于它能够从各种上皮性 RCC 亚型(最常见的是 ccRCC)发展而来,并且肉瘤样特征通常以病灶形式嵌套在上皮样 RCC 内。肉瘤样克隆是由上皮样 RCC 细胞通过上皮-间质转化 (EMT) 而产生的。然而,EMT 相关肉瘤样转化的含义和由此产生的生物学易感性仍未完全确定。sRCC 不仅具有高度侵袭性,还具有免疫炎症肿瘤微环境 (TME),与 ccRCC 相比,其程序性死亡配体 1 (PD-L1)、效应 T 细胞特征和炎症髓系程序表达丰富。针对程序性细胞死亡1 (PD-1)-PD-L1 轴的免疫检查点阻断(ICB)极大地提高了 ccRCC 患者群的生存率,并且没有任何一个亚群从 ICB 中获得的益处比对其他抗癌疗法有抗药性的 sRCC 患者更大。sRCC的这种 ICB 反应性可能部分由其炎症特征解释;然而,包括PD -L1 表达在内的炎症标志物不能预测 RCC 中的 ICB 反应。此外,ICB 在 RCC 中的抗肿瘤机制仍未完全了解。
实验设计
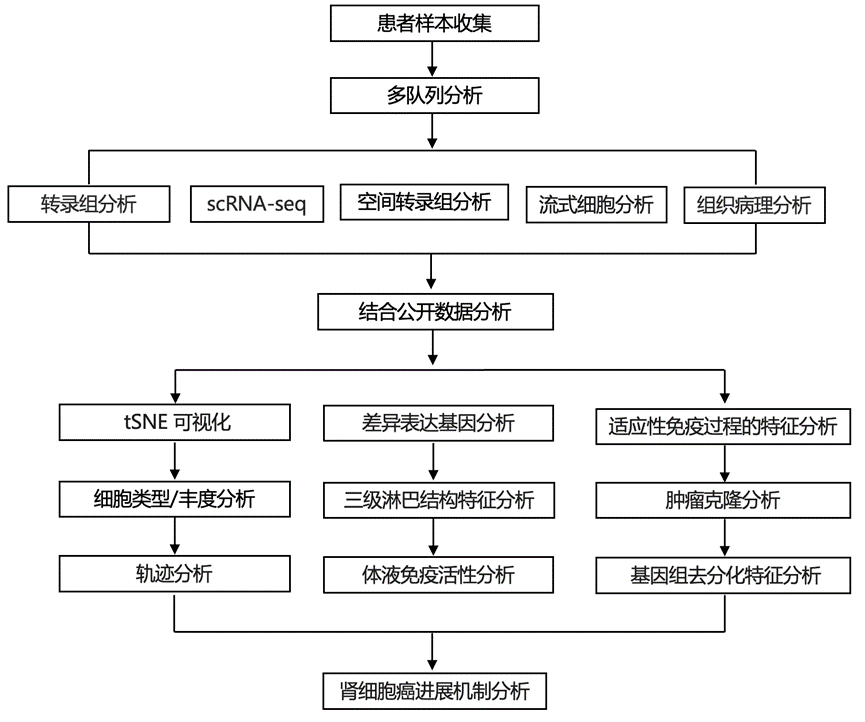
结 果
01
sRCC 中的 T 细胞表达活化和耗竭标志物
为了更好地了解与 sRCC 相关的细胞程序,研究团队对来自 IMmotion151 试验(688 名 ccRCC 患者,134 名 sRCC患者)的转录组数据进行了加权基因共表达网络分析。一个包含 173 个基因的单个模块与肉瘤样特征的存在显著相关。该模块内的蛋白质-蛋白质相互作用分析显示 T 细胞受体信号传导和 T 细胞活化通路显著富集,因此最初的询问集中在肿瘤浸润性 T 细胞上。他们前瞻性收集接受肾切除术的初治 RCC 患者的肿瘤标本,处理成单细胞悬浮液并冷冻保存,选择了一组经病理学确诊的 sRCC 和 ccRCC 病例进行分析(图 1 A)。使用 33 个标记物组进行全谱流式细胞分析以探究淋巴细胞群特征。他们还使用t 分布随机邻域嵌入 (tSNE) 进行降维,并根据谱系标记表达对聚类进行注释,结果显示 ccRCC 和 sRCC 之间整体 TME 组成没有明显差异(图1B-D)。
提取总计 138870 个CD8 + T 细胞群,然后再次进行降维和聚类(图 1 E)。在 25 个 CD8 + T 细胞聚类中,有 7 个聚类显著富集于 ccRCC(聚类 6、8、12、17、18、19 和 22),而有 3 个聚类显著富集于 sRCC(聚类 14、16 和 20)(图1E-G)。与 ccRCC 富集的聚类相比,在 sRCC 肿瘤中富集的聚类表达更高水平的抗原体验、活化和耗竭标志物,包括 CD45-RO、CCR5、PD-1、CD38 和 TOX(图 1 H)。相反,富含 ccRCC 的聚类表达了更高水平的幼稚和早期激活标记,包括 CD45RA、CD127 和 CCR7。
在 CD4 + T 细胞中,七个聚类(聚类 3、4、9、12、13、17 和 23)在 sRCC 中显著富集,而两个聚类(聚类 14 和 15)(图1I-K)在 ccRCC 中显著富集。sRCC 富集聚类的活化和耗竭标志物表达再次增强,而 ccRCC 富集聚类表达更多的幼稚/早期活化标志物(图1L)。聚类23 表达高水平的 CD25,与调节性 T 细胞表型一致,据报道在 sRCC 中富集。这些发现表明,与 ccRCC 相比,sRCC 中的肿瘤浸润性 T 细胞更加活跃。

图1. sRCC 中肿瘤浸润 T 细胞的全谱流式细胞分析。
(A) 在 sRCC 和 ccRCC 之间进行的分析。(B) 通过全光谱流式细胞分析的细胞 tSNE 减少。(C) 细胞群的相对丰度。(D) 映射到包含 ccRCC 和 sRCC 样本的 tSNE 坐标的谱系标记表达。(E) tSNE 减少 CD8 + T 细胞。(F) CD8+ T细胞聚类的相对丰度。(G) ccRCC 和 sRCC 中显著差异 CD8+ T 细胞聚类的相对丰度。(H) ccRCC 和 sRCC 中显著富集的 CD8+ T 细胞聚类中标志物表达的直方图。(I) tSNE 减少 CD4+ T 细胞。(J) CD4+ T细胞聚类的相对丰度。(K) ccRCC 和 sRCC 中显著差异 CD4+ T 细胞聚类的相对丰度。(L) 在 ccRCC 和 sRCC 中显著富集的 CD4+ T 细胞聚类中标志物表达的直方图。
02
CXCL13在 sRCC 肿瘤浸润 T 细胞中富集
接下来对 18 例患者肿瘤进行单细胞转录组分析 (scRNA-seq) ,产生 73123 个独特细胞,初始聚类产生 34 个聚类,然后根据典型谱系标记的表达将其浓缩为 13 个群体(图 2 A-C),细胞比例与先前报告的 RCC TME 一致。在 ccRCC 和 sRCC 中定量了细胞类别的相对丰度,sRCC 中的浆细胞丰度显著增加。
分离出CD8 + T 细胞(定义为CD3D和CD8A共表达,且不表达CD4)。重新进行聚类和降维,共得到 11 个聚类中的 13946 个细胞(图 2 D-E)。相对于 ccRCC,注释为增殖性(MKI67)、高干扰素刺激基因 (ISG)(IFI44、IFI44L和STAT1)和高CXCL13的 T 细胞的 sRCC 聚类在 sRCC 中更为丰富,含有 γ-δ (TRDC) 和自然杀伤 (NK) 样 T 细胞(NCAM1)(图 2 E-F)的聚类也是如此。相反,ccRCC 样本富集了一个注释为高热休克蛋白(HSPA1A和HSPA1B)的聚类,该聚类也表达早期活化标志物CD69、FOS和JUN。一个由包括IL2在内的细胞因子表达定义的聚类,该聚类同样表达早期活化标志物;以及一个表达PMCH的群体,同时表达终末衰竭标志物。从scRNA-seq 数据中获得的衰竭 T 细胞特征的表达对 ICB 反应具有预测能力,但在 IMmotion151 临床试验队列中的 sRCC 患者中未达到显著性,而在 ccRCC 患者中则未达到显著性。
为了进一步了解ccRCC和sRCC之间CD8 + T细胞分化状态的变化,他们进行了轨迹分析。由于γ-δ和NKT样CD8 + T细胞的独特分化特性,他们将其剔除,并绘制了源自干细胞样和终末分化CD8 + T细胞的特征图,以定义一个轨迹起源的聚类(图2 G)。三个谱系从干细胞样起源分支,并终止于以增殖标志物(MKI67)、耗竭标志物(TOX)和METRNL(重复抗原刺激的特征)表达为特征的区域(图2 G-H)。在不同谱系中,ccRCC 克隆在伪时间进展的早期阶段富集,而 sRCC 克隆主要分布在中期和末期(图 2 I),但TOX轨迹最终汇聚于以PMCH表达的终末耗竭聚类——该聚类主要由ccRCC浸润T细胞构成。这些结果验证了流式细胞的结果:ccRCC T 细胞表达更多早期活化程序,而 sRCC T 细胞则富集效应子和衰竭标志物的表达。
与CD8+T细胞类似,CD4+T细胞(表达CD3D但不表达CD8A/CD8B的淋巴样细胞)(图2L-M)在ccRCC中富集于初始样和早期激活亚群,而sRCC的T细胞则高表达包括CCL5在内的激活基因。CXCL13同样是sRCC与ccRCC CD4+T细胞中差异最显著的基因(图2N),且CXCL13高表达亚群在sRCC CD4+T细胞中的占比显著高于ccRCC。与CD8+T细胞一致,表达CXCL13的CD4+T细胞相对丰度在sRCC中更高。这种CXCL13的高表达在比较sRCC与上皮样RCC的RNA-seq数据集中得到验证:在Javelin101、TCGA KIPAN、CheckMate以及城市希望医疗中心(COH)转移性RCC患者队列中,CXCL13表达均一致性地在sRCC肿瘤微环境(TME)中富集(图2O)。
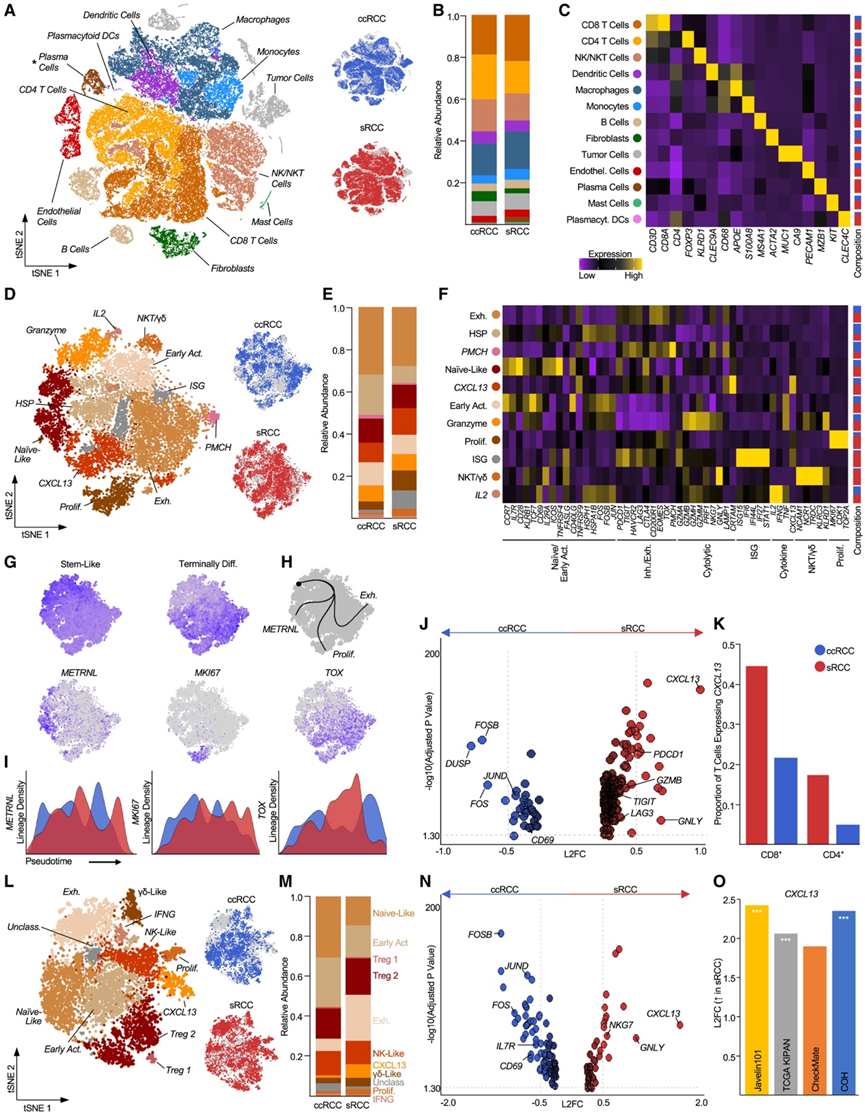
图2. sRCC中T细胞的scRNA-seq。
(A) tSNE 减少细胞群体(左)和起源组织学(右)。(B) 细胞群的相对丰度。(C) 用于定义人群的典型谱系标记基因表达热图。(D) 通过 Louvain 聚类和注释(左)以及根据来源组织学定义的(右)分离的 CD8+ T 细胞群的 tSNE 减少。(E) CD8+聚类的相对丰度。(F) 根据功能和/或表型对定义的 CD8 +聚类进行分类的基因热图。(G)干细胞样和终末分化 CD8 + T 细胞基因特征与 tSNE 的映射。 (H)轨迹分类的基因特征映射。(I) ccRCC 和 sRCC 样本中 CD8+ T 细胞群的密度随伪时间进展的轨迹变化。(J) ccRCC 和 sRCC 衍生的 CD8+ T 细胞之间的差异表达分析。(K) 表达CXCL13的 T 细胞丰度。(L) 通过 Louvain 聚类和注释(左)以及通过来源组织学(右)定义的分离 CD4 + T 细胞的 tSNE 减少。(M) CD4 +聚类的相对丰度。(N) ccRCC 和 sRCC 衍生的 CD4+ T 细胞之间的差异表达分析。(O) 在转录组数据集中,sRCC 相对于上皮样 RCC 中CXCL13的差异表达。
03
sRCC 内有丰富的三级淋巴结构
鉴于sRCC TME中CXCL13表达T细胞的富集现象,他们进一步探究了sRCC中三级淋巴结构(TLS)的存在。通过分析五个独立队列(TCGA KIRC、IMmotion151、CheckMate、HCRN-GU16-260和COH的肿瘤转录组数据,他们检测了两组TLS特征基因的表达:12-趋化因子特征和基于TLS阳性ccRCC空间转录组分析获得的Imprint特征。在所有队列中,sRCC肿瘤均一致性地显示出12-趋化因子和Imprint TLS评分的显著富集(图3 A)。
接下来,他们尝试通过H&E染色以及CD20和外周淋巴结地址素(PNAd)的免疫组化染色来识别sRCC组织切片中的TLS(图3 B)。在27/30例sRCC病例中发现了>15000 μm2的致密CD20 + B细胞聚集体,这可能提示TLS的存在,其中18/30例肿瘤中存在确诊TLS(以PNAd共表达为定义)(图3 C)。
采用空间转录组学方法来表征 8 例同时含有肉瘤样和透明细胞成分的 sRCC 肿瘤中 TLS 的存在、成分和成熟状态。Imprint 和卵巢癌衍生的 TLS 特征图谱显示在 sRCC 肿瘤基质中表达增强。随后,根据 Imprint TLS 表达,将 8 例 sRCC 病例中的 5 例归类为 TLS+,这也正确识别了先前工作中的7 例 TLS+样本(图 3 D)。TLS+区域与匹配的 TLS -区域的差异表达分析显示,sRCC 样本中 8 个基因保守富集,均与 B 淋巴细胞成熟和浆细胞功能有关(图 3 E)。对七例无肉瘤样去分化区域的 TLS+ ccRCC 病例进行一致性分析得到了相似的结果,其中五种基因(IGHA1、IGHG1、IGHG3、IGKC和IGLC1)在 sRCC 和 ccRCC 衍生的 TLS 中保守。H&E 染色显示,超过 500 μm 的高度有核淋巴聚集体(提示成熟 TLS)位于 TLS+感兴趣区域 (ROI) 之下(图 3 F)。TLS特征的表达以及与 TLS 成熟相关的多个基因在 TLS 位点共定位,包括 T 细胞、B 细胞、浆细胞和滤泡树突状细胞的标志物(图 3 G)。
最近的报告将 TLS 与 RCC 的 ICB 反应联系起来;因此,他们在 IMmotion151 试验中评估了 TLS 相关基因表达的生物标志物潜力。根据中位TLS Imprint 标记表达将病例分为 TLS-high和TLS-low。在 sRCC 亚组中,TLS-high可预测对 ICB 的反应:与 TLS-low患者和接受舒尼替尼治疗的 TLS -high的患者相比(图3H),使用阿特珠单抗/贝伐单抗治疗的 TLS -high患者的无进展生存期 (PFS) 延长(图3 I)。在分析客观缓解率 (ORR)时观察到了类似的结果(图 3 J)。然而,这些趋势并不适用于 IMmotion151 中的 ccRCC 人群(图3K-M)。
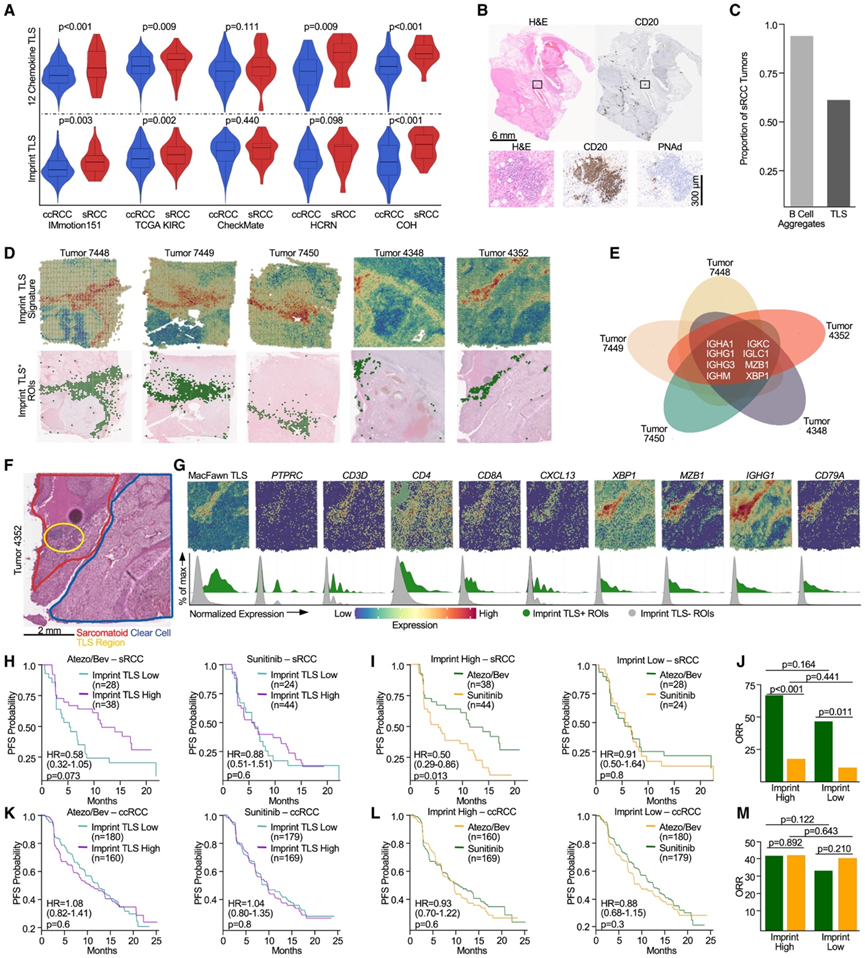
图3. sRCC 中的三级淋巴结构。
(A) 不同队列中 sRCC 和 ccRCC 病例的 TLS 特征 ssGSEA 值。(B) 连续 sRCC 肿瘤切片上 CD20 和 PNAd 的代表性 H&E 和免疫组织化学染色。(C) 具有 B 细胞聚集体和 TLS 的 sRCC 肿瘤比例。(D) 定义为 TLS+ 的五个 sRCC 肿瘤中的Imprint TLS 特征表达和 Imprint TLS +区域。(E) 通过空间转录组学分析所有五例 TLS + sRCC 病例中 TLS 中富集的基因。(F) sRCC 肿瘤切片的 H&E 染色,包含邻近的肉瘤样(红色)和透明细胞(蓝色)区域。(G) TLS 相关特征和肿瘤基因的TLS+和 TLS−区域之间的空间映射(上)和表达直方图(下)。(H-I) 生存分析。(J) sRCC 病例中不同 TLS 状态和治疗组的客观缓解率。(K-L) 生存分析。(M) IMmotion151 中 ccRCC 病例按 TLS 状态和治疗组划分的客观缓解率。
04
体液免疫是 sRCC 抗肿瘤反应的功能组成部分
CXCL13 通过 CXCR5 在淋巴组织(包括 TLS)中发挥 B 细胞趋化因子的作用。scRNA-seq 数据的相互作用分析显示,与 ccRCC 相比,sRCC 中CXCL13-CXCR5 的增强预示着 CD8+ T 细胞与 B 细胞之间的通讯(图 4 A)。因此,sRCC 肿瘤中表达CXCL13的 T 细胞和 TLS的富集促使他们探究体液免疫的作用。
他们对 TCGA KIPAN、COH 和 CheckMate 队列进行了基因集富集分析 (GSEA),拥有这些队列的完整差异表达基因数据。与 B 细胞信号转导和免疫球蛋白生成相关的通路在 sRCC 中富集(图 4 B)。对 IMmotion151 队列的数据进行反卷积分析,还观察到 sRCC 和类别转换记忆 B 细胞中总 B 淋巴细胞的富集增加(图 4 C),这表明 sRCC 中的 B 细胞活化和抗体产生潜力增强。
对 COH 队列进行了适应性免疫组库重建;在 sRCC 中观察到每个肿瘤的独特 IGH 和 TCRB 克隆型均显著增加(图 4D),但是患者之间的克隆型重叠很小。独特 IGH 克隆的数量与 TLS 印记评分相关(图4E),sRCC 样本显示出比 ccRCC 样本更高的相关性。当按中位 IGH 克隆型计数和 TLS 印记评分值分层时,69% 的 sRCC 病例归类为 IGH 克隆型highTLShigh,而 ccRCC 病例为 38%。每个患者水平的适应性淋巴细胞克隆性揭示了 RCC 中 TLS 印记评分和 B 细胞克隆型丰度之间的显著相关性(图 4 F)。然而,在评估治疗结果时,无论治疗类别如何,B 细胞克隆型丰度与一线治疗的客观疗效之间均无显著关联(图 4 F)。对 T 细胞受体组进行了类似的分析,再次表明 Imprint 评分与独特的 TCRB 克隆之间存在相关性,且 sRCC 中的 TCRB 克隆型丰度增加,但与治疗疗效无关。
从scRNA-seq数据集中提取了B淋巴细胞(3769个细胞),可视化了两个主要亚群中的六个细胞群:以表达CD19和MS4A1(编码CD20)为特征的B细胞,以及以免疫球蛋白编码基因表达为特征的抗体表达细胞(图4G-H)。sRCC B淋巴细胞在免疫球蛋白基因表达方面显著富集(图4I)。sRCC中抗体表达细胞的丰度增加了近10倍,占sRCC中所有B淋巴细胞的39.2%,而ccRCC中该比例为4.4%(图4J)。抗体产生B细胞的比例也与scRNA-seq检测出的表达CXCL13的CD8+ T细胞的丰度相关,sRCC病例更有可能表现出两种细胞群水平的升高,这表明适应性免疫群之间存在相互作用,这些细胞群可能通过TLS进行整合(图4K)。此外,与ccRCC相比,sRCC肿瘤中CD38+ B细胞(抗体产生能力的替代指标)的丰度显著富集,流式细胞术检测的B细胞中CD38的中位荧光强度(MFI)也显著富集(图4L-M)。
为了确定这种增加的 B 细胞活化和免疫球蛋白产生是否是 sRCC 中抗肿瘤免疫反应的功能特征,他们研究了 sRCC 和 ccRCC 患者的 IgG 抗体对癌细胞的反应性。将肿瘤悬浮液与未接受过治疗的患者匹配血清一起孵育。通过比较 CD3+ T 细胞、CD14/15+髓系细胞和 CD45− CD31− CD90 −癌细胞之间的 IgG 染色来评估血清来源的 IgG 对肿瘤克隆的特异性。在癌细胞中观察到 IgG 结合增加(通过 MFI 测量),而与 T 细胞和髓系细胞的反应性最小(图 4 N)。sRCC中 IgG 阳性的癌细胞比例明显高于ccRCC,与 sRCC 癌细胞之间的 IgG 结合增加相平行(图 4 O-P)。这些结果揭示了体液免疫作为 sRCC 中功能富集的效应过程。
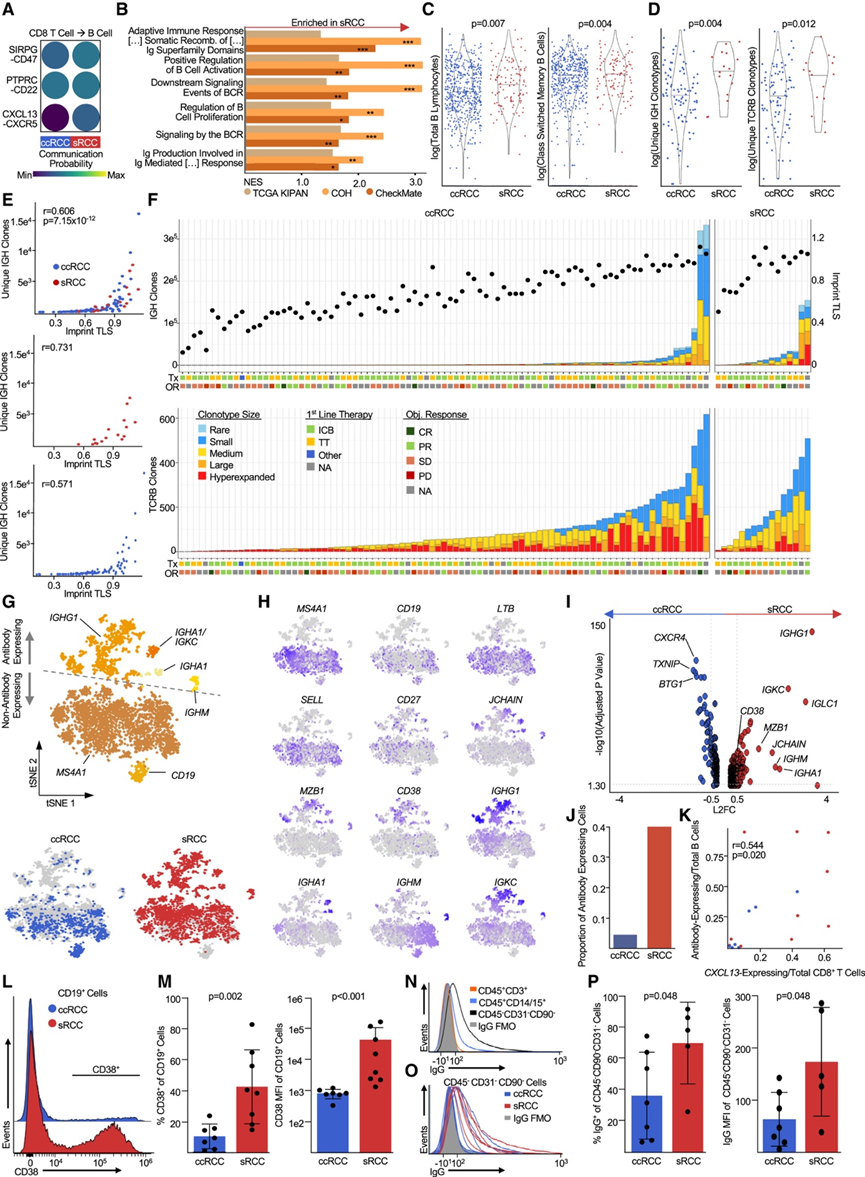
图4. sRCC中的体液免疫活性。
(A) 从 scRNA-seq 预测 T 细胞和 B 细胞群体之间的细胞通讯信号传导。(B) 通过基因集富集分析,筛选出 TCGA KIPAN、CheckMate 和 COH 队列中 sRCC 富集的 B 淋巴细胞通路。(C) 通过 xCell 免疫反卷积计算 IMmotion151 队列中的 B 细胞丰度。(D) 通过 TRUST4 组库重建,显示 COH 中 sRCC 和 ccRCC 患者个体独特的 B 细胞受体和 T 细胞受体克隆型。(E) BCR 克隆型丰度和每个样本的 TLS Imprint 得分的散点图(上),COH 中 sRCC(中)和 ccRCC(下)之间的分离。(F) 上图:COH 中每位患者的 BCR 克隆型计数及相应的 TLS Imprint 评分。下图:COH 中每位患者的 TCR 克隆型计数。(G) 通过 scRNA-seq 分析 B 淋巴细胞的 tSNE 减少情况。(H) B 淋巴细胞相关基因的特征映射到 scRNA-seq tSNE 减少。(I) 通过 scRNA-seq 对 ccRCC 和 sRCC 衍生的 B 淋巴细胞进行差异表达分析。(J) 通过 scRNA-seq 测定表达抗体的 B 淋巴细胞(在 G 中定义)相对于总 B 淋巴细胞的丰度。(K) scRNA-seq分析显示,每位患者表达抗体的B淋巴细胞相对比例和表达CXCL13的CD8+ T细胞相对比例的散点图。(L) 通过全光谱流式细胞分析的CD19+ B 细胞中的 CD38 荧光。(M) CD19+细胞群中 CD38 的表达情况。(N) T 细胞(CD45+ CD3 +)、髓系(CD45+ CD14/15 +)和肿瘤细胞(CD45−CD31− CD90−)群体之间的 IgG 结合。(O) sRCC 和 ccRCC 样本中肿瘤细胞之间的 IgG 结合。(P) IgG与肿瘤细胞群结合的定量分析。
05
髓系细胞群支持 sRCC 微环境中的适应性免疫过程
从 scRNA-seq 数据集中提取髓系细胞群,并重新聚类为 11 个聚类 (图 5 A-B),其中 4 个在 sRCC 样本中富集,分别以CCL20、S100A9、FTH1和SELENOP的表达为特征(图 5 C)。在SELENOP聚类中,SLC40A1也是差异富集最多的基因之一。FTH1和SLC40A1分别编码铁蛋白重链 1 和铁转运蛋白,它们是铁储存和运输的关键调节因子。此外,编码铁蛋白轻链的FTL——另一个铁储存基因——是 sRCC 衍生的髓系细胞群中最显著富集的基因之一 (图 5 D)。两聚类在 ccRCC 中富集,由CCL3和FCER1A的表达定义。
进行细胞通讯分析,以探究髓系细胞群对免疫过程的影响。预测巨噬细胞上的 CD86 与 CD4+ T 细胞上的 CD28 之间的共刺激相互作用在 sRCC 中相对于 ccRCC 中富集,CD86 与 CTLA-4 之间的抑制性相互作用亦是如此,这表明巨噬细胞支持的 T 细胞活化和耗竭在 sRCC 中发挥作用(图5E-F)。在细胞群亚群中,在调节性 CD4 +和PMCH耗竭的 CD8+ T 细胞亚群中,CD86-CD28/CTLA-4 信号在 sRCC 中增强。
鉴于 sRCC 中体液免疫监视增强,他们探讨了髓系细胞群在促进 B 细胞介导的免疫反应中的作用。预测 sRCC 中的髓系细胞群通过 APRIL 和 BAFF 信号网络支持 B 细胞成熟过程,与 ccRCC 相比信息流更大,表明 B 淋巴细胞在 sRCC 中发挥作用。此外,体液免疫依赖于吞噬效应分子来清除抗体结合细胞。由FCGR3A编码的 CD16是 NK 和单核细胞谱系抗体依赖性细胞毒作用 (ADCC) 的最终介质。先前在 RCC 中的研究已发现 IgG 结合的肿瘤细胞与巨噬细胞浸润之间存在相关性,但与 NK 细胞存在无关。细胞通讯预测的过度表达分析显示 sRCC 中的吞噬作用和髓系激活程序上调(图 5 G)。scRNA-seq结果显示,FCGR3A在 sRCC 髓系群体中的表达高于 ccRCC(图 5 D)。转录组学分析显示, FCGR3A在 Javelin101、TCGA KIPAN、CheckMate 和 COH 队列中的 sRCC 中也富集(图 5H)。然而, FCGR3A 的表达与 IMmotion151 中的 ICB 反应性无关。FCGR 依赖性吞噬基因集在 sRCC 中增强(图 5I),空间转录组学分析显示,吞噬程序在肉瘤样区域中富集,而非成对的透明细胞区室(图5J)。
为了检测血清来源的 IgG 对吞噬功能的影响,用 CellTrace Violet (CTV) 标记 RCC 肿瘤悬浮液中的CD45 −细胞,然后在有或没有血清的情况下与 CD45 +级分共培养(图 5K)。通过免疫群体中的 CTV 水平来测量吞噬作用,无论是否暴露于血清,T 细胞的摄取量都很小,而血清处理后,髓系细胞的 CTV 显著富集,CD16+髓系细胞中也观察到类似的趋势(图 5L)。这些发现表明 sRCC 中的髓系群体具有 ADCC 所必需的吞噬能力,从而验证体液免疫活性。
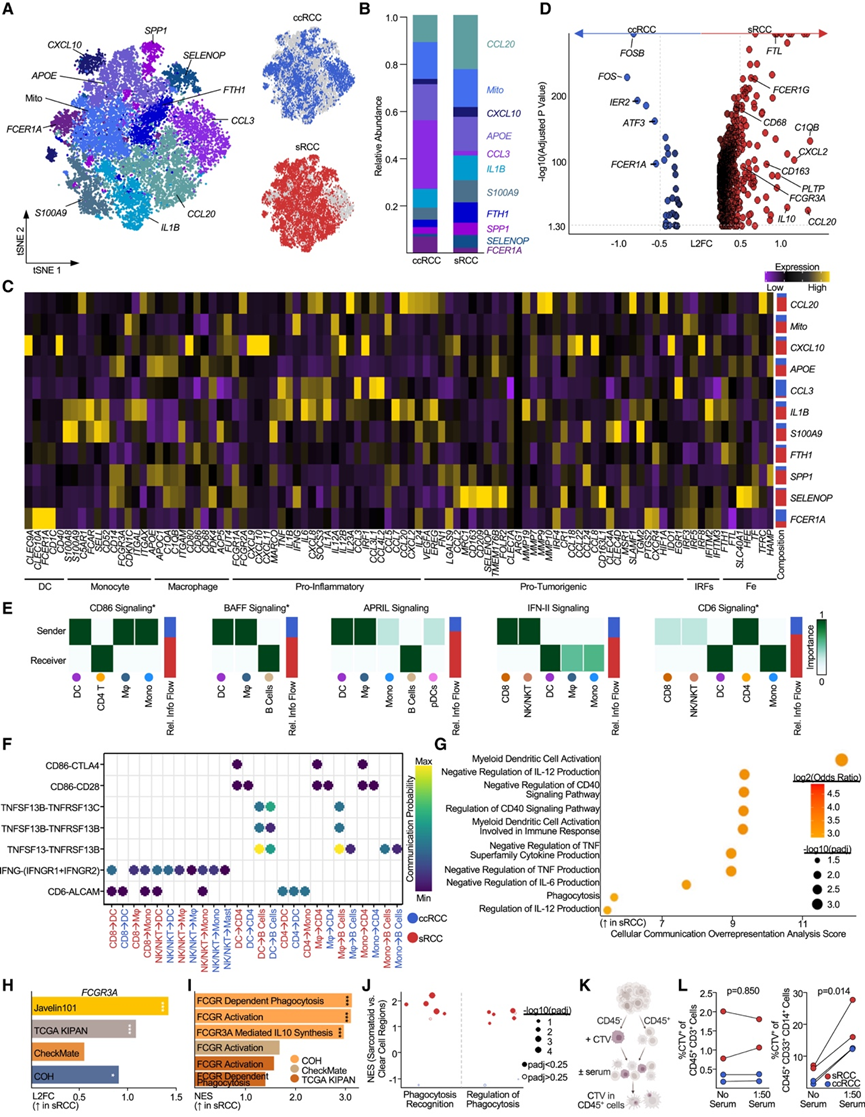
图5. sRCC 中的髓系细胞群。
(A) tSNE可视化。(B) 聚类的相对丰度。(C) 按功能和/或表型分类的髓系相关基因热图。(D) sRCC 和 ccRCC 衍生的髓系细胞之间的差异表达基因。(E) sRCC中淋巴细胞和髓系细胞群之间的细胞内信号网络。(F) sRCC 和 ccRCC 中免疫群体之间的配体-受体相互作用。(G) 通过 scDiffComm 进行细胞通讯过度表达分析。(H) sRCC 相对于上皮样 RCC 中FCGR3A的差异表达。(I) 选择在sRCC样本中富集的FCGR通路。 (J) Visium 空间转录组学分析了肉瘤样(红色)与透明细胞(蓝色)区域中吞噬基因集表达的富集情况。(K) 进行吞噬作用试验的示意图。(L) 在有或无血清条件下孵育后,T 细胞和髓系细胞对 CTV 的摄取。
06
肿瘤克隆分析揭示了 sRCC 中铁程序和假定新抗原的富集
通过空间转录组学将 IMmotion150/151 分子亚群映射到肿瘤切片,以表征异质性 sRCC TME 中病理上不同的肉瘤样与透明细胞区域的特征。与先前在 sRCC 中增强的效应 T 细胞、髓系炎症、补体和细胞周期程序的转录组学发现一致,这些炎症和增殖途径在肉瘤样去分化区域中富集,而脂肪酸氧化 AMP 激酶特征在透明细胞区室中富集(图 6 A-B)。先前描述为在 sRCC 中富集的标志通路也持续富集在肉瘤样区域(图 6 C) ,适应性免疫活动的基因本体特征(特别是体液免疫和抗原加工/呈递)以及来自scRNA-seq 队列的耗竭 CD8+ T 细胞基因集也存在(图 6 D)。
由于肉瘤样特征是由恶性细胞的形态学变化定义的,他们在 scRNA-seq 数据集中研究了癌细胞。在肿瘤克隆分离和降维之后,观察到 sRCC 衍生克隆和 ccRCC 衍生克隆之间的明显分离(图 6 E)。按病例汇总基因表达计数,进行差异表达分析,结果显示 sRCC 克隆中 20 个基因显著上调,包括SEMA3C、DCBLD2和CD44(图 6 F)。Hallmark GSEA 显示 EMT 信号转导富集(图 6 G),这与先前将肉瘤样转化与 EMT 相关联的发现一致。通过 scRNA-seq 分析在 sRCC 克隆中富集的20 个基因的表达在通过空间转录组学分析的肿瘤肉瘤样区域中持续增加(图 6 H)。
CD44 此前已证明与 RCC 中的 EMT 过程相关,并且是过渡金属(包括铁和铜)内吞进入肿瘤细胞的非典型介质。scRNA-seq 显示CD44在sRCC癌细胞中显著富集,而批量转录组学显示 CD44 在 sRCC 中整体富集(图6 I)。与之前强调的 sRCC 髓系群体中CD44表达增强和铁调节因子上调一致,来自 ccRCC 肿瘤的铁死亡相关特征在各个队列中相对于 ccRCC 在 sRCC 样本中富集(图 6 J)。空间转录组学显示,与相邻透明细胞区域相比,与过渡金属有关的基因本体集也在肉瘤样区域持续富集(图 6 K),这些数据表明 sRCC 中过渡金属相关活性增加。
基于hERV表达、抗hERV体液免疫应答与RCC及其他肿瘤免疫检查点阻断(ICB)敏感性间的已知关联,他们研究了hERV,通过对COH队列3179条hERV参考序列的差异表达分析,发现49个hERV结构在sRCC中较ccRCC显著富集,其中21个属于hERV-H家族。利用TCGA KIRC标准化hERV表达数据进一步比较sRCC与ccRCC,鉴定出hERV_1366、hERV_5738和hERV_6095在两组队列中均显著富集于sRCC(图6L)。这三个hERV均属HERVHF超家族,其中hERV_1366和hERV_6095为HERV-H家族成员。值得注意的是,hERV-H衍生肽段在其他肿瘤类型中可产生免疫反应性表位。他们对hERV-H包膜蛋白序列进行表位预测及主要组织相容性复合体(MHC)结合分析,鉴定出20个氨基酸的hERV-H表位与HLA-A∗02:01(作为高人群覆盖率的模型等位基因)具有强预测结合力。
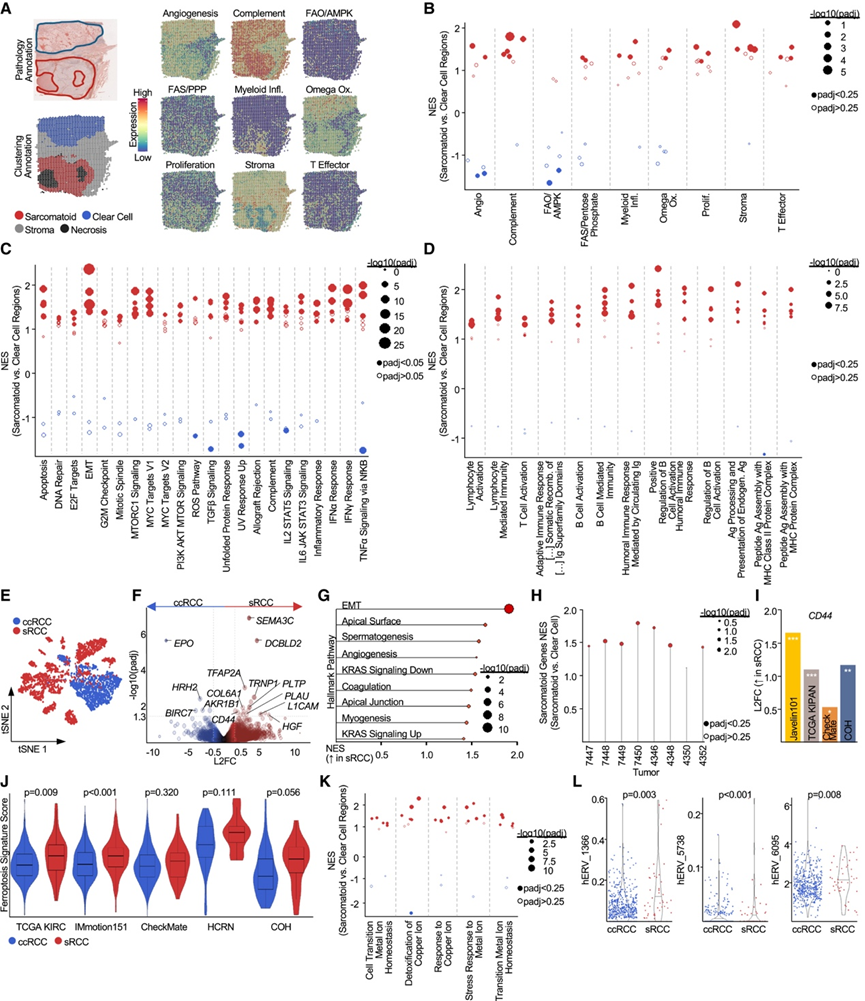
图6. sRCC 中的微环境特征和肿瘤克隆。
(A) 代表性sRCC的H&E染色,包含邻近的肉瘤样(红色)和透明细胞(蓝色)区域(左上),以及基于病理注释的空间转录组数据聚类(左下)。通过空间转录组学对IMmotion分子亚群进行映射(右)。(B) IMmotion 分子亚群表达在 Visium 空间转录组学分析的肉瘤样(红色)与透明细胞(蓝色)区域中富集。(C) 通过空间转录组学选择在肉瘤样(红色)与透明细胞(蓝色)区域中富集的 Hallmark 通路表达。(D) 通过空间转录组学分析,基因本体适应性免疫通路表达在肿瘤的肉瘤样(红色)与透明细胞(蓝色)区域中富集。(E) tSNE可视化。(F) sRCC 和 ccRCC 衍生的癌细胞之间的假性差异表达基因。(G) 选择在 sRCC 肿瘤克隆中富集的 Hallmark 通路。(H) 通过空间转录组学分析,肉瘤样区域与匹配的透明细胞区域中肉瘤样基因的富集。(I) sRCC 相对于上皮样 RCC 的CD44差异表达。(J) 不同队列的铁死亡特征ssGSEA值。(K) 通过空间转录组学分析肉瘤样(红色)与透明细胞(蓝色)区域中的基因本体过渡金属通路表达。(L) TCGA KIRC 中 hERV_1366、hERV_5738 和 hERV_6095 的标准化表达。
07
来自 sRCC 肿瘤克隆的转录特征对转移性 RCC 具有负面预后作用
他们进一步构建了一种转录组特征(Genomic Dedifferentiation Signature,GDS),用于鉴定具有sRCC高侵袭性-免疫应答表型的RCC肿瘤(无需病理学肉瘤样特征支持)。通过整合scRNA-seq鉴定的sRCC肿瘤克隆差异富集基因,并对比Javelin101、CheckMate和TCGA KIPAN中sRCC与上皮样RCC的差异表达数据,最终筛选出10个在scRNA-seq和转录组层面均一致富集于sRCC的基因(CD44、COL6A1、DCBLD2、GFPT2、L1CAM、PLAU、PLTP、SEMA3C、TFAP2A和TRNP1)。该特征在病理标注的肉瘤样区域中显著富集(图 7 A-B)。
在 TCGA KIRC 中,sRCC 患者的 GDS 评分较高(图 7 C),核级 4 级疾病(所有 sRCC 病例均归为此类)、转移性疾病和 IV 期疾病患者的 GDS 评分也较高(图 7 D)。通过总生存期 (OS) 和无病生存期 (DFS) 分析探究 GDS 的预后意义,分析采用中位数将病例分为 GDS 高组和 GDS 低组,对识别 sRCC 病例的灵敏度为 87%。具有 GDS 高特征的患者的 OS 和 DFS 明显较差(图 7 E)。此外,较高的 GDS 评分预示着 TCGA KIRC 内所有临床分期的结果均较差。
为了评估GDS对免疫检查点抑制剂(ICB)疗效的预测价值,他们分析了未参与特征构建的IMmotion151数据集。GDS评分在sRCC患者及PD-L1阳性病例中均显著富集(图7C)。整个IMmotion151队列中,无论接受何种治疗,GDS-high患者的无进展生存期(PFS)均缩短(图7F),印证了该特征的不良预后意义。在ICB治疗亚组中,GDS-high与GDS-low患者的PFS无显著差异(图7G),而舒尼替尼治疗的GDS-high患者较GDS-low患者PFS显著降低(图7H),这与sRCC人群相较于ccRCC的治疗反应模式一致。
与舒尼替尼相比,GDS-high患者接受阿替利珠单抗/贝伐珠单抗联合治疗可获得更长的PFS(图7I),而GDS-low患者两组治疗方案的PFS无显著差异(图7J)。经校正诊断年龄、国际转移性肾细胞癌数据库联盟风险分级和PD-L1状态的多变量Cox回归分析后,GDS-high患者的PFS差异仍然显著。基于ICB治疗的客观缓解者(OR)较无应答者具有显著更高的GDS评分,而舒尼替尼应答者较无应答者GDS评分显著更低(图7K)。比较不同GDS状态和治疗组的客观缓解率(ORR)也观察到疗效差异(图7L):GDS-high患者对阿替利珠单抗/贝伐珠单抗的ORR(44.9%)显著高于舒尼替尼(26.5%),且高于GDS-low患者对联合治疗的ORR(33.9%);相反,GDS-low患者对舒尼替尼的ORR(46.2%)优于联合治疗,且显著高于GDS-high患者对舒尼替尼的应答率。
HCRN-GU16-260 试验提供了另一组独立的接受 ICB 治疗的转移性肾细胞癌 (RCC) 患者。sRCC 患者的 GDS 评分增高(图 7 C),且 GDS-high与 OS 结果恶化相关,但是差异不显著(图 7 M)。比较抗 PD-1 纳武单抗 (nivolumab) 的疗效时,GDS-high患者的 PFS 延长于 GDS-low患者(图 7 N)。与 IMmotion151 类似,在对纳武单抗获得客观缓解的患者中,GDS 评分显著增高(图 7 O),且 GDS-high患者的 ORR 显著高于 GDS-low患者(图 7 P)。在七例对纳武单抗获得完全缓解的患者中,六例归类为 GDS-high患者。除了 RCC 患者外,GDS 评分在获得 nivolumab 治疗 OR 的黑色素瘤患者中也较高(图 7 G),与 GDS-low的患者相比,GDS-high的患者 PFS和 ORR改善。
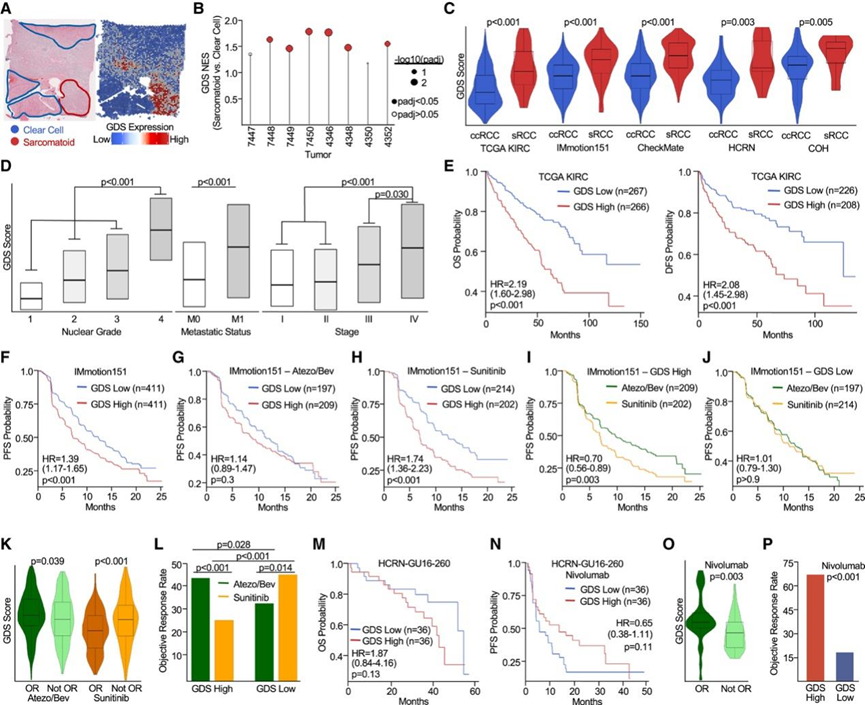
图7. 基因组去分化特征作为 RCC 的生物标志物。
(A) 通过空间转录组学将 GDS 表达映射到肿瘤区域。(B) 病理注释的肉瘤样区域与空间转录组学分析的匹配透明细胞区域中 GDS 的富集。(C) 不同队列的GDS ssGSEA值。(D) TCGA KIRC 中不同核级别、转移状态和肿瘤分期的 GDS 值。(E) GDS 高分患者与 GDS 低分患者的总生存期和无病生存期。(F-J) 无进展生存期分析。(K) 阿替利珠单抗/贝伐单抗组与舒尼替尼组客观缓解状态之间的GDS值。(L) 不同GDS状态和治疗组的客观缓解率。(M-N)生存分析。(O) Nivolumab 客观缓解状态之间的 GDS 评分。(P) 不同GDS状态下nivolumab的客观缓解率。
+ + + + + + + + + + +
结 论
本研究对人类 sRCC 肿瘤进行了单细胞转录组分析,并与ccRCC 数据集进行了比较,并在超过 3000 个 RCC 肿瘤的转录组数据集上进行了空间验证,利用以下正交方法描述了 sRCC 中强大的免疫网络:sRCC 中的肿瘤浸润 T 细胞的激活程度更高,随后发生耗竭,同时富集CXCL13表达。同时,三级淋巴结构在 sRCC 中广泛存在,与体液免疫活性的功能性富集相一致。肿瘤克隆分析显示 sRCC 中铁相关程序增多,这表明存在潜在的脆弱性。此外,本研究利用 sRCC 的生物学特性来获得基因组去分化特征 (GDS),虽然其具有负面预后,但可以识别出最有可能在各个队列和肿瘤类型中受益于 ICB 的患者。
+ + + + +



 English
English


