文献解读|Nat Med(50):血浆蛋白质组学将大脑和免疫系统衰老与健康寿命和长寿联系起来
✦ +
+
论文ID
原名:Plasma proteomics links brain and immune system aging with healthspan and longevity
译名:血浆蛋白质组学将大脑和免疫系统衰老与健康寿命和长寿联系起来
期刊:Nature Medicine
影响因子:50
发表时间:2025.07.09
DOI号:10.1038/s41591-025-03798-1
背 景
衰老会导致器官功能障碍、慢性疾病甚至死亡。虽然热量限制、年轻血浆和雷帕霉素等干预措施能够延长模型生物的健康寿命,并可能延缓衰老,但由于分子层面的理解和评估工具有限,这些干预措施在人体中的疗效尚不明确。目前需要找到与健康和疾病相关的人类生物年龄的分子生物标记物。特定器官的血浆蛋白可以估算器官年龄和死亡率,但其对环境因素的敏感性以及预测器官疾病发生和死亡率的稳健性仍不清楚。
实验设计
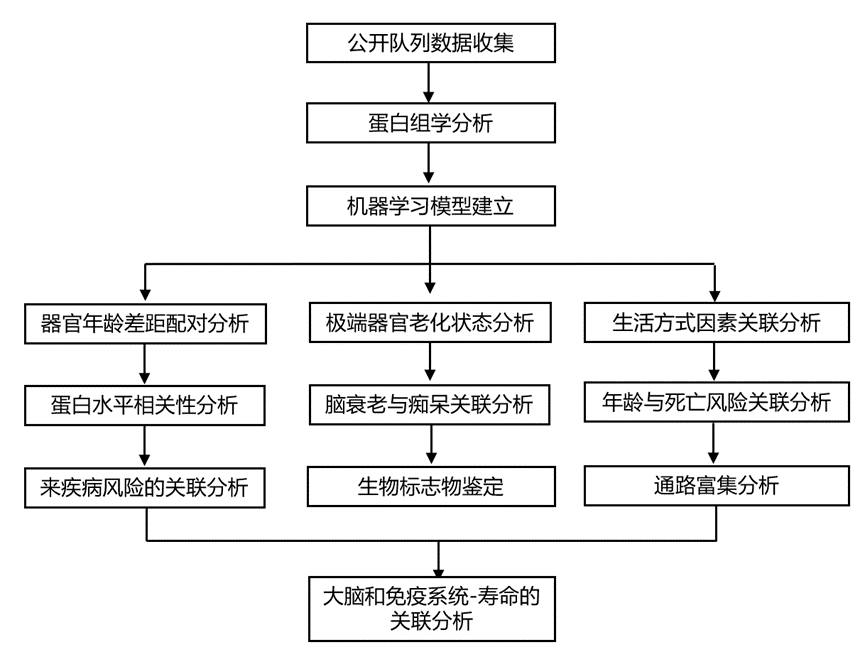
结 果
01
英国血浆蛋白衍生器官年龄分析
为了从血浆蛋白质组中估算器官特定的生物学年龄,研究团队确定了可能来自特定器官的血浆蛋白,他们训练了一个机器学习模型,根据已确定的器官富集蛋白水平预测实际年龄,然后根据每个人的预测年龄(与相同实际年龄的个体相比的相对预测年龄)分析年龄差距(图1a),年龄差距可以衡量与同龄人相比的相对生物学年龄。
他们对 11 个主要器官(包括脂肪组织、动脉、大脑、心脏、免疫组织、肠道、肾脏、肝脏、肺、肌肉和胰腺)分别执行了这三个步骤。由于英国生物样本库 (UKB) 中提供了与年龄相关的表型数据,因此他们将分析重点放在这些器官上。为了将器官年龄差距与器官不可知的生物年龄测量值进行比较,他们还从针对非器官特异性蛋白质(占所有蛋白质的 80%)训练的“有机体”衰老模型和针对 Olink 检测中的所有蛋白质训练的“传统”衰老模型中得出了年龄差距。传统衰老模型中的顶级蛋白质与之前基于 UKB 数据集开发的蛋白质组学衰老模型重叠。
来自 22 个血浆采集中心中的 11 个的数据用于模型训练,其余 11 个用于测试(图1a)。模型性能在训练和测试中心之间高度稳定。年龄差距按衰老模型进行z分数计算,以便在下游分析中直接比较器官(图1a)。他们观察到器官年龄差距之间存在一些性别差异,男性的肾脏、免疫系统和肠道较老,而女性的脂肪组织、动脉和心脏较老。
如果器官以不同的速度衰老,那么一个器官的年龄差距应该与另一个器官的年龄差距无关。年龄差距之间的成对相关性表明,器官年龄差距仅有弱相关性(图1b),证实了先前的研究。器官年龄差距不同于传统的年龄差距,由于大多数蛋白质重叠,后者与生物体年龄差距密切相关。生物体 、大脑和动脉年龄解释了 97% 的传统年龄差异,其中生物体年龄贡献了 74%(图1c)。
他们通过鉴定任何器官的年龄差距高于或低于人口平均值 1.5 个标准差的个体,在 UKB 中寻找极端衰老者。不仅发现了器官衰老快(z年龄差距≥1.5)的个体,而且发现了器官衰老慢的个体(图1d)。研究之间的差异可能源于不同的样本量、蛋白质组学平台和阈值。他们还鉴定出具有两个或两个以上极端器官年龄差距的多器官衰老者。14% 的样本不明确,既有正极端年龄差距,也有负极端年龄差距,其余样本的 27% 定义为正常衰老。多器官衰老者明显比正常和单器官衰老者年龄大,这表明衰老的器官会随着时间的推移而积累。
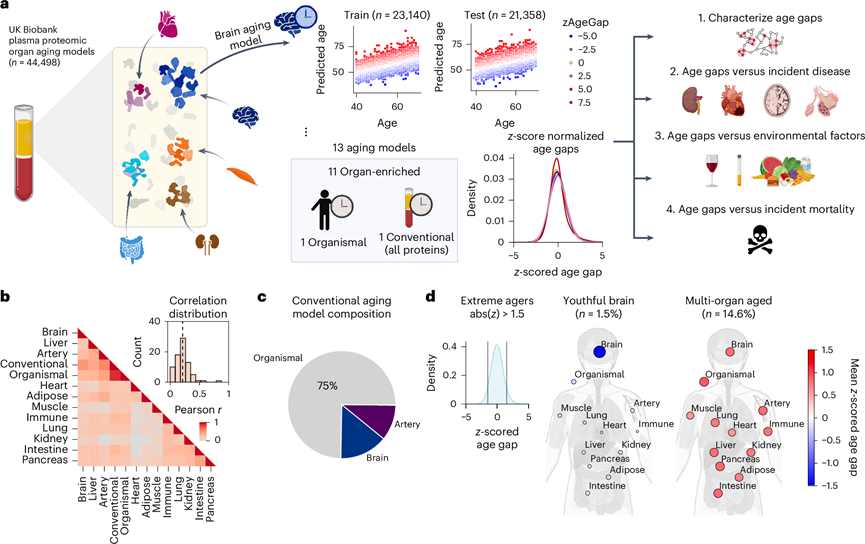
图1. UKB 中的血浆蛋白衍生器官年龄估计。
(a) 研究设计旨在利用英国国立卫生研究院(UKB)的血浆蛋白质组学数据估算器官特异性生物年龄。(b) 所有样本中器官年龄差距的相关性。(c) 使用 LASSO 回归模型根据器官年龄和生物体年龄预测常规年龄。(d) 极端衰老定义为至少一个年龄差距增加或减少 1.5 个标准差。显示了极年轻大脑衰老和多器官加速衰老的平均器官年龄差距。
02
器官年龄估计可预测未来与年龄相关的疾病
为了使生物年龄估计值具有参考价值,它必须与器官或个体的生理状态紧密相关,从而与年龄相关的健康和疾病结果紧密相关。因此,他们试图确定器官年龄差距是否可以预测其各自器官未来的疾病。他们使用Cox比例风险回归检验了所有13个z得分年龄差距与15种年龄相关疾病(2至17年随访)之间的关联,同时调整了年龄和性别。在对多重假设检验进行Benjamini-Hochberg校正后,他们在195个检验中发现了176个显著正相关和4个显著负相关(图S5)。
器官衰老与疾病的广泛显著关联(176/195)凸显了衰老的系统性特征。为解析这些系统性影响并识别独立于其他器官衰老的器官年龄-疾病关联,他们采用包含所有器官年龄差作为协变量的多变量Cox模型进行分析。在控制其他器官衰老因素后,发现器官年龄差与疾病的关联呈现更强的器官特异性(图2a)。例如:心力衰竭事件虽与全部13项基线年龄差存在个体关联,但仅与其中7项年龄差保持独立关联。然而,他们发现血管年轻化与多种疾病风险升高相关(包括2型糖尿病、慢性阻塞性肺病、慢性肝病等),这揭示了衰老与疾病关联的复杂性。值得注意的是,阿尔茨海默病无论在单独分析还是控制其他器官因素后,均显示出与大脑衰老的高度特异性关联(图2b)。
他们还研究了极端器官老化状态与疾病风险之间的关联,这种关联与年龄、性别和其他极端器官无关(图S5b)。由于大多数疾病的样本量有限,5-7 岁和 8 岁以上的多器官老化者未纳入研究。拥有 2-4 个老化器官的个体,其每种疾病的风险显著增加。拥有极度老化的大脑、心脏、肾脏或肺的个体患病风险也普遍增加。相反,拥有 2-4 个极度年轻器官的个体可以免受多种疾病的侵害,包括慢性肾病、骨关节炎和 COPD。在年轻的器官概况中,大脑、免疫系统和肠道对至少四种疾病具有名义上的保护作用。年轻的大脑对阿尔茨海默病和其他痴呆症具有特别的保护作用,年轻的肠道对糖尿病具有特别的保护作用(图S5b)。
鉴于大脑与阿尔茨海默病之间的独特而密切的联系,他们进一步研究了所有大脑极度年轻或衰老的个体(无论单器官还是多器官衰老状态),以及他们与阿尔茨海默病风险的关联,同时控制年龄、性别以及APOE基因型(阿尔茨海默病最强的遗传风险因素)。有趣的是,极度大脑衰老使阿尔茨海默病风险增加 3.1 倍,而极度大脑年轻使阿尔茨海默病风险降低 74%,与年龄、性别、APOE4和APOE2无关(图2c-d)。因此,与大脑年轻的人相比,大脑老化的人罹患阿尔茨海默病的风险高出 13.5 倍。值得注意的是,当将大脑年龄与APOE基因型的影响进行比较时,大脑老化的风险与携带一个APOE4拷贝的风险相似,而大脑年轻的人则提供的保护与携带两个APOE2拷贝的风险相似(图2c)。大脑年龄与APOE基因型的相关性非常弱(图2e)。在 17 年的随访期间,2628 名大脑老化的人中有 120 人(4.56%)患上了阿尔茨海默病,而 1998 名大脑年轻的人中只有 7 人(0.35%)患上了这种疾病。
鉴于脑衰老与痴呆症之间关联的特异性,他们基于随访的MRI数据(图S5c),探究器官年龄差距是否与脑容量相关。基线随访时的脑年龄差距与第2次随访时(平均约9年后)脑室容量增加和皮质区域容量减少存在独特的相关性。
既往研究已采用脑部MRI数据推演生物学脑年龄。为比较本研究的血浆蛋白质组脑年龄评估与MRI脑年龄评估的差异,他们基于45574名受试者的479项FreeSurfer脑容积表型数据建立了MRI脑衰老模型。与既往报道一致,MRI脑年龄与实际年龄显著相关(图S5d)。MRI脑年龄差每增加1个标准差,未来阿尔茨海默病风险升高3.2倍,证实其与功能性脑衰老密切关联。但值得注意的是,MRI与血浆评估的脑年龄差仅呈弱相关性(图2f),提示二者捕获了脑衰老的不同组分。虽然这种弱相关性部分源于MRI与血浆样本采集存在约9年的时间间隔,但最新研究表明仅血浆中的短蛋白聚糖(BCAN)和胶质纤维酸性蛋白(GFAP)——而非本研究发现的其他脑衰老相关蛋白——与MRI脑年龄相关,暗示生物学差异也是导致相关性弱的原因。他们推测MRI脑年龄主要反映整体细胞丢失,而血浆脑年龄既能捕捉部分容积变化,也能反映细胞状态及相互作用相关的分子改变。
他们还评估了器官年龄差距与疾病进展的关联性,方法是将年龄差距与确诊年数进行回归分析,研究对象为在抽血前就已确诊的个体。许多器官的年龄差距在整个慢性肾脏病进展过程中都在扩大(图S5e)。有趣的是,大脑年龄差距与痴呆症进展无关(图S5f),这表明大脑年龄差距反映了可能导致个体易患痴呆症的年龄相关变化,但并未反映疾病发作后发生的变化。
接下来,为深入探究器官衰老机制,他们进一步分析了衰老模型蛋白及其权重。基于全部基线样本与仅随机选择86%基线样本训练的衰老模型及其蛋白权重基本一致。在大脑衰老模型中,权重最高的蛋白是神经丝轻链(NEFL)(图2h),其水平随年龄增长而升高,是轴突变性的临床生物标志物,常用于阿尔茨海默病临床试验,近期还批准作为治疗超氧化物歧化酶1肌萎缩侧索硬化症(SOD1 ALS)临床试验的替代终点。本研究的数据表明,该蛋白与其他蛋白联用,或可作为普通人群脑衰老及痴呆风险的可行替代指标。其他高权重脑衰老蛋白包括:随年龄增加的髓鞘少突胶质细胞蛋白(MOG,髓鞘外表面组分)和反应性星形胶质细胞标志物GFAP;以及随年龄减少的脑细胞外基质成分短蛋白聚糖(BCAN,由少突胶质前体细胞产生)和蛋白酪氨酸磷酸酶受体R型(PTPRR)(图2h)。既往研究已指出血浆NEFL、GFAP和BCAN是未来痴呆风险的预测因子。
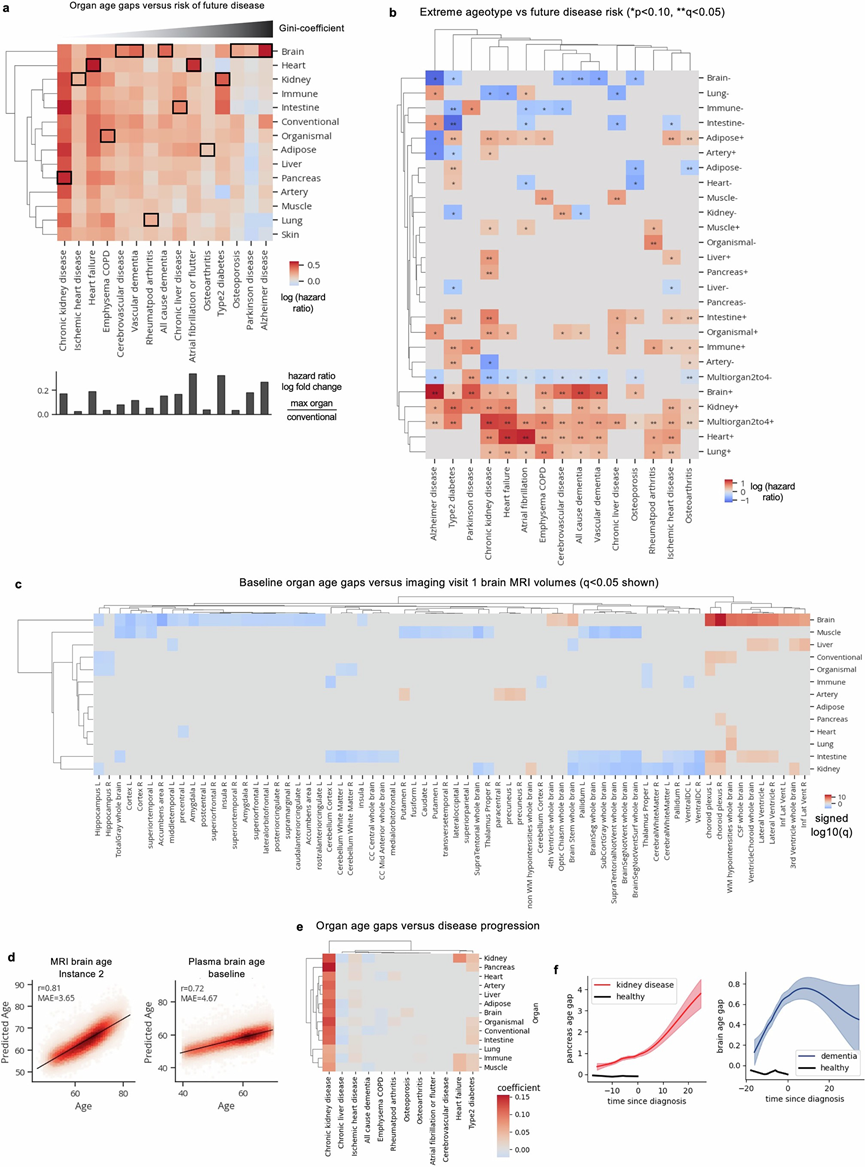
图S5. 年龄差距与疾病关联。
(a) 使用 Cox 比例风险回归分析检验年龄差距与未来患病风险之间的关联。(b) 使用 Cox 比例风险回归分析确定极端年龄者与未来患病风险之间的关联。(c) 使用线性回归确定基线器官年龄差距与实例 2 脑 MRI 体积之间的关联。(d) 来自实例 2 的 45574 名个体的基于 MRI 的大脑年龄与实际年龄(左)。来自基线的 44498 名个体的基于血浆蛋白质组学的大脑年龄与实际年龄(右)。(e-f) 使用线性回归确定器官年龄差距与疾病诊断年数之间的关联。
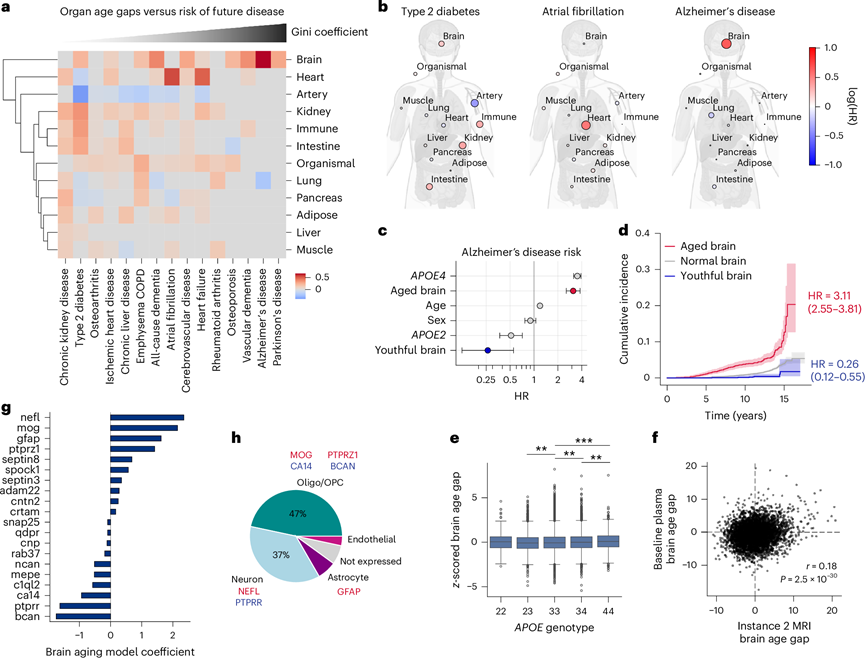
图2. 器官年龄估计预测未来与年龄相关的疾病。
(a) 使用 Cox 比例风险回归检验年龄差距与未来疾病风险之间的关联。(b) 2 型糖尿病、心房颤动和阿尔茨海默病的 logHR 值。(c) 使用 Cox 比例风险回归检验极端大脑年轻/衰老与未来阿尔茨海默病风险之间的关联。(d) 在比较大脑极度衰老的个体、大脑极度年轻化的个体和大脑年龄正常的个体时,显示阿尔茨海默病随时间的发病率累积发病率曲线和 95% 置信区间。(e) 大脑年龄差距与APOE基因型的箱线图可视化。(f) 基线时基于血浆的大脑年龄差距与实例 2(基线访问几年后)时基于 MRI 的大脑年龄差距。(g) 条形图显示脑老化模型中前20个蛋白质的系数。(h)分配给每种脑细胞类型的脑老化蛋白质的比例。
03
器官年龄与生活方式有关
他们接下来探讨了基于器官功能生理状态的生物年龄估计是否对生活方式的变化敏感,使用线性回归检验了所有 13 个z分数年龄差距与 18 种生活方式因素(即饮食、饮酒、吸烟、锻炼和失眠)和社会经济因素(即教育和汤森剥夺指数)之间的关联,并根据年龄和性别进行了相互调整。在校正了多重假设检验后,他们发现 69 个正相关和 57 个负相关显著关联。与已知的健康关联一致,吸烟、饮酒、加工肉类摄入、汤森剥夺指数和失眠与多个器官的衰老加速有关,而剧烈运动、食用油性鱼、食用家禽和高等教育与年轻的器官有关(图3a)。
他们还检测了所有 13 个z得分年龄差距与 137 种药物/补充剂消费之间的关联。经过多重假设检验校正后,发现六种产品——普力马林、布洛芬、葡萄糖胺、鱼肝油、复合维生素和维生素 C—— 与至少两种器官的年轻化显著相关(图3b)。布洛芬、葡萄糖胺、鱼肝油、复合维生素和维生素 C 产品主要与肾脏、大脑和胰腺的年轻化相关(图3b)。
Premarin 是一种结合雌激素药物,通常用于治疗绝经后症状的女性,最近有研究表明雌激素药物与降低 UKB 的死亡风险有关。因此,他们想知道雌激素药物是否可以通过预防绝经引起的器官加速老化和疾病风险来延长寿命。在 47 名接受雌激素治疗的正常、早期或过早绝经的女性中,早期绝经与大多数器官的加速老化有关(图3c),而雌激素治疗与年轻的免疫、肝脏和动脉状况相关(图3d)。
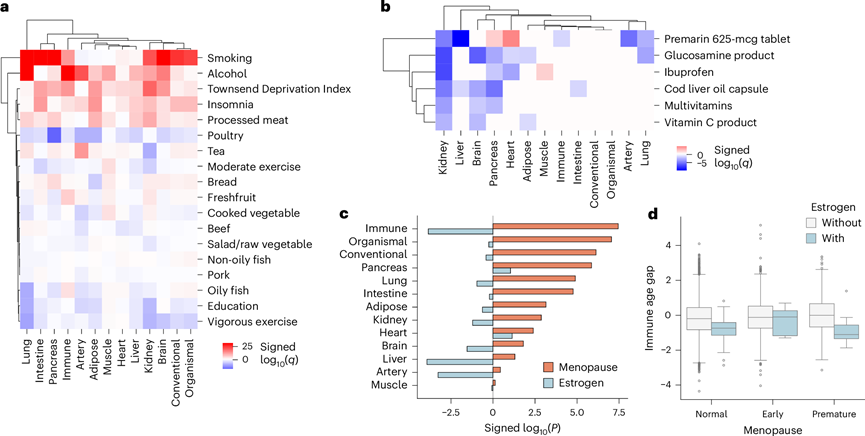
图3. 器官年龄与生活方式有关。
(a) 使用线性回归确定年龄差距与可改变的生活方式因素之间的关联。(b) 使用线性回归确定年龄差距与药物/补充剂摄入量之间的关联。(c) 使用多元线性回归来确定年龄差距与早期更年期和雌激素治疗之间的关联。(d) 按更年期状况和雌激素治疗分层的个体的免疫年龄差距箱线图可视化。
04
大脑和免疫系统年轻可预测寿命
接下来,他们试图确定器官年龄估计是否与未来死亡率相关,使用 Cox 比例风险回归检验了器官年龄差距与全因死亡风险之间的关联,并根据年龄和性别进行了 2-17 年的随访。所有器官均表现出显著关联,年龄差距每增加一个标准差,死亡风险就会增加 20-60%(图4a),这与基于 SomaScan 的器官老化模型的结果相似。这些关联经血液胱抑素 C(肾脏滤过率标志物)和 PhenoAge(一种成熟的基于血液生化/细胞计数的生物年龄估计值)调整后依然稳健,这表明器官年龄估计值提供了现有临床生物标志物无法捕捉到的独立信息。令人惊讶的是,大脑衰老具有最强的预测性(图4a),这表明大脑可能是人类寿命的中心调节器,类似于动物模型(蠕虫、苍蝇和老鼠)的发现。事实上,大脑老化的人患痴呆症以外的几种疾病的风险增加,包括慢性阻塞性肺病和心力衰竭,这与先前的研究一致,表明大脑调节全身炎症。
为了检验器官年龄估计是否提供了除胱抑素C和PhenoAge之外的额外预测能力,他们比较了包含胱抑素C、PhenoAge、器官年龄或组合的死亡风险Cox模型的一致性指数,并以年龄和性别作为协变量。器官年龄单独预测结果与组合模型相似,优于胱抑素C和PhenoAge,表明它们能够捕捉到额外的预测信息(图4b)。脑年龄、常规年龄、PhenoAge和性别是组合模型的关键预测因子(图4c)。应用 FIBA 来了解大脑和传统衰老模型蛋白质对死亡风险的贡献,突出了来自大脑的 BCAN、NEFL 和 PTPRR 以及来自传统衰老模型的细胞外发育异常蛋白 A2 受体(EDA2R,生物体蛋白)、趋化因子 CXC 基序配体 17 (CXCL17,生物体蛋白)和弹性蛋白(ELN,动脉蛋白)是重要蛋白质。
虽然每个器官年龄差距都与死亡风险相关,但他们怀疑器官老化的累积是否会日益增加其危害。因此,在校正年龄和性别后,检验了单器官极端老化者和多器官老化者(2-4个、5-7个和8个以上器官)是否比正常老化者死亡风险更高。有趣的是,拥有一个老化器官(脑、肺、肠、心脏、免疫系统、肾脏、肝脏或胰腺)会使死亡风险增加 1.5-3 倍,而拥有 2-4 个、5-7 个和 8 个以上极度老化器官则会使死亡风险分别增加 2.3 倍、4.5 倍和 8.3 倍(图4d-e)。值得注意的是,在抽血时拥有 8 个以上极度老化器官的个体中,超过 60% 在 15 年内死亡(图4d)。
然后,他们试图确定年轻的器官特征是否与长寿相关,动脉外观年轻的个体死亡风险增加,而多器官年轻的个体与正常老年人相比死亡风险没有差异(图4d)。他们发现动脉蛋白血小板反应蛋白2(THBS2),一种随年龄增长而减少但与死亡风险呈正相关的蛋白质,是动脉年龄差距与死亡风险之间非线性关联的原因。
但值得注意的是,拥有年轻大脑和免疫系统的个体死亡风险显著降低(图4d),类似于他们与疾病的独特保护关系。因此,他们评估了同时拥有年轻大脑和免疫系统的个体,发现这一群体在效应大小上受到的死亡保护最强(图4d-e),强调了拥有一个有弹性的大脑和免疫系统的益处。在 17 年间,10000 名正常老年人中有 792 人(7.92%)死亡,而拥有年轻大脑和免疫系统的 160 人中只有 6 人(3.8%)死亡。
为了探究与大脑和免疫系统相关的长寿有关的潜在机制,他们根据死亡风险 FIBA 评分对前 10 种大脑和免疫衰老模型蛋白进行了GO富集分析(图4f-g)。神经元周围网络是最富集的大脑通路(BCAN、PTPRZ1 和 NCAN),分泌颗粒是最富集的免疫系统通路。有趣的是,神经炎症是另一种富集的免疫系统通路,由金属蛋白酶 9(MMP9)(神经元周围网络组成的调节剂)以及肿瘤坏死因子受体超家族成员 1B(TNFRSF1B)和整合素 α M(ITGAM)(也称为 CD11B)组成。年轻的脑老化者BCAN和NCAN水平较高,而年轻的免疫老化者MMP9水平较低,这表明,部分由于外周炎症因子降解减少以及部分受大脑调控的慢性炎症减少,大脑细胞外基质的整体保存可能对促进长寿至关重要。总之,这些数据表明,血浆蛋白衍生的器官年龄估计值优于现有的用于死亡风险预测的衰老生物标志物,衰老器官的累积会逐渐增加死亡风险,而年轻的大脑和免疫系统是长寿的关键。
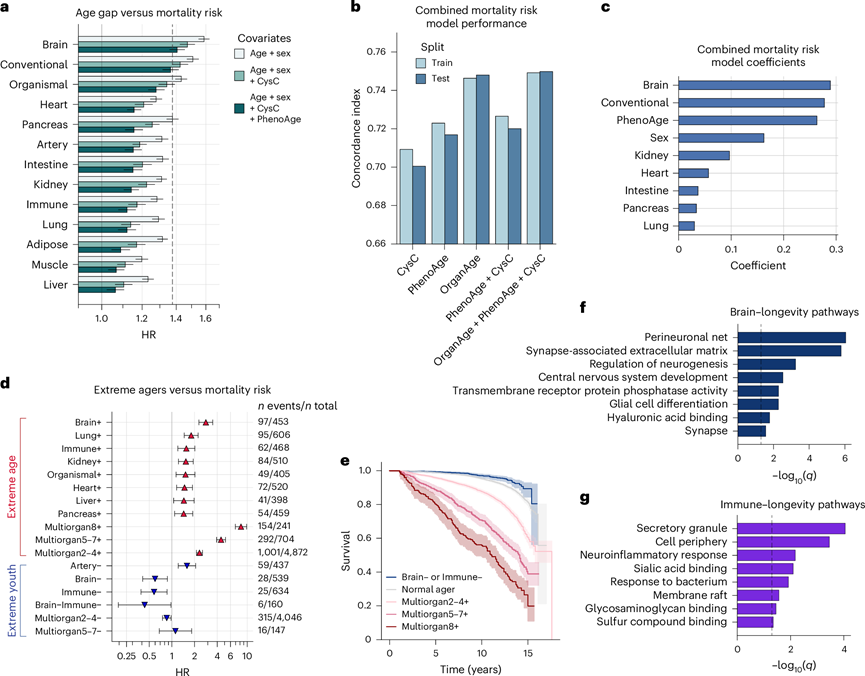
图4. 衰老器官的积累逐渐增加死亡风险,而大脑和免疫系统的年轻与长寿相关。
(a) 条形图显示 Cox 比例风险回归分析的结果,测试每个年龄差距与未来全因死亡风险之间的关联。 (b) 来自各种 LASSO 正则化 Cox 比例风险模型的一致性指数经过训练以预测死亡风险。(c) 显示了来自b的组合模型(OrganAge + PhenoAge + CysC)的模型系数。(d) 森林图显示 Cox 比例风险回归的结果,测试极端衰老状态(“+”表示衰老;“-”表示年轻)与未来全因死亡风险之间的关联。(e) Kaplan-Meier 曲线分析。(f-g)通路富集分析。
+ + + + + + + + + + +
结 论
本研究利用英国生物样本库中 44498 名个体的血浆蛋白质组学数据(2916 种蛋白质)估算了 11 个器官的生物年龄。器官年龄估算对生活方式因素和药物敏感,并且与未来(17 年随访内)一系列疾病的发病率相关,包括心力衰竭、慢性阻塞性肺病、2 型糖尿病和阿尔茨海默病。老化器官的积累逐渐增加死亡风险,而年轻的大脑和免疫系统与长寿有独特的联系。总之,这些发现支持使用血浆蛋白来监测器官健康,并指出大脑和免疫系统是长寿干预的关键目标。
+ + + + +



 English
English


