文献解读|Nat Med(50):小胶质细胞机制驱动免疫阿尔茨海默病患者的淀粉样β蛋白清除
✦ +
+
论文ID
原名:Microglial mechanisms drive amyloid-β clearance in immunized patients with Alzheimer's disease
译名:小胶质细胞机制驱动免疫阿尔茨海默病患者的淀粉样β蛋白清除
期刊:Nature Medicine
影响因子:50
发表时间:2025.03.06
DOI号:10.1038/s41591-025-03574-1
背 景
近三十年来,临床试验一直以阿尔茨海默症(AD)患者的脑内Aβ蓄积为目标。主要策略包括针对Aβ的主动和被动免疫。虽然这些策略可以减少脑内Aβ ,但也可能引发不良副作用,了解Aβ免疫的细胞机制对于改善患者预后至关重要。AN1792临床试验是首个对AD患者进行主动免疫的临床试验。该试验采用了针对合成Aβ 1-42肽的免疫。临床前研究显示出良好的前景,但由于部分患者出现与脑淀粉样血管病(CAA)相关的无菌性脑膜脑炎,该试验暂停。研究团队之前对AN1792脑组织的尸检分析显示,部分免疫患者脑组织中存在Aβ清除,可能通过小胶质细胞进行。然而,这些脑组织中小胶质细胞介导Aβ清除的机制仍不清楚。
实验设计
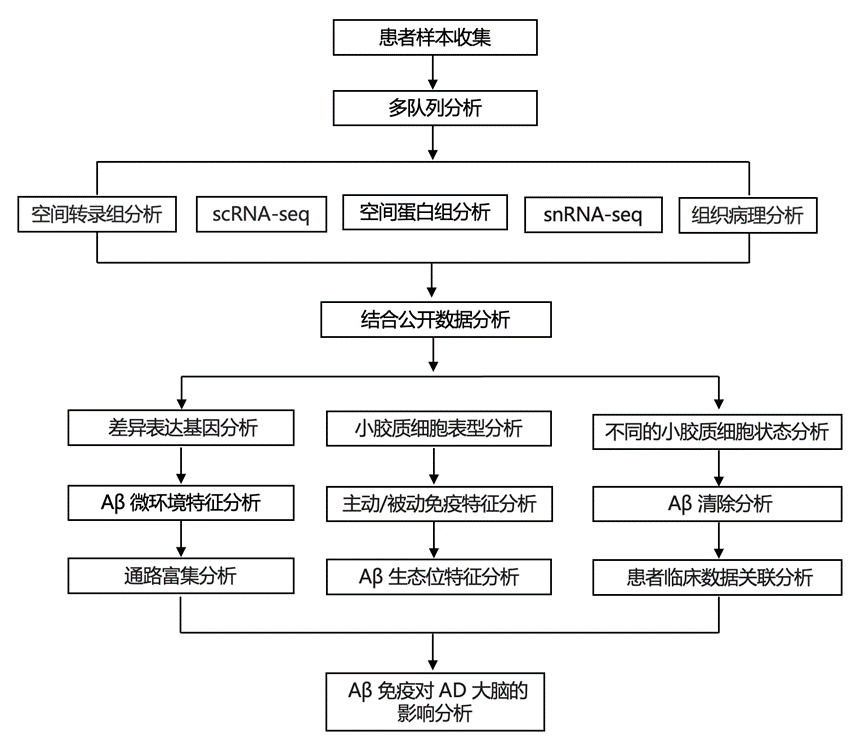
结 果
01
主动 Aβ 免疫维持 Aβ 微环境的炎症
研究团队利用空间转录组分析(ST)技术研究了 AN1792 试验中 AD 患者的大脑额叶皮质 (FCX) 切片(图1a)。该队列包括 13 个AN1792免疫阿尔茨海默病(iAD)大脑,以及 6 个非AN1792免疫性阿尔茨海默病(nAD)和 6 个非神经系统疾病(NND)对照大脑(图1b)。不同组年龄匹配且性别匹配(图1c)。他们分析了 6.5 × 6.5 毫米 ST 捕获区域(4992 个点),并使用 H&E 染色按皮质层、脑膜或白质手动注释 ST 点(图1d)。每个区域的 ST 点或特征计数没有发现显著差异。 iAD 样本的皮质层 I 显示线粒体基因表达较低,提示线粒体代谢发生改变。通过绘制脑膜、白质和层特异性灰质基因表达图来验证注释。
他们使用DESeq2方法来鉴定每个区域的差异表达基因 (DEG)。在 nAD 与 NND 对照中,皮质深层显示的 DEG 最多,而在 iAD 与 nAD 对照中,皮质浅层受影响最大(图1e)。皮质层 III 在 iAD 与 nAD 和 nAD 与 NND 的比较中均表现出许多 DEG。这种高度的转录组失调促使他们进一步检测该皮质层。与对照相比,几乎所有皮质层 III DEG 都是 iAD 或 nAD 所独有的,只有 7.1% 是共有的(图1f)。这些结果表明主动免疫的 AD 皮质浅层发生了转录组改变。
值得注意的是,与 nAD 对照组相比,iAD 皮质 III 层中上调的基因包括髓系细胞表达触发受体 2 (TREM2) 和载脂蛋白 E (APOE) (图1g-h)。这两个基因都是已确定的 AD 风险因素,并且与小胶质细胞对Aβ的反应有关。与 nAD 相比, iAD 中其他上调的皮质 III 层基因包括A2M和CAVIN1,它们参与炎症和溶酶体功能。与 nAD 相比,iAD 中下调的基因包括编码热休克蛋白 (HSP) 的基因,例如热休克蛋白家族 A (Hsp70) 成员 1A (HSPA1A) 和热休克蛋白家族 H (Hsp110) 成员 1 (HSPH1)(图1g-h)。与 NND 对照相比,参与蛋白质折叠和细胞应激的 HSP在nAD 中有所增加(图1h)。对 iAD 与 nAD 和 nAD 与 NND 之间差异最大的 DEG 的分析表明,免疫后 HSP 基因下调,但与 NND 相比,nAD 中呈现相反的方向。相反,突触可塑性相关基因,例如信号蛋白3G (SEMA3G) 和Hes家族BHLH转录因子5 (HES5),在iAD患者的大脑中上调。这些发现表明,免疫接种后皮质层III的转录组发生了改变,包括蛋白质折叠和应激基因减少,以及小胶质细胞反应基因(例如APOE和TREM2)增加。
他们之前证实了 AN1792 患者亚组中存在 Aβ 清除。为了研究驱动 AN1792 患者不同程度 Aβ 清除的机制,他们利用免疫组织化学分析技术 (IHC)对 ST 组织连续切片上的 Aβ 病理进行了定量(图 1i)。Aβ 清除在浅皮质层最为明显,这与之前的研究结果一致。根据残留Aβ覆盖量,iAD 队列分为 Aβ 清除有限 (iAD-lim) 和 Aβ 清除广泛 (iAD-ext) 的队列(图1j-k)。使用 AT8 负荷对这些组灰质中的磷酸化 tau (pTau) 进行定量,结果显示没有显著差异。这与之前的结果相吻合,证明 tau 病理在 Aβ 清除的皮质区域仍然存在。
为了捕获 Aβ 沉积周围的转录组改变,他们将连续载玻片(间隔 5-10 μm)的 Aβ IHC 图像与 ST 数据叠加,并将 Aβ 信号延长 100 μm,每 20 μm 降低强度一次(图1l),血管中富含 Aβ 的 ST 点排除在分析之外。使用基于模型的单细胞转录组学分析(MAST) 对灰质中富含 Aβ 的 ST 点进行差异表达分析,发现 iAD Aβ 微环境内的APOE和富含肉豆蔻酰化丙氨酸的 C 激酶底物(MARCKS)(图1m)表达增加。MARCKS 在 Aβ 斑块周围的活化小胶质细胞中表达。Aβ 微环境中最上调的基因是FAM107A,这是一个影响突触效率和认知的应激反应性肌动蛋白捆绑因子。
比较 iAD-lim 和 iAD-ext 大脑中的 Aβ 微环境,发现 iAD-lim 中炎症基因如 β-2-微球蛋白 (B2M)、A2M、CD74分子 (CD74)、APOE和MARCKS上调,而 iAD-ext 大脑中没有上调(图1n)。通路分析显示,iAD-lim Aβ 微环境内干扰素 α 反应和白细胞介素 2 (IL-2)-STAT5 信号富集。总的来说,在富含 Aβ 的 ST 点中发生改变的基因显示出 iAD-lim 与 iAD-ext 的 Aβ 微环境内的炎症特征。
他们使用局部估计的散点图平滑法 (LOESS)将富含 Aβ 的 ST 点(半径 200 μm)中基因表达和 Aβ 密度之间的非线性关系可视化。层次聚类描绘了 iAD 组内随着 Aβ 密度增加而出现的不同表达模式(图1o)。基因聚类的通路分析显示,在富含 Aβ 的 ST 点中达到峰值的聚类 4 富含免疫相关通路,包括补体信号传导、炎症反应和 IL-2–STAT5 信号传导(图1p)。聚类4 基因在 iAD-lim Aβ 微环境内显示最高的上调,在 iAD-ext 中的增幅较小,在 nAD 中没有上调(图1q)。该基因聚类包含许多免疫相关基因,包括A2M、APOE、补体 C3 (C3)、 RAS 致癌基因家族成员 (RAB13) 和分泌性磷蛋白 1 (SPP1)(图1r)。总之,这些发现揭示了在 AN1792 免疫的大脑中, Aβ 微环境持续存在炎症, Aβ 清除有限,以 IL-2–STAT5 和补体信号为标志,以及 AD 中的炎症反应基因上调。
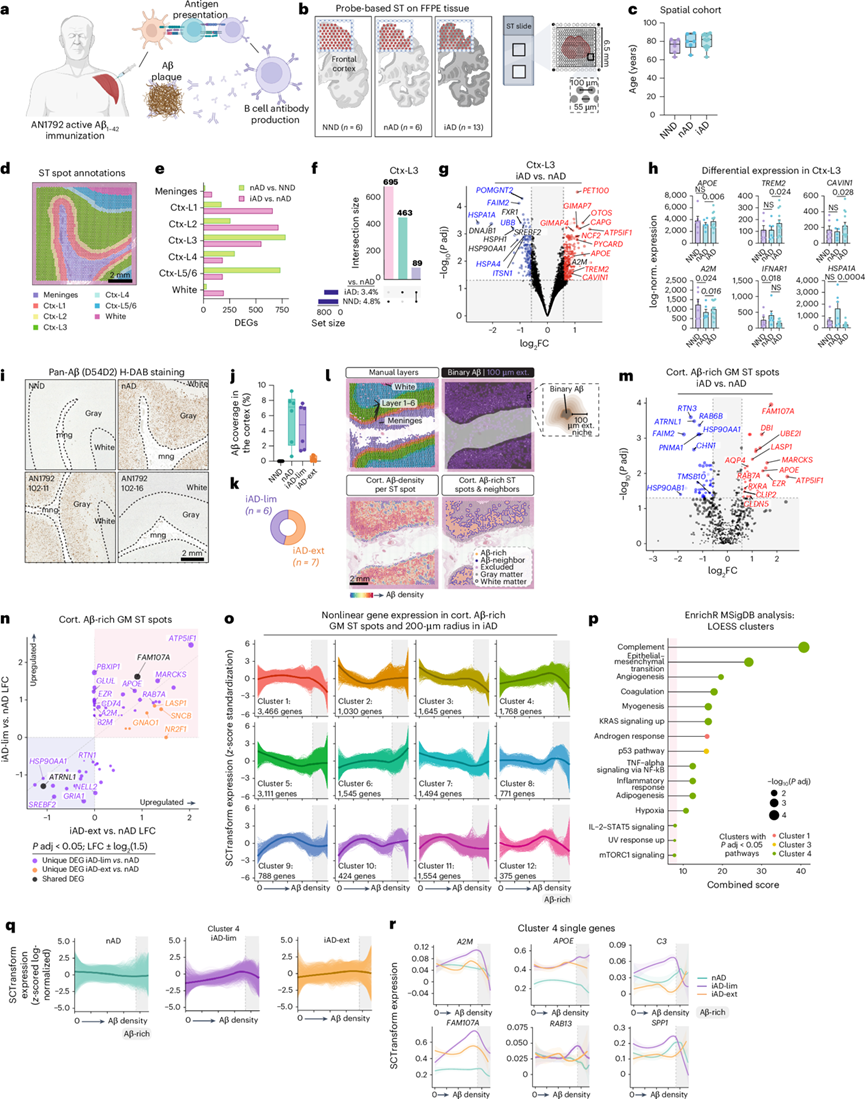
图1. 主动 Aβ 免疫维持 Aβ 微环境的炎症。
(a)实验设计。(b) NND、nAD 和 iAD FCX 组织的 ST 方法分析。(c) 研究人口统计数据表明每位患者的年龄。(d) FCX 中手动注释的 ST 点。(e) 每个手动注释区域每次比较的 DEG 数量。(f) UpSet 图显示皮质层 III 中各组比较的唯一和共有 DEG。(g) 皮质层 III 中的 DEG。(h) 富含小胶质细胞的灰质 ST 点中各种基因的表达。(i) 每组的代表性泛 Aβ H-DAB 染色。(j) 每组皮质 Aβ 覆盖率的定量。(k) AN1792 主动免疫患者中的 iAD-lim 和 iAD-ext 患者人数。(l) Aβ IHC 图像的处理方法。(m) 来自富含 Aβ 的灰质 ST 点(iAD 与 nAD)的 DEG。(n) 灰质中富含 Aβ 的 ST 点的 LFC 图。(o) LOESS图显示相对于 iAD 中 Aβ 密度的非线性基因表达模式聚类。(p) 与 iAD 中 Aβ 密度相关的非线性表达聚类中基因的通路富集分析。(q) 相对于 Aβ 密度的 nAD、iAD-lim 和 iAD-ext 聚类 4 预测的 LOESS 图。(r) LOESS 聚类 4 中选定基因的 LOESS 图。
02
小胶质细胞表型决定了不同程度的 Aβ 清除
由于每个 ST 点包含 1-10 个细胞,他们旨在使用 Cell2Location (C2L) 来分析它们的细胞组成,该方法将 ST 数据与单细胞核转录组分析 (snRNA-seq) 数据相结合。他们从来自 AD 和 NND 对照的 424 个背外侧前额皮质 (DLPFC) 组织的 snRNA-seq 数据集构建了一个参考图谱,采样至 34695 个细胞以获得接近相等的细胞类型表示(图2a)。C2L 分析将细胞类型映射到预期的空间位置(图2b)。在 AN1792 免疫后的灰质中,由于细胞映射不可靠而排除第 I 层,他们观察到星形胶质细胞相对数量增加,第 2/3 层 (L2/3) 兴奋性神经元 (EN) 减少,但是这些变化在统计学上并不显著,预计小胶质细胞在 iAD-lim 皮质中最为丰富。
然后,他们注释了特定细胞类型在其预期空间区域内最富集的 ST 点(图2c)。比较细胞类型富集的 ST 点中 iAD 与 nAD 基因表达,结果显示 L2/3 EN 富集的 ST 点中 DEG 最多,其次是小胶质细胞和星形胶质细胞(图2d)。相反,与 NND 相比,nAD 样本的 DEG 主要出现在 4/5 层 (L4/5) EN、中间神经元和 L2/3 EN 中(图2d)。与 nAD 相比,iAD 中富含小胶质细胞的 ST 点显示APOE、TREM2、A2M、RAB13、FAM107A和其他淀粉样蛋白反应基因[如溶酶体相关膜蛋白 1 (LAMP1)、CD163 分子 (CD163)、含有 PYD 和 CARD 结构域 (PYCARD)、整合素亚基 alpha X (ITGAX) 和载脂蛋白 C1 (APOC1)]的上调,而 HSP 基因下调(图2e)。 iAD 与 nAD 和 nAD 与 NND 之间最不同的 DEG[例如,DnaJ 热休克蛋白家族(Hsp40)成员 A1 (DNAJA1) 和 Fas 凋亡抑制分子 2 (FAIM2)]表明 AN1792 后细胞应激降低,细胞凋亡中断(图2f)。
对富含小胶质细胞的 ST 点进行差异表达分析显示,与 nAD 相比,iAD-ext 中的 DEG 比 iAD-lim 中的多,表明小胶质细胞状态更独特,Aβ 清除范围更广(图2g)。iAD-ext 中唯一上调的基因包括APOE、MARCKS和成纤维细胞生长因子受体 3(FGFR3)(图2h)。FGFR3 是成纤维细胞生长因子 2 (FGF2) 的受体,神经元在寡聚 Aβ 诱导的损伤后释放该因子。这种相互作用促进小胶质细胞迁移和碎片吞噬,有助于神经保护。在 iAD-lim 中, TREM2、A2M和LAMP1以及TYROBP上调,它将 TREM2 与小胶质细胞中的APOE转录联系起来。共有的上调基因包括PYCARD和 Toll 样受体 7(TLR7)(图2h),而非共有基因在两组中显示出相似的趋势,但没有显著性(图2i)。PYCARD激活炎症小体,形成凋亡相关的斑点样蛋白,其中含有可以交叉播种 Aβ 病理的 CARD(ASC)斑点。在 AN1792 免疫的 FCX 中,在 Aβ 斑块周围的 IBA1+小胶质细胞中证实了蛋白质 TMS1/ASC(由PYCARD编码)、A2M 和 APOE的定位(图2j-l)。
在Aβ清除能力不同的组别间,小胶质细胞富集ST点位中差异最显著的基因分别为:iAD-lim组的白细胞特异性蛋白1(LSP1)和免疫相关GTP酶(GIMAP)基因家族,以及iAD-ext组的FGFR3和HSPA1A。LSP1在Fcγ受体介导的吞噬过程中定位于新生吞噬杯 (phagocytic cup)。通路分析显示两组均存在IL-2-STAT5信号通路上调,其中iAD-ext特异性激活氧化磷酸化与脂肪生成通路,而iAD-lim则表现为补体系统和未折叠蛋白反应通路的下调(图2m)。
接下来,他们检测了小胶质细胞富集区域中 iAD-ext 与 nAD 和 NND 与 nAD 之间共有的基因,以确定 iAD-ext 大脑中的转录组变化是否反映了与 NND 类似的恢复稳态。共有的上调基因包括FGFR3、冷诱导 RNA 结合蛋白(CIRBP)和SORBS3,而下调基因包括FAIM2、DNAJA1和热休克蛋白 90 α 家族 A 类成员 1(HSP90AA1)(图2n-o)。CIRBP是一种应激反应基因,可通过抗氧化和抗凋亡通路调节炎症并改善神经元淀粉样蛋白毒性。这些发现表明,iAD-ext 大脑中小胶质细胞富集的 ST 点中的一些 DEG 反映了小胶质细胞基因表达向 NND 对照谱的转变。
为了研究 AN1792 免疫后的小胶质细胞功能,他们将iAD大脑中富含小胶质细胞的 ST 斑点特征与已发表的人类 AD 小胶质细胞状态进行了比较。在这里,AN1792 免疫后的 iAD 大脑显示应激反应性小胶质细胞 (MG6)、炎症状态(MG2、MG8、MG10)和糖酵解小胶质细胞 (MG7) 减少,核糖体生物合成小胶质细胞 (MG3)增加(图2p)。值得注意的是,MG3 小胶质细胞表现出与疾病相关的小胶质细胞 (DAM) 特征基因的强烈富集。相反,与 NND 相比,nAD 中的炎症和应激反应性小胶质细胞状态增加。使用单独的小胶质细胞分类显示免疫后应激反应性小胶质细胞(Mic.11)、小胶质细胞(Mic.2、Mic.4)、反应性小胶质细胞(Mic.6-Mic.8)、干扰素反应性小胶质细胞(Mic.14)和丝氨酸蛋白酶抑制剂家族 E 成员 1(SERPINE1)表达的小胶质细胞(Mic.16)减少(图2q)。总体而言,无论残留 Aβ 水平如何,主动 Aβ 免疫均可降低应激反应性小胶质细胞。然而,iAD-ext 中的小胶质细胞从糖酵解转向氧化磷酸化,而 iAD-lim 中的补体和未折叠蛋白反应减弱,吞噬基因上调。这些发现表明,有效的 Aβ 清除依赖于平衡的小胶质细胞代谢状态,而这种平衡状态也能保护细胞免受 Aβ 的神经毒性。
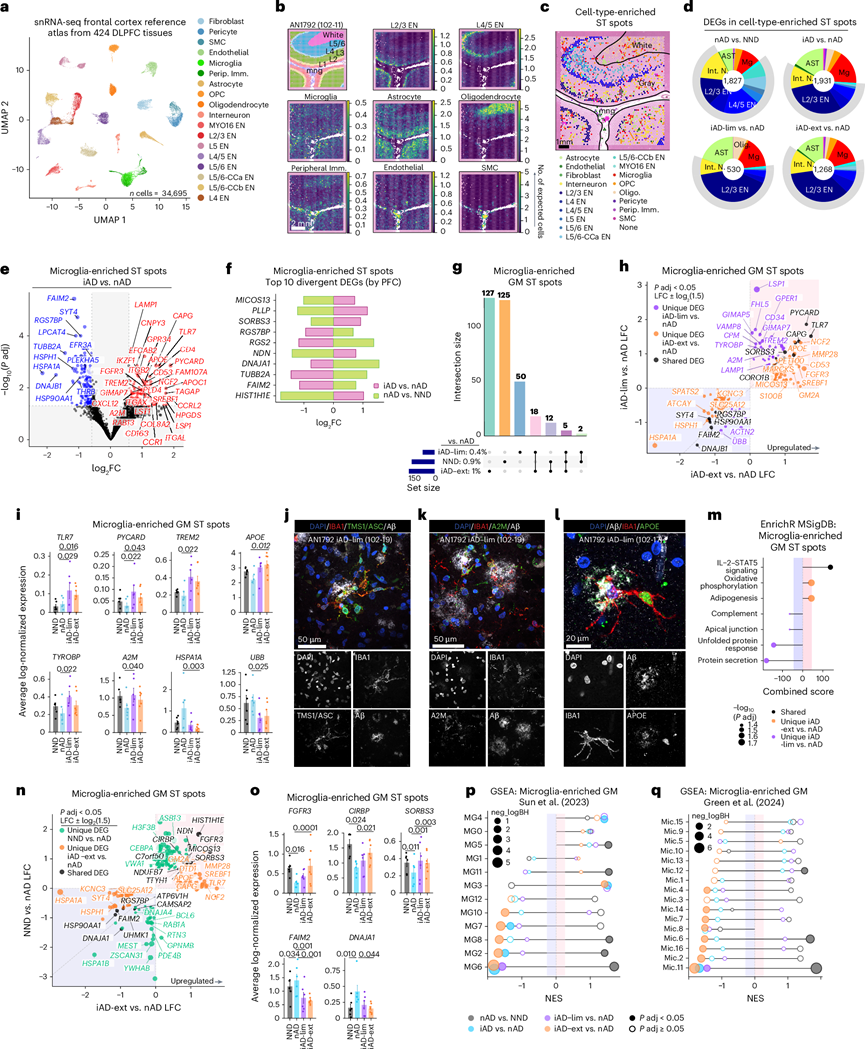
图2. 小胶质细胞表型决定了不同程度的 Aβ 清除率。
(a) 来自 DLPFC snRNA-seq 数据的参考图谱 UMAP。(b) 显示反卷积细胞类型丰度的空间图。(c) 突出显示反卷积细胞类型的富集 ST 点的空间图。(d) 每种细胞类型在富集 ST 点中表达的 DEG 百分比。(e) 来自富含小胶质细胞的 ST 点的 DEG。(f) 基于 PFC 的富含小胶质细胞的 ST 点中前十个不同的 DEG。(g) 与nAD 相比,翻转图显示各组灰质中富含小胶质细胞的 ST 点中独特和共有的 DEG。(h) 灰质中富含小胶质细胞的 ST 点的 LFC 图。(i) 富含小胶质细胞的 ST 灰质点中各种基因的表达。(j-l) 共聚焦图像显示 iAD 的 FCX 中 Aβ 沉积物周围的细胞。(m) 通路富集分析。(n) 富含小胶质细胞的灰质 ST 点的 LFC 图。(o) 灰质中富含小胶质细胞的 ST 点中各种基因表达分析。(p-q) 使用iAD-lim 与 nAD 以及 iAD-ext 与 nAD 中按 PFC 排序的基因。
03
被动Aβ免疫诱导不同的小胶质细胞状态
他们对主动免疫的 AD 患者大脑中小胶质细胞对 Aβ 的反应很感兴趣,因此他们扩大了研究范围,以检测对被动 lecanemab 免疫的免疫反应(图3a)。他们分析了一个特殊的 AD 患者病例,该患者在 5 周内接受了三次 lecanemab 输注,不久后因脑出血去世。他们的尸检分析显示,受 CAA 感染的血管中存在组织细胞性血管炎,血管 Aβ 碎裂和皮质内吞噬作用,同时根据美国国家老龄化和阿尔茨海默病协会 (NIA-AA) 指南,AD 病理负担“很高”。值得注意的是,还观察到实质 Aβ 斑块吞噬作用。他们将该患者与三名APOE ε4/ε4 匹配的对照者进行了比较,这三名对照者均具有高 AD 病理和血管性 AD 病理,且未接受抗 Aβ 治疗(图3b)。研究的皮质组织来自左侧中部 FCX、颞上皮质 (TCX) 和顶下小叶 (PCX),以及后海马 (HIPP)。选择这些区域是因为该患者脑内 Aβ 清除水平不同。他们使用 scRNA-seq 和空间蛋白质组学技术来鉴定这些区域中对被动 Aβ 免疫的细胞类型特异性免疫反应(图3c)。
组织切片进行了IBA1和泛Aβ染色,他们利用人工注释和机器学习技术,区分了皮质和血管性Aβ病理(图3d)。灰质Aβ定量分析显示,与对照组相比,Lecanemab组TCX和PCX的皮质Aβ减少(图3e)。此外,Lecanemab组皮质Aβ中IBA1阳性细胞覆盖的比例更高(约44%),而对照组仅为约15%(图3f)。这些数据表明髓系细胞对Aβ的清除存在区域差异。为了进一步探索被动免疫后对 Aβ 的免疫反应,他们对从每个脑区分离的细胞进行了 scRNA-seq,并使用 SoupX 技术来最大限度地减少环境 RNA 污染。他们评估了质量控制指标、来自所有组织的整合细胞并使用其高表达基因注释的细胞聚类(图3g)。Lecanemab 病例显示 GABA 能中间神经元相对增加,内皮细胞、成纤维细胞和平滑肌细胞减少(图3h)。除 HIPP 外,所有区域均富集 T 细胞,PCX 和 TCX 中的单核细胞/巨噬细胞,以及 TCX、PCX 和 HIPP 中的小胶质细胞(图3h)。
小胶质细胞和巨噬细胞的差异表达分析显示,上调的基因与小胶质细胞活化[SPP1和几丁质酶 3 样 1 (CHI3L1)]、溶酶体功能[组织蛋白酶 B (CTSB)、颗粒蛋白 (GRN)]和干扰素反应[Lecanemab 病例中的干扰素 α 诱导蛋白 6 (IFI6)]有关(图3i)。其他上调的基因包括与铁储存相关的基因[铁蛋白重链 1 (FTH1)、铁蛋白轻链 (FTL) ]和脂质代谢(APOC1)(图3i)。SPP1和APOC1是小胶质细胞独有的上调最多的基因(图3j)。SPP1由活化反应小胶质细胞表达,并有助于组织修复。他们证实了斑块相关小胶质细胞中 SPP1 和 APOC1 蛋白的表达利卡尼单抗治疗后的HIPP。巨噬细胞特异性上调基因包括TREM2、APOE和CD68(图3j)。两种细胞类型均表现出HSP基因表达下降,而血红素加氧酶1 (HMOX1)是它们之间共有的上调最多的基因,反映了Lecanemab治疗的病例中对出血的免疫反应。
为了研究免疫后小胶质细胞和巨噬细胞的功能,他们进行了富集分析。在Lecanemab病例中,调节血管功能(例如顶端连接、凝血和血管生成)的通路在巨噬细胞和小胶质细胞中上调(图3k) 。此外,他们发现巨噬细胞中补体信号失调,而小胶质细胞中补体信号增强(图3k)。他们还观察到小胶质细胞中IL-2-STAT5信号失调,与该通路相关的DEG既有下调的,也有上调的(图3k),这些数据突显了被动Aβ免疫后脑髓系区室的明显改变。
值得注意的是,Lecanemab 病例中的小胶质细胞转录组特征因大脑区域而异。小胶质细胞基因表达的大多数变化都观察到在 TCX 和 PCX 中,这两个区域具有最多的 Aβ 清除率。来自这些区域的小胶质细胞表现出参与补体信号传导(C3)、溶酶体功能和蛋白质降解(例如,组织蛋白酶基因)、铁储存和调节(FTH1、FTL)和SPP1表达增加。区域 DEG 与各种信号通路相关。在 FCX 中,DEG 表明活性氧信号传导增加(图3l) 。TCX 和 PCX 显示补体信号增强,而 PCX 还表现出干扰素反应降低,以及其他变化(图3l)。HIPP 显示胆固醇稳态降低(图3l)。此外,小胶质细胞DEG与血管通路(例如血管生成和凝血)相关,但这种关联仅存在于TCX和PCX(Aβ清除率较高的区域)(图3l)。因此,不同的小胶质细胞表型可能是导致Lecanemab治疗的病例不同脑区Aβ清除率差异的原因。
免疫细胞亚群鉴定出两种小胶质细胞状态,Mg-2 和 Mg-4,它们在接受 Lecanemab 治疗的脑区中富集,这些脑区 IBA1-Aβ 募集和 Aβ 清除最多(图3m-o)。Mg-2 表现出混合的 DAM 和稳态特征,表达TREM2、APOE和稳态标志物,以及高水平的 AXL 受体酪氨酸激酶 (AXL)、C3、CD74和SPP1(图3o-p)。Mg-4 显示出经典的 DAM 特征,ITGAX、脂蛋白脂肪酶(LPL)、基质金属肽酶 9 (MMP9)、CHI3L1和SPP1升高(图3o-p)。两个聚类均显示补体通路信号增强(图3q)。
综上所述,在接受Lecanemab治疗后,小胶质细胞中存在上调基因(例如SPP1和APOC1)。此外,他们在Aβ清除的脑区观察到两种不同的小胶质细胞表型,均表达APOE和TREM2,并显示补体信号增强。这些发现表明,被动Aβ免疫会触发与Aβ清除相关的特定小胶质细胞适应性改变。
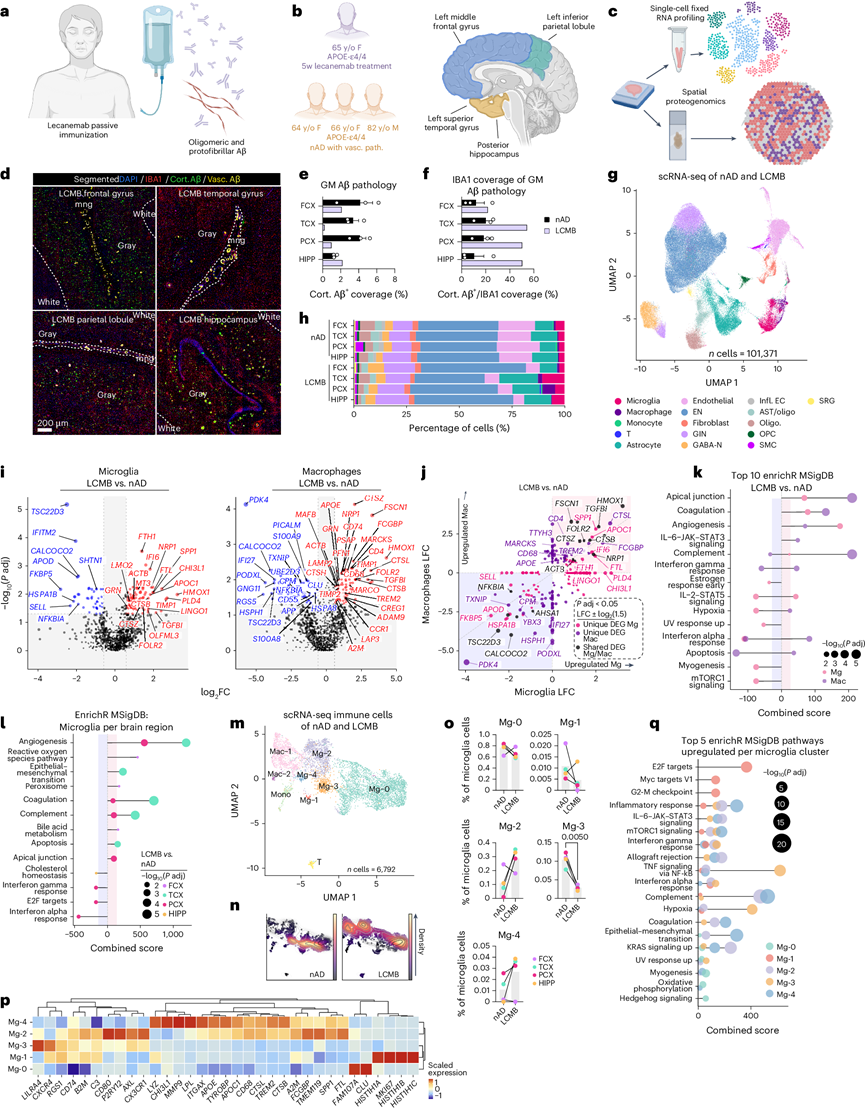
图3. 被动 Aβ 免疫诱导不同的小胶质细胞状态。
(a) Lecanemab 结合寡聚和原纤维 Aβ 以促进大脑中的 Aβ 清除。(b) 研究参与者包括一名接受 Lecanemab 治疗的 65 岁 AD 女性患者和三名匹配的 nAD 对照。(c) 通过 scRNA-seq 和空间蛋白质组学分析组织。(d) 共聚焦图像显示接受 Lecanemab 治疗的患者大脑区域中分段式 Aβ 负担和微胶质增生。(e) Lecanemab 病例和 nAD 对照大脑区域中皮质 Aβ 覆盖率的百分比。(f) IBA1 覆盖的皮质 Aβ 百分比。(g) UMAP 显示带注释的细胞类型。(h) nAD 对照和 Lecanemab 病例之间每个大脑区域每种细胞类型的百分比。(i) 比较 Lecanemab 与 nAD 的小胶质细胞和巨噬细胞中的 DEG。(j) 比较小胶质细胞和巨噬细胞中 DEG 的 LFC 图。(k) 小胶质细胞和巨噬细胞中的前十大通路富集分析。(l) 来自 FCX、TCX、PCX 和 HIPP 的小胶质细胞中的通路富集分析。(m) 来自 Lecanemab 病例和 nAD 对照的 scRNA-seq 的小胶质细胞聚类。(n) UMAP 密度图显示 Lecanemab 病例和 nAD 对照的小胶质细胞聚类分布。(o) Lecanemab 病例与 nAD 对照中的小胶质细胞聚类百分比。(p) 每个小胶质细胞聚类的标记基因。(q) 使用定义小胶质细胞状态的标记基因的前五条上调通路。
04
空间蛋白质组学将 Aβ 微环境与小胶质细胞状态联系起来
在使用单细胞分析确定了小胶质细胞对 Lecanemab 的反应后,他们接下来使用空间蛋白质组学对相邻组织切片进行研究,以研究 Aβ 微环境的免疫反应(图4a)。他们分析了一个 11 × 11 毫米的 ST 捕获区域(14336 个点),使用 DAPI 染色注释的 ST 点以描绘脑膜、皮质层和白质,并排除出血区域(图4b)。质量控制指标揭示了 nAD 大脑中表达基因数量和线粒体读取百分比的变化。然而,区域比较显示 nAD 组和 Lecanemab 病例之间没有显著差异。他们区分了皮质和血管 Aβ,构建了扩张的 Aβ 微环境并定义了富含 Aβ 的 ST 点(图4c)。与 AN1792 的结果一致,他们发现皮质浅层(I 和 II)的 Aβ 减少。然而,与 AN1792 不同的是,差异表达分析显示,皮质深层(III、IV 和 V/VI)(图4d)中的 DEG 最多。
皮质 Aβ 阳性 ST 点的转录组分析表明,在清除最多的区域(TCX 和 PCX),残留的富含 Aβ 的 ST 点失调最严重。与图3中小胶质细胞的单细胞分析一致,TCX 中富含 Aβ 的 ST 点表现出与补体信号传导[C3、补体 C1q C 链(C1QC)]和脂质代谢[APOE、脂肪酶 A、溶酶体酸型(LIPA)]相关的基因表达更高(图4e)。他们观察到 APOE 定位于接受 Lecanemab 治疗的大脑中由 IBA1+髓系细胞包围的 Aβ 斑块上。此外,除 FCX 外,所有区域的 Aβ 微环境都上调了参与溶酶体功能和蛋白质降解(CTSB)、铁储存(FTH1、FTL)和炎症期间细胞外基质重塑(CHI3L1)的基因。A2M在 TCX 和 HIPP Aβ 微环境上调。他们还观察到 A2M 定位于 Aβ 沉积物周围的 IBA1+髓样细胞。值得注意的是,他们发现所有脑区 Aβ 微环境的SPP1和FTH1均上调。TCX 中富含 Aβ 的 ST 点的通路分析显示补体信号通路上调(图4f)。有趣的是,所有区域的脂肪生成通路都有所增加,表明参与脂质代谢过程(图4f)。
接下来,他们在皮质 Aβ 微环境内的蛋白质水平上评估了免疫反应。他们调整了 ST 方法,纳入了 31 种针对免疫蛋白的条形码抗体,这些抗体与 RNA 探针一起转移,以生成空间蛋白质组学数据。他们评估了有或没有相应 DEG 转录本的差异表达蛋白 (DEP)(图4g)。在 DEP 中,HLA II 类组织相容性抗原 DR α 链 (HLA-DRA) 在所有脑区富含 Aβ 的 ST 点中上调(图4g)。与小胶质细胞吞噬反应相关的蛋白质,例如 CD11c 和 CD68,在 TCX 和 HIPP 中上调。IHC 揭示了HIPP 中 Aβ 沉积周围的IBA1+小胶质细胞内有许多 CD68+溶酶体结构(图4h)。有趣的是,免疫抑制受体配体程序性细胞死亡 1 配体 1 (PD-L1) 在 Aβ 清除率最高的区域(TCX、PCX)减少。
他们使用 LOESS 评估了 Lecanemab 治疗脑中富含 Aβ 的 ST 点内的非线性表达变化。他们鉴定了 11 个聚类,其中聚类 3 与免疫途径最相关,包括高补体和 IL-2–STAT5 信号传导。在 Lecanemab 病例中,聚类 3 在 Aβ 含量最高的 ST 点中显著上调,并包括之前鉴定的基因,例如A2M、APOE、APOC1、CTSB、CD68、FCGBP、ITGAX、SPP1和TREM2(图4i-j)。总之,对 Aβ 微环境进行蛋白质组学分析,鉴定了接受 Lecanemab 治疗的 AD 患者中与 Aβ 清除相关的小胶质细胞状态。
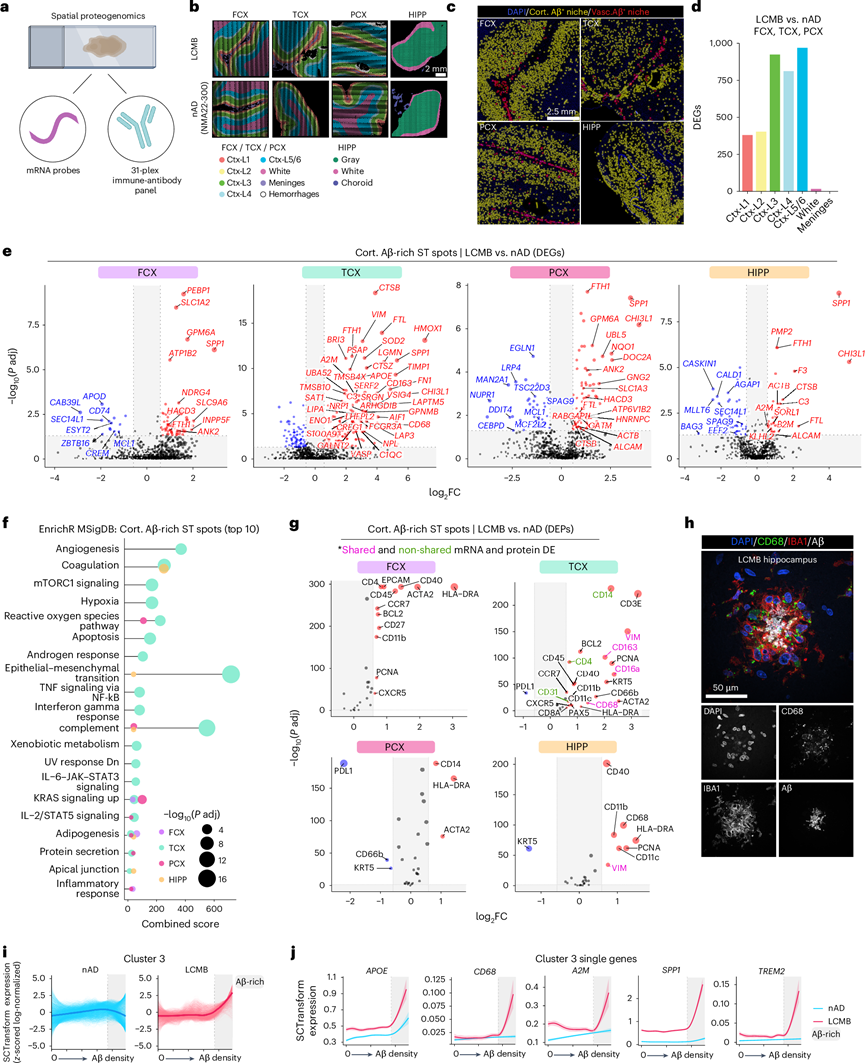
图4. 空间蛋白质组学将 Aβ 生态位与小胶质细胞状态联系起来。
(a) 蛋白质组学可以同时分析 Lecanemab 治疗组和 nAD 对照组的 RNA 和蛋白质。(b) 对大脑区域的手动注释进行分析。(c) 代表性图像显示 Lecanemab 病例中大脑区域中皮质和血管 Aβ 的分段区别。(d) 手动注释区域之间每次比较的 DEG 数量。(e) FCX、TCX、PCX 和 HIPP 中富含 Aβ 的灰质 ST 点(Lecanemab 与 nAD)的 DEG。(f) 每个大脑区域(Lecanemab 与 nAD)富含 Aβ 的灰质 ST 点中 DEG 的前十大通路富集分析。(g) 每个大脑区域(lecanemab 与 CAA 对照)中与皮质 Aβ ST 点相关的 DEP。(h) 共聚焦图像显示接受 Lecanemab 治疗的患者的 HIPP 中 Aβ 沉积物周围的CD68+IBA1+髓系细胞。(i) Aβ 密度的 LOESS 图。(j) LOESS 聚类 3 中选定基因的 LOESS 图。
05
免疫后小胶质细胞反应驱动Aβ清除
为了识别主动和被动免疫后对 Aβ 的常见和不同小胶质细胞反应,他们整合了所有组织的分析。他们定量了灰质中的 Aβ 覆盖率,证实了免疫相关的覆盖率下降(图5a-b)。此外,他们观察到 Aβ 的髓系募集增加(图5c)。他们整合并聚类了皮质灰质富含 Aβ 的 ST 点(图5d)。这产生了九个基于基因表达的不同 Aβ 生态位聚类(图5e)。他们假设这些差异是由不同的细胞微环境驱动的,并使用 C2L 从整合的 scRNA-seq 图谱中预测细胞类型丰度来验证这一点。富含小胶质细胞的皮质 Aβ-6 聚类在 Lecanemab 治疗后的样本中最为突出,其次是 AN1792 样本中的增幅较小(图5f )。该聚类由A2M、APOE、C1QC、C3、SPP1和其他基因的表达定义。因此,皮质 Aβ-6 聚类可能代表富含 Aβ 的 ST 点,其中募集了髓系细胞。在 Aβ 清除有限的 AN1792 样本和 Lecanemab 治疗的大脑区域中,与 nAD 对照相比,该聚类显示出更高的 Mg-2 和 Mg-4 小胶质细胞丰度。
AN1792 和 nAD 样本之间的 Aβ-6 ST 点差异表达分析发现,AN1792 样本中FAM107A、RAB13、TREM2和其他基因上调(图5g)。在 Lecanemab 处理的 ST 点中,他们观察到A2M、APOE和其他基因上调(图5h)。通过 DESeq2分析,他们发现SPP1在 Lecanemab 处理的皮质 Aβ-6 ST 点中高度上调(图5i),在接受 Lecanemab 治疗的脑区的 Aβ 微环境内 Mg-2 和 Mg-4 小胶质细胞亚型富集(图5j-k)。Aβ 相关 Mg-2 和 Mg-4 ST 点的基因表达分析显示,在 AN1792 样本中APOE和FAM107A表达增加(图5l),并且在接受 Lecanemab 治疗的区域中,溶酶体功能和铁代谢基因中APOE、LIPA、SPP1和TREM2上调(图5m)。FAM107A在 AN1792 样本中的 Mg-2 和 Mg-4 Aβ 相关 ST 斑点中特异性增加,而SPP1和LIPA仅与 Lecanemab 治疗相关。使用 CellChat 技术分析,他们绘制了与 APOE、补体和 SPP1 通路相关的细胞间信号传导,发现在 Lecanemab 治疗的大脑中通过补体和 SPP1 通路增加了小胶质细胞信号传导,并且在 Lecanemab 和 AN1792 样本中 APOE 信号传导均增强。
为了实现单细胞分辨率,他们将高清 ST 应用于接受 Lecanemab 治疗的大脑和 nAD 对照的 HIPP。将细胞核分割、聚类并用顶部标记注释(图5n)。他们使用免疫荧光染色将细胞核映射到 Aβ 斑块(图5o)。在接受Lecanemab 治疗的大脑中,在 Aβ 斑块 20 µm 范围内,髓系细胞(假定的小胶质细胞)过度表达,但在 nAD 对照中则没有(图5o-p)。差异表达分析证实,在 lecanemab治疗后,Aβ 斑块附近的小胶质细胞中SPP1、APOE和其他基因表达增加(图5q),SPP1表达定位于 Aβ 周围的细胞核(图5r)。这些数据验证了研究过程中许多低分辨率 ST 结果。
最后,为了鉴定 AN1792 处理和 Lecanemab 处理后大脑中小胶质细胞和 Aβ 斑块微环境的常见和不同基因表达变化,他们根据概率差异倍数 (PFC) 对基因进行排序并分配百分位数等级。在 AN1792 样本中,FAM107A是反应最活跃的基因,其次是 ATP 合酶抑制因子亚基 1 (ATP5IF1)、TREM2和APOE(图5s)。在 Lecanemab 处理的大脑区域中,CHI3L1、F3、HMOX1和SPP1是诱导最活跃的基因(图5t)。值得注意的是,TREM2和APOE在两种治疗中均成为常见的反应基因(图5u),这些结果突出了与主动和被动Aβ免疫相关的独特(FAM107A、SPP1)和常见(APOE、TREM2)小胶质细胞反应基因。
他们将TREM2和APOE表达与 AN1792 患者的临床数据关联起来,发现 AN1792 抗体滴度与富含小胶质细胞的 ST 区斑点中的TREM2 / APOE表达之间存在正相关(图5v)。使用标准化方法评估整个新皮质中的APOE表达与 Aβ 斑块评分之间也呈负相关趋势。这表明小胶质细胞APOE和TREM2的表达水平与免疫反应和 Aβ 清除率直接相关。
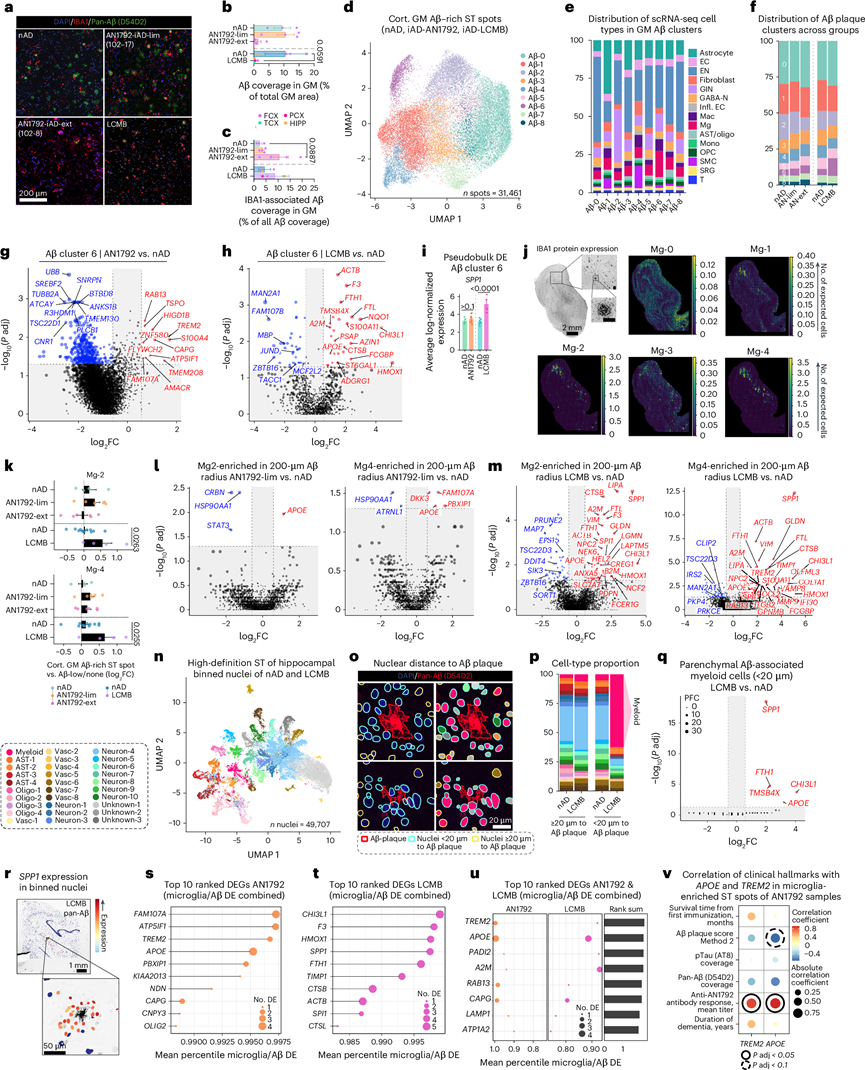
图5. 免疫后,共有的小胶质细胞反应驱动 Aβ 清除。
(a) 共聚焦图像显示 nAD、AN1792-lim、AN1792-ext 和 Lecanemab 治疗患者的 FCX 脑区中的泛 Aβ 和 IBA1。(b) AN1792、nAD 和 Lecanemab 病例的皮质和海马区域中皮质 Aβ 覆盖率的百分比。(c) AN1792、nAD 和 Lecanemab 病例的皮质和海马区域中由 IBA1 覆盖的皮质 Aβ 的百分比。(d) 基于基因表达的富含 Aβ 的皮质灰质斑点的聚类。(e) 不同 Aβ 斑块聚类中 scRNA-seq 细胞类型的 C2L 预测。(f) AN1792、nAD 和 Lecanemab 病例中富含 Aβ 的聚类的百分比。(g-h) 富含 Aβ 的聚类 6 中的 DEG。(i) 富含 Aβ 的聚类6 中的SPP1表达。(j) 显示反卷积 scRNA-seq 小胶质细胞类型丰度的空间图。(k) 在 AN1792、nAD 和 Lecanemab 案例中,富含 Aβ 的 ST 点中反卷积 scRNA-seq 小胶质细胞类型的预测丰度。(l-m) 来自富含 Mg-2 和富含 Mg-4 的 Aβ 相关 ST 点的DEG。(n) UMAP 显示来自高清 ST 检测的带注释的细胞核。(o) 空间图指示细胞核与 D54D2 染色的 Aβ 斑块的距离(左)及其注释(右)。(p) nAD 和 Lecanemab 病例中距离 Aβ 斑块 ≥20 µm 和 <20 µm 处高清 ST 检测中每种细胞类型的百分比。(q) 来自距离 Aβ 斑块 <20 µm 范围内髓系细胞核的 DEG。(r) 空间图显示Lecanemab HIPP 中 Aβ 斑块周围细胞核中的SPP1表达。(s-t) 按 AN1792和 Lecanemab中小胶质细胞和 Aβ 差异表达的平均百分位数排序的前十个上调反应 DEG。(u) 按基因排名平均百分位数相加,对 AN1792 和 Lecanemab 的前十个组合反应基因。(v) TREM2和APOE之间的协变量调整 Spearman 相关性AN1792 患者富含小胶质细胞的灰质 ST 点的表达和临床特征。
+ + + + + + + + + + +
结 论
本研究使用多组学技术来探索主动和被动 Aβ 免疫对 AD 大脑的影响,比较了主动免疫的 AD 患者、未免疫的 AD 患者和神经健康对照者,确定了与 Aβ 清除相关的不同小胶质细胞状态,深入研究了 Lecanemab 治疗后与 Aβ 清除有关的转录通路,发现了因大脑区域而异的空间上不同的小胶质细胞反应。本研究的分析表明,在不同免疫方法中,TREM2 和APOE均上调,这与抗体反应和 Aβ 清除呈正相关。此外,本研究还发现脑髓系细胞中的补体信号有助于免疫接种后Aβ的清除。这些结果为调控Aβ清除的转录机制提供了新的见解,并阐明了小胶质细胞在免疫介导的Aβ清除中的作用。重要的是,本项研究发现了可能增强Aβ靶向免疫疗法的潜在分子靶点,为开发更有效的AD治疗策略开辟了新途径。
+ + + + +



 English
English


