文献解读|Sci Transl Med(14.6):蛋白质组学表征揭示脂滴形成促进食管鳞状细胞癌进展
✦ +
+
论文ID
原名:Proteogenomic characterization reveals that lipid droplet formation promotes esophageal squamous cell cancer progression
译名:蛋白质组学表征揭示脂滴形成促进食管鳞状细胞癌进展
期刊:Science Translational Medicine
影响因子:14.6
发表时间:2025.06.11
DOI号:10.1126/scitranslmed.adt0214
背 景
食管鳞状细胞癌 (ESCC) 是一种高发癌症,尤其在中国,占全球病例的一半以上。大多数 ESCC 患者确诊时已为晚期,淋巴结 (LN) 或远处转移与预后不良相关(中位生存期:4 至 6 个月)。此外,分化较差的 ESCC 肿瘤患者的预后更差。中国的全基因组关联研究发现了 ESCC 反复改变的基因[包括肿瘤蛋白 53 (TP53) 和赖氨酸甲基转移酶 2D ( KMT2D )]。508例 ESCC 患者的全外显子组测序 (WES) 发现了三个与转移和不良预后相关的突变特征聚类,体细胞畸变涉及 WNT、Notch 和 Hippo 通路。蛋白质组学研究将患者分为高危(S2)亚型和低危(S1)亚型,分别以增殖和粘附为特征。然而,基因组变异与食管鳞状细胞癌表型之间的机制关联尚不清楚。
实验设计
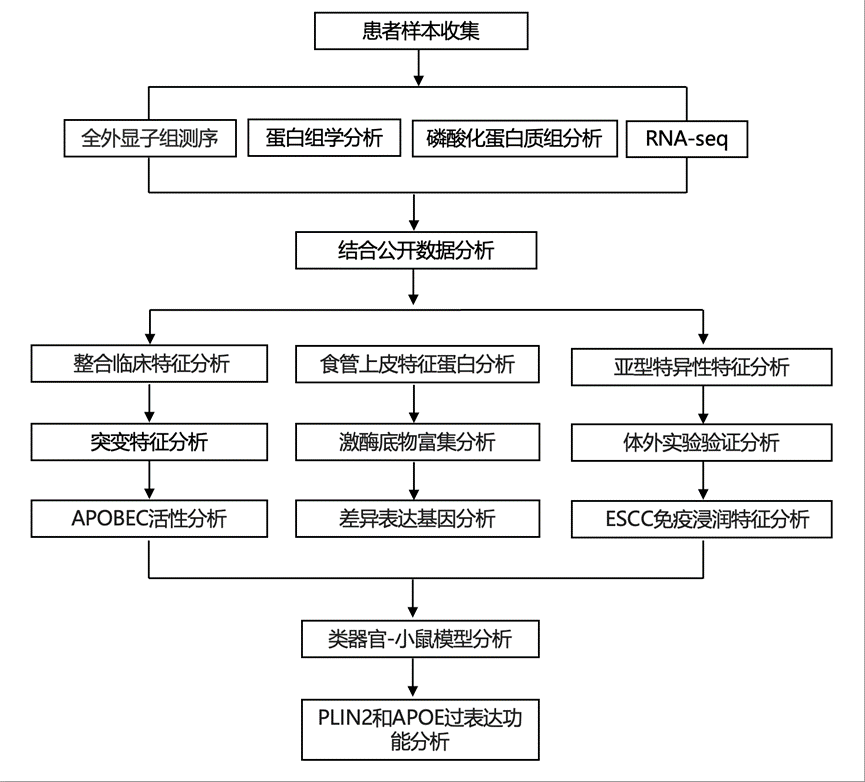
结 果
01
ESCC的多组学分析
本研究的ESCC队列包括290例肿瘤、212例正常癌旁组织 (NAT)、30例淋巴结转移和28例正常淋巴结,这些患者来自293例初治ESCC患者,临床特征各异(图1 A-B)。所有样本均采用WES、转录组分析 (RNA-seq) 以及基于质谱 (MS) 的蛋白质组学和磷酸化蛋白质组学进行分析。
WES 鉴定出 41620 个体细胞变异(图 1C-D)。胞嘧啶到胸腺嘧啶的转变 (C>T) 是载脂蛋白 B mRNA 编辑催化多肽样 (APOBEC) 介导的诱变的标志,在本研究的队列中占主导地位,这与其他 ESCC 队列一致(图 1E)。四种突变谱(A、B、C 和 D)与癌症体细胞突变目录 (COSMIC) 突变特征相似,例如单碱基替换特征 30 和 13(SBS30 和 SBS13),均与胞苷脱氨酶的 APOBEC 家族相关。APOBEC 特征与 ESCC 致癌作用有关。研究团队使用富集评分评估了APOBEC的富集情况,发现APOBEC活性高的肿瘤在晚期食管鳞状细胞癌中普遍存在,且与较差的总生存期(OS)(图1F)相关。具体而言,过氧化物酶体脂质代谢是APOBEC高表达组中主要富集的通路之一(图1G),提示APOBEC诱变与脂质代谢失调之间存在潜在的机制联系。
在 50 个肿瘤中检测到29479 个独特基因,在 52 个 NAT 中检测到28434个独特基因(图 1A)。mRNA 和蛋白质表达分析显示,样本间 mRNA-蛋白质相关性相当一致,但肿瘤和 NAT 之间的基因间相关性不同。mRNA 和蛋白质量高度相关的基因与细胞外基质 (ECM) 受体相互作用和脂肪酸 (FA) 代谢有关,而 mRNA 和蛋白质表达量不一致的基因则在核糖体、氧化磷酸化和剪接体成分中富集。转录组学和蛋白质组学之间的这种不一致凸显了转录后和翻译后调控机制在塑造基因功能中的重要性,表明仅靠 mRNA 丰度可能无法准确反映 ESCC 中的功能性蛋白质水平。
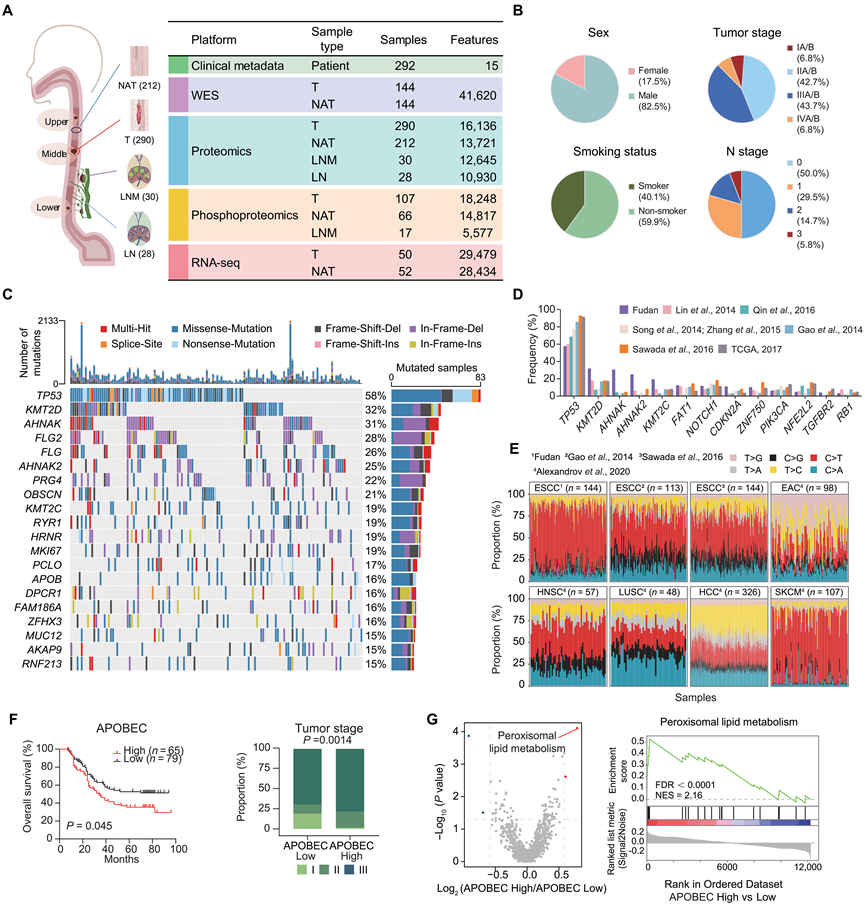
图1. ESCC 样本的多组学景观。
(A) 293 例 ESCC 患者的临床特征和多平台数据概览。(B) 饼图展示 ESCC 患者的主要临床特征。(C) 直方图(上)显示每位 ESCC 患者的突变数量,全基因组突变图景(下)显示按突变类型划分的 SMG。直方图(右)显示左图中 ESCC 患者中 SMG 的发生情况。(D) 条形图比较复旦队列与其他 ESCC 研究中所有样本的 WES 突变频率。(E) ESCC 中的替代分类和富集的突变特征。(F) Kaplan-Meier 图(左)显示按 APOBEC 特征表达量分层的总生存率,直方图(右)显示 ESCC 中不同肿瘤分期中 APOBEC 特征比例的分布。(G) 火山图(左)和 GSEA 图(右)显示 APOBEC -high组与 APOBEC -low组之间过氧化物酶体脂质代谢途径的富集。
02
基因畸变对多组学的影响
在食管鳞状细胞癌中,发现了染色体的增加,包括11q13.3、12q13.13、17q25.3和8q24.13,这些染色体的增加影响了RNA、蛋白质和磷蛋白的丰度。显著的顺反效应表明,RNA数量变化在核糖体生物合成和肌动蛋白细胞骨架等管家通路中富集,而蛋白质/磷蛋白数量变化在WNT信号和钙信号等癌症相关通路中富集。综合多维数据分析显示,染色体 11q13.3 的增加与死亡结构域相关 Fas (FADD) 和细胞周期蛋白 D1 (CCND1)等基因表达增加相关,尤其是在位于下食管区域的肿瘤中。
Cox 回归分析显示,染色体 12q13.13和 17q25.3 的增加与 ESCC 预后不良相关,而染色体 11p11.12 的增加与预后良好相关;具体而言,12q13.13 包含编码 II 型 KRT 的基因(图 2A)。他们发现染色体 12q13.13 的增加与分化良好的 ESCC 肿瘤相关,并与 KRT76 和 KRT78 的蛋白表达以及 KRT5 和 KRT6 的磷酸化表达增加呈正相关,而这些都与肿瘤大小的增加呈正相关(图 2B-C)。KRT76编码一种对维持上皮结构完整性至关重要的细胞骨架蛋白,主要在复层上皮(包括毛囊和指甲)中表达。类似地,KRT78 参与中间丝的形成,提供结构支撑,尤其是在机械应力作用下。在 12q13.13 染色体上观察到的 KRT(包括KRT76和KT78)的积极作用提示,该区域的扩增可能与 ESCC 的高分化和中分化组织相关。12q13.13 染色体扩增与患者高分化和中分化(而非低分化)ESCC 组织的不良预后相关。
在高分化和中分化的 ESCC 组织中,染色体 12q13.13 增益与 V-Yes-1 Yamaguchi 肉瘤病毒相关致癌基因同源物 lck/yes 相关 (LYN)、酰基辅酶 A 合成酶短链家族成员 1 (ACSS1) 和卷曲螺旋-卷曲螺旋-螺旋结构域 6 (CHCHD6) 等蛋白质的增加相关,这些蛋白质仅在高分化和中分化的 ESCC 组织患者中与不良预后相关(图 2D)。基因集富集分析 (GSEA) 显示,ACSS1和CHCHD6与 FA 代谢和氧化磷酸化途径相关。研究表明,脂肪酸代谢与肿瘤生长和恶性程度有关,提示ACSS1和CHCHD6在 ESCC 致癌作用中可能发挥作用。此外,FC γ 受体 1a(FCGR1A)和富含亮氨酸重复序列和钙调蛋白同源结构域 1(LRCH1)通过 FCGR 激活信号通路影响免疫调节。LYN 是一种肉瘤 (SRC) 家族激酶,可激活 Janus 激酶信号转导和转录激活因子信号通路,这与通路蛋白表达增加相关,并促进肿瘤增殖、侵袭和免疫逃逸。总之,这些研究结果表明,染色体 12q13.13 的获得通过 KRT 支持肿瘤分化,但通过增强致癌信号传导和代谢重编程与高分化 ESCC 中的恶性程度相关。
在前 30 个显著突变基因 (SMG) 中,只有KMT2D突变(一种 H3K4 甲基转移酶)与良好预后呈显著正相关(图 2E)。KMT2D突变不影响其 mRNA、蛋白质和磷酸化量,但降低了其靶基因 (TG) 的蛋白质量,表明 KMT2D 突变体的转录调控受到抑制(图2F-G)。关键的KMT2D TG,包括围脂滴蛋白2 (PLIN2) 和磷脂酰肌醇 4-激酶 α (PI4KA),显示蛋白质减少(图 2H-I)。 PLIN2 在 LD 形成中起关键作用,影响磷脂酰肌醇 (PI) 代谢途径,该途径参与上调 ESCC 中的磷酸肌醇 3-激酶-蛋白激酶 B (PI3K-AKT) 途径。此外,包括 PLIN2 和 PI4KA 在内的脂质代谢蛋白与不良预后相关(图 2J)。LD 与 PI 信号传导之间的关联已得到充分证实,质膜 (PM) 上的磷脂酰肌醇 4-磷酸 (PI4P) 作为 PIP2/PIP3 的前体,调节脂质运输和 LD 形成。PI4KA 对于在 PM 上生成 PI4P 至关重要。本研究的数据分析表明,食管癌中的 LD 与 PI4KA 之间存在很强的相关性。
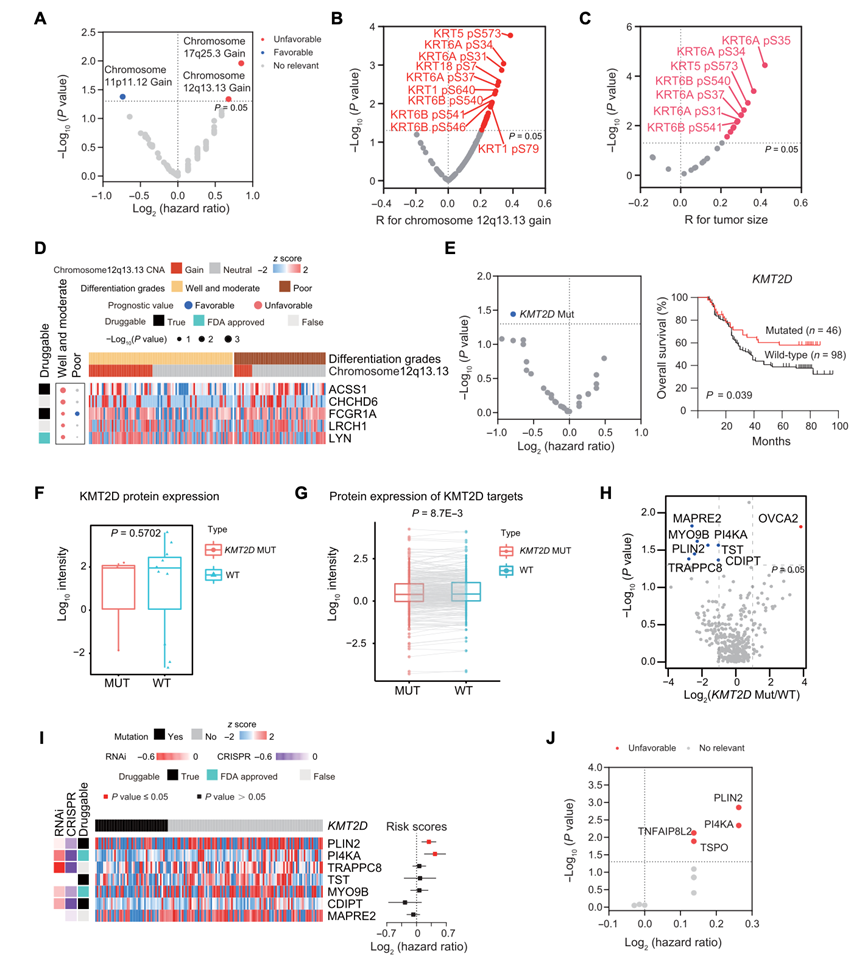
图2. 拷贝数变异和体细胞突变对 ESCC 多基因组图谱的潜在影响。
(A) 该图显示了 ESCC 中局部增益峰的预后影响。(B) 火山图显示了 12q13.13 染色体增益对 II 型角蛋白磷酸化位点表达的顺式影响。(C) 火山图显示了 II 型角蛋白磷酸化位点表达与肿瘤大小之间的相关性。(D) 高分化和中分化 ESCC 中 12q13.13 染色体增益相关基因的热图,标注了可用药性和预后。(E) 山图显示前 30 个 SMG 的预后关联。(F-G) KMT2D 的蛋白质表达。(H) KMT2D突变组和 WT 组之间差异表达 TG 的火山图。(I) 左图显示了RNA干扰 (RNAi)、成簇的规律间隔短回文重复序列 (CRISPR) 介导的TG敲除的影响及其药物性,右图显示了TG相关的预后风险评分。(J) 与ESCC患者不良预后(红色)相关的脂质代谢相关蛋白。
03
肿瘤-NAT比较揭示ESCC相关的多组学改变
多组学分析(包括转录组学、蛋白质组学和磷酸化蛋白质组学)揭示了食管鳞状细胞癌 (ESCC) 的关键特征。主成分分析 (PCA) 显示,在蛋白质组学、转录组学和磷酸化蛋白质组学数据中,肿瘤与 NAT 之间存在界限(图 3A)。反应组通路分析表明,ECM 组织和细胞周期通路在肿瘤中以拷贝数变异 (CNA)、RNA、蛋白质和磷酸化量丰富,而角质化包膜形成和黏附连接相互作用在 NAT 中占主导地位(图 3B-C)。这些通路的差异表达蛋白 (DEP) 与 ESCC 临床结果相关,表明这些通路在 ESCC 进展中的作用。
蛋白质组学分析显示,食管上皮特征蛋白,尤其是KRT(包括KRT4和KRT6A),在肿瘤中表达降低(图3D)。KRT4和KRT6A的高表达与良好的预后相关。然而,KRT17、KRT18和KRT23在肿瘤中表达升高,其中磷酸化的KRT17 S12和S13表达升高,与不良预后相关(图3D-E)。KRT 磷酸化与角蛋白溶解度和细胞变形性增加有关,从而促进肿瘤进展。在 NAT 中高表达的 KRT5、KRT6A 和 KRT6B 在肿瘤中也过度磷酸化,这与肿瘤增大和预后不良相关(图 3D-E)。为了验证 KRT 在 ESCC 中的发现,他们整合了公开队列数据集,该数据集展示了从正常食管组织到早期 ESCC 和晚期 ESCC (A-ESCC) 的动态进展,KRT 表达模式证实了它们在 ESCC 进展中的作用。在 ESCC 进展中,II 型 KRT 减少,而 I 型 KRT (KRT17 和 KRT18) 增加。在A-ESCC中,KRT5 (S52)、KRT6 以及 KRT17(KRT17 S13、S17、S50 和 S323)的磷酸化水平升高。这些发现表明,在ESCC中,大多数II型KRT在蛋白质水平上降低,但磷酸化水平升高;而大多数I型KRT在ESCC中,蛋白质和磷酸化蛋白的含量均升高,这突显了KRT过度磷酸化是ESCC的潜在治疗靶点。
为了探索食管鳞状细胞癌 (ESCC) 的潜在药物靶点,他们进行了肿瘤和 NAT 之间的差异表达分析(数据文件 S4),并确定了一组候选标志物,包括整合素 β 亚基 5 (ITGB5)、胰岛素受体 (INSR)、硫酸软骨素蛋白聚糖 4 (CSPG4) 和成纤维细胞活化蛋白 α (FAP)。免疫组化染色证实了这些标志物在肿瘤组织中的表达升高,支持它们在 ESCC 发病机制中的潜在作用。此外,PLIN2 和 APOBEC3B 与较差的 OS 相关(图 3F),提示这些标志物具有潜在的预后价值。
为了探究分子标记物 PLIN2 和 APOBEC3B 是否可以作为食管癌的血浆标记物,他们收集了另一个队列数据,包括来自 55 名 ESCC 患者的 55 个 ESCC 血浆样本、来自 15 种其他癌症类型的 966 个血浆样本和 200 名非癌症对照者,并在每个样本中检测到约 1800 种蛋白质。比较分析表明,与健康对照或其他癌症类型相比,ESCC 血浆样本中的 PLIN2 和 APOBEC3B 升高(图 3G-H)。此外,在 LNM 患者中发现了更高含量的 PLIN2 和 APOBEC3B(图 3I)。
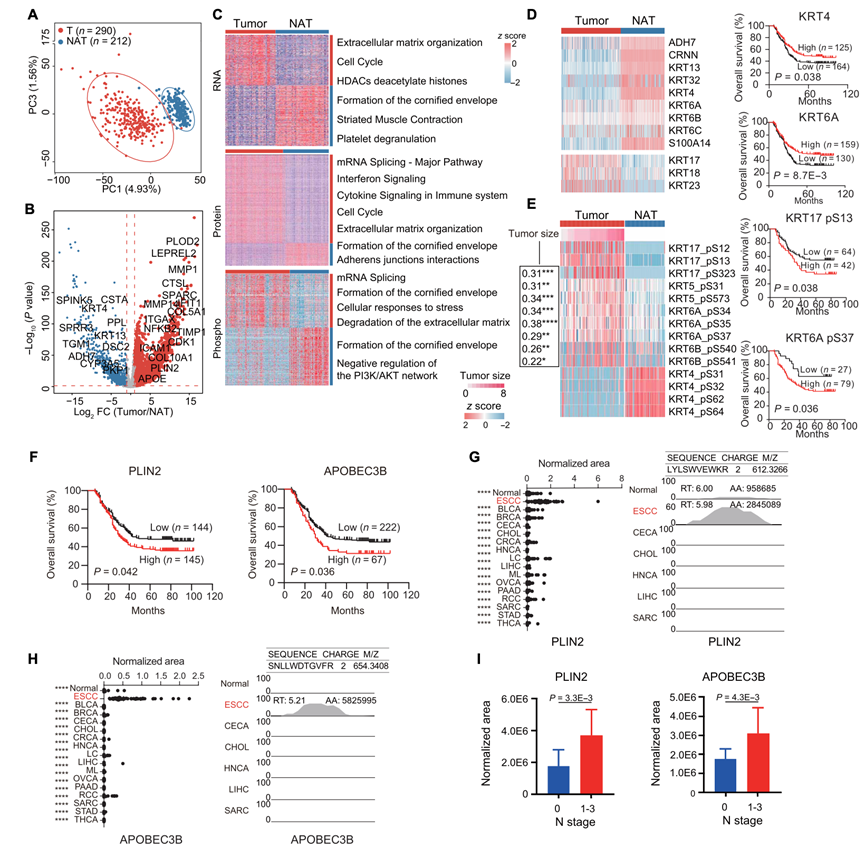
图3. ESCC 中的肿瘤和 NAT 的多组学特征。
(A) PCA 显示,根据 DEP数据,肿瘤和 NAT之间存在明显分离。(B) 火山图显示肿瘤和 NAT 之间的 DEP。(C) ESCC 肿瘤和 NAT 之间差异表达的 mRNA、蛋白质、磷酸位点和通路。(D) 热图显示食管上皮特征蛋白和 KRT(左)以及预后相关蛋白(KRT4 和 KRT6A;右)的表达。(E) 热图(左)显示角化相关磷酸位点的表达量及其与肿瘤大小的相关性,Kaplan-Meier 图(左)显示这些磷酸位点在 ESCC 患者中的预后意义。(F) Kaplan-Meier 图显示高和低 PLIN2(左)和 APOBEC3B 表达(右)的 OS。(G) 直方图显示 ESCC、正常对照和其他 15 种癌症血浆样本中 PLIN2 表达的标准化面积(左)和总面积(右)。(H) 直方图显示 ESCC、正常对照和其他 15 种癌症血浆样本中 APOE 的标准化面积(左)和总面积(右)。(I) 柱状图显示患有LNM和不患有LNM 的 ESCC 患者的 PLIN2(左)和 APOBEC3B(右)的标准化面积。
04
ESCC患者的蛋白质组亚型
基于多组学数据中 NAT 和肿瘤之间的差异表达基因 (DEG) 进行无监督聚类,并鉴定出三种蛋白质组亚型(图 4A)。与转录组和磷酸化蛋白质组亚型相比,蛋白质组亚型表现出分离和不同的预后结果。反应组通路分析显示,第 1 组 (G1;n = 53) 的特征是细胞周期相关基因表达增加,AHNAK2、teneurin 跨膜蛋白(TENM4) 和15 号染色体开放阅读框 39 (C15orf39) 突变富集。G1 中的患者具有最佳的 10 年 OS 和无病生存率 (DFS)(图 4B-C)。 KSEA 显示 CDK 和核糖体蛋白 S6 激酶 (RPS6K) 激活,同时其底物如 RB 转录辅阻遏物样 (RBL2) S1068 和真核翻译起始因子 4B (EIF4B) S422 表达上调(图 4D)。第 2 组 (G2;n = 117) 与 ECM 组织相关,其特征为锌指同源框 3 (ZFHX3)、锌指 CCCH 型含 13 (ZC3H13) 和钙粘蛋白 EGF LAG 七通道 G 型受体 1 (CELSR1) 突变。 P21 活化激酶 1 (PAK1)、PAK2 和 AKT1 参与促进细胞迁移,预测它们在 G2 中发生激活,并与 G2 组中其底物的上调相关(图 4D)。第 3 组(G3,n = 38)的特点是脂质代谢和显著的染色体获得事件(包括 2p、2q 和 3p 增益)。G3 中的患者的 OS 和 DFS 率最差(图 4B-C)。CSNK2A1、DNA 依赖性蛋白激酶催化亚基 (PRKDC) 和 MAPK 等激酶发生激活(图 4D)。磷酸化蛋白质组学数据的 KSEA 鉴定了亚组特异性的活化激酶,这与不同的分子特征相一致,并表明了 ESCC 精准治疗的潜在脆弱性。
将含有染色体 2p 增益的样本主要分配到 G3。染色体 2p 增益与小分子转运和脂质代谢相关蛋白的上调相关,其中大多数与 ESCC 预后不良相关(图 4E)。PLIN2 是 LD 形成和脂质代谢的关键因素,在 ESCC 中显示出致癌潜力(图 2I)。此外,PLIN2 在染色体 2p 增益组中过度表达(图 4E)。视黄醇 X 受体 α (RXRA) 和 β (RARB) 与过氧化物酶体增殖物激活受体 α (PPARα) 形成 TF 复合物,调节脂质代谢酶,并且 PPARα 通路在具有染色体 2p 增益的 ESCC 患者中富集。这些结果表明,G3 的特征性染色体 2p 增益增强了 PPARα 功能,促进了脂质代谢和 LD 积累,这与 ESCC 中最差的预后相关。
为了评估本研究的蛋白质组亚型的适用性,他们整合最具代表性的蛋白质对 公开队列进行分类,鉴定出三种亚型(SG1、SG2 和 SG3),其中与 SG1 和 SG2 亚型相比,SG3 显示出最差的 OS,并且与高风险 S2 亚型聚集(图 4F-G)。SG3 亚型以脂质代谢为特征(图 4H),与G3 亚型一致,并显示峰值 PLIN2 表达。在 TCGA 队列中,本研究的算法识别出两种亚型(TG1 和 TG2)。TG2亚型与高危G3亚型一致,且与TG1亚型相比,其总生存期更差。通路富集分析显示,TG2与G3亚型之间存在共同特征,并且PLIN2在TCGA队列中也与较差的总生存期相关。
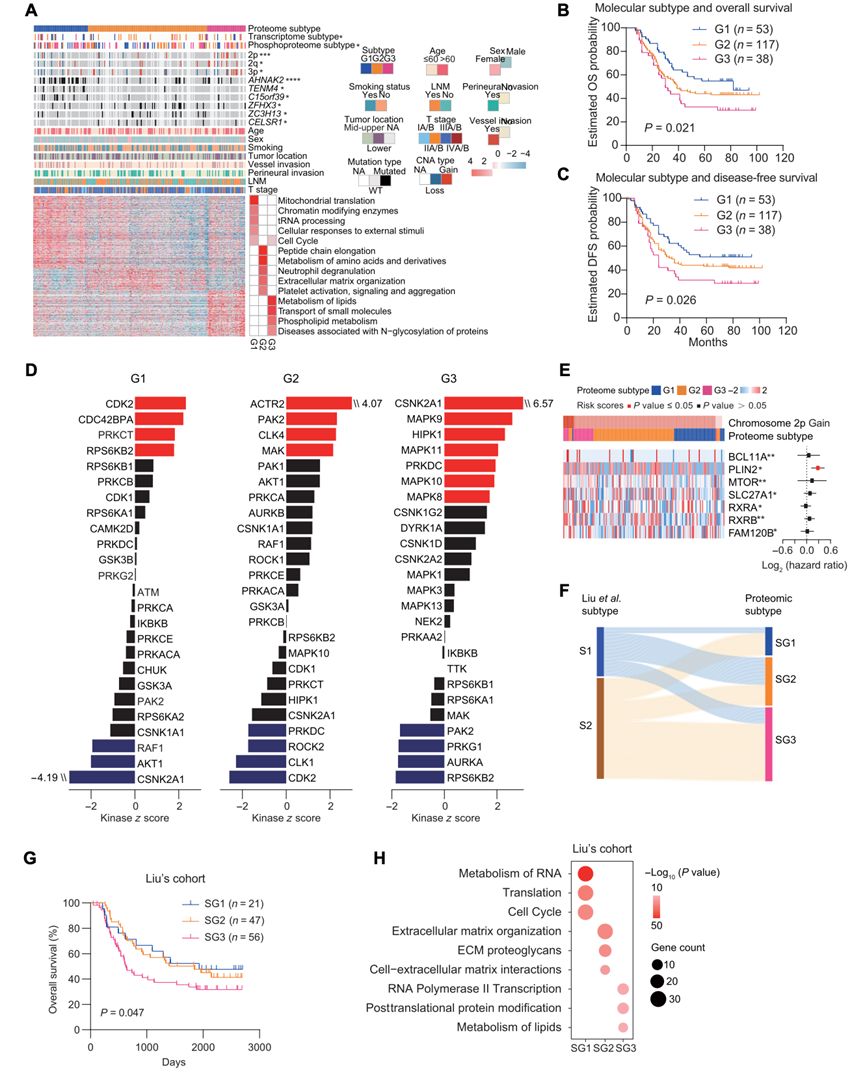
图4. 蛋白质组亚型和亚型特异性靶向治疗。
(A) 热图显示三种蛋白质组亚型及其与 ESCC 其他亚型和临床特征的相关性(左)及其主要通路富集(右)。(B) Kaplan-Meier 图显示 208 例 ESCC 患者中三种蛋白质组亚型的 OS。(C) Kaplan-Meier 图显示 208 例 ESCC 患者中三种蛋白质组亚型的 DFS。(D) 亚组激酶富集分析。(E) 热图(左)显示染色体 2p 增益对脂质代谢相关蛋白表达的影响,森林图(右)显示它们在 ESCC 患者中的预后意义。(F) Sankey 图显示基于各自分类方法的的蛋白质组亚型分布。(G) Kaplan-Meier 生存分析。(H)通路分析。
05
8q 染色体增益是 ESCC 中淋巴结转移的基因组驱动因素
淋巴结转移患者的总生存期 (OS) 和无病生存期 (DFS) 最差。复旦队列的多组学分析显示,淋巴结转移病例中晚期和脉管侵犯的比例更高(图 5A)。KEGG分析显示,淋巴结转移阳性的ESCC细胞周期和脂质代谢通路富集,而淋巴结转移阴性的ESCC细胞间隙连接和胶原形成较为显著。
为了探究基因变异对ESCC淋巴结转移(LNM)的影响,他们检测了染色体增加与淋巴结转移状态之间的关联,发现8q染色体增益与LNM、淋巴结分期和血管侵犯显著相关(图5B)。为了进一步阐明LNM的多维调控机制,他们进行了多组学数据分析,发现8q染色体顺式调控基因中,只有ATPase家族AAA结构域基因2(ATAD2)和ST3β-半乳糖苷α-2,3-唾液酸转移酶1(ST3GAL1)与8q染色体拷贝数呈正相关(图5B)。 ST3GAL1 与唾液酸代谢和恶性肿瘤相关,而 ATAD2 是驱动 E2F 靶点激活的致癌辅助因子,两者均与LNM相关(图 5C)。此外,他们发现 ATAD2 高表达与ESCC中的 E2F 靶基因呈正相关,其中驱动蛋白家族成员 20A (KIF20A) 与LNM呈正相关,可预测 E2F 靶点和 G2 - M 检查点通路活性(图 5D)。
为了验证ATAD2和ST3GAL1在促进ESCC淋巴结转移中的作用,他们进行了一系列体外实验,评估它们对细胞侵袭和增殖的影响。细胞计数试剂盒8(CCK-8)检测结果显示,与未接受抑制剂的对照组相比,用UCN-01抑制ATAD2和用siastatin B抑制ST3GAL1可显著降低ESCC细胞增殖。Transwell实验显示,与对照组相比,两种抑制剂均抑制了细胞侵袭(图5E)。上皮间质转化(EMT)是转移性细胞的一个关键特征。此外,与抑制剂治疗组相比,对照组中EMT相关蛋白的表达过高。
PCA 显示 LNM 中的蛋白质表达模式与 LN 和原发性肿瘤组织不同(图 5F-H)。LNM 和 LN 的比较显示 LNM 中高表达的蛋白质参与细胞周期、ECM 组织和包膜形成。LNM 和原发性肿瘤组织之间的蛋白质组学和磷酸化蛋白质组学比较显示,包括连环蛋白 beta 1 (CTNNB1)、丝氨酸蛋白酶抑制剂家族 B 成员 5 (SERPINB5) 和 stratifin (SFN) 在内的蛋白质在 LNM 中上调,而核因子 κB 亚基 2 (NFKB2)、烟酰胺N -甲基转移酶 (NNMT) 和胞苷/尿苷单磷酸激酶 2 (CMPK2) 在原发性肿瘤中上调(图 5I)。KSEA 显示 LNM 和原发性肿瘤中多种激酶发生激活(图 5J)。 GSEA分析显示,WNT信号在LNM中增强,WNT相关蛋白和磷酸化位点在LNM中上调,而非经典WNT蛋白和磷酸化位点在原发性肿瘤中高表达。GSK3B在原发性ESCC中表达上调;然而,其激酶活性在LNM肿瘤中减弱,这可能导致CTNNB1稳定,进而激活经典WNT通路。这些发现表明,在原发性ESCC中靶向GSK3B,在LNM中靶向CTNNB1是潜在的治疗策略(图5K)。
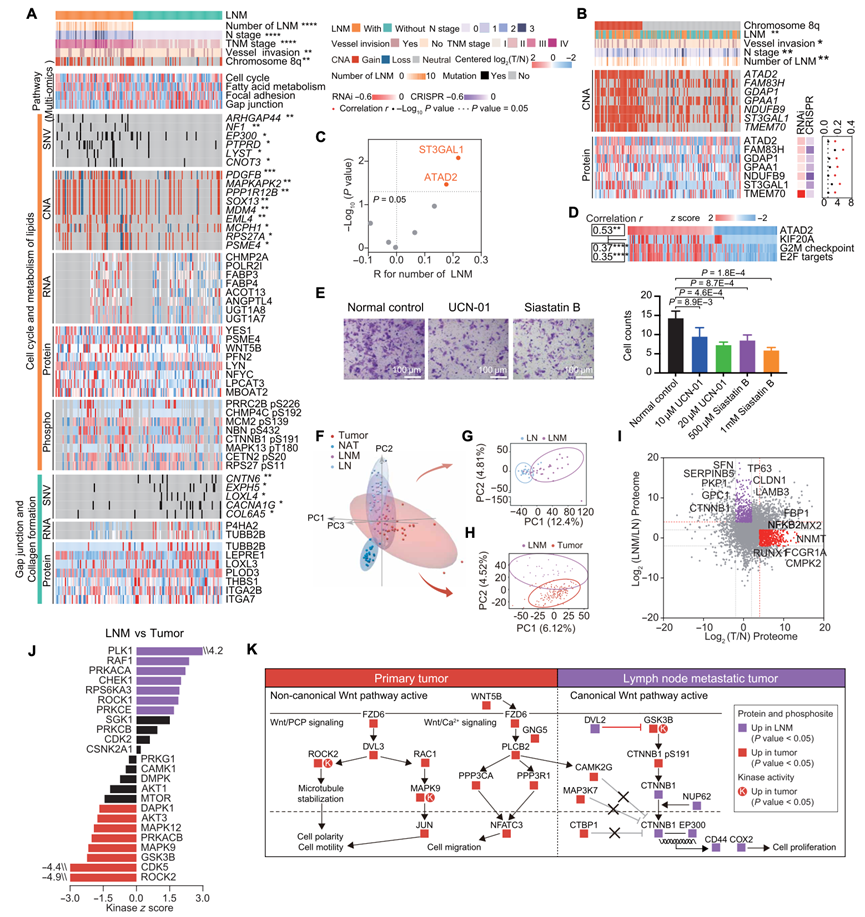
图5. 伴有淋巴结转移的 ESCC 中的多组学改变。
(A) 显示有或无 LNM 的 ESCC 的多组学图谱,突出显示关键通路和基因改变。(B) 8q 染色体增益相关基因和生存分析。(C) 火山图显示 8q 染色体增益相关基因与 LNM 之间的(双侧)Spearman 相关性。(D) 热图显示驱动蛋白家族成员 20A (KIF20A) 和 ATAD2 与细胞周期相关通路活性之间的(双侧)Spearman 相关性。(E) Transwell 测定(左)和柱状图(右)显示治疗组中的细胞计数。(F) 肿瘤、NAT、LNM和 LN的 PCA。(G) LN和 LNM的 PCA。(H) LNM和肿瘤的 PCA。(I) 散点图显示原发性肿瘤和 LNM 之间的 DEP。(J) 激酶活性分析。(K) 原发性肿瘤和 LNM 的多组学特征总结。
06
ESCC免疫浸润的特征
PD-1 配体 1 (PD-L1) 和 PD-1 抗体已获批用于 ESCC 治疗,但可靠的疗效预测因子(例如 PD-L1 表达和免疫背景)仍不清楚且未得到充分验证。为了探索 ESCC 中的免疫浸润,他们基于 289 个肿瘤的蛋白质组学数据,使用 xCell进行了细胞类型反卷积分析。他们鉴定出五个主要免疫聚类(xCell 聚类),它们具有独特的免疫和临床特征。虽然免疫聚类与结果不相关,但它们与临床变量相关,分别称为聚类1(冷肿瘤,侵袭性,晚期 T 分期),聚类2(上皮样肿瘤,角质形成细胞评分高),聚类3(肌源性肿瘤,神经周围侵犯),聚类 4(T 细胞耗竭肿瘤,基质评分高)和聚类5 [热肿瘤,分化差,主要组织相容性复合体 (MHC) 和 T 细胞活化高](图 6A-B)。可以通过血小板和 CD8 +中央记忆 T 细胞(Tcm细胞)的特征来区分。聚类 5 具有最高的 CD8+ Tcm细胞评分,代表肿瘤微环境的免疫能力。同时,聚类 1 具有最低的 CD8 + Tcm细胞评分。
与其他聚类相比,聚类1肿瘤的晚期T期和全肌层浸润比例更高(图6C-D)。蛋白质表达分析显示,聚类1富含ECM组织相关蛋白,尤其是基质金属蛋白酶(MMP)和整合素(图6E),它们是肿瘤生长、转移和浸润的关键驱动因素。同样,全肌层浸润的肿瘤也表现出ECM相关蛋白表达升高,CD8+幼稚T细胞特征增加,内皮细胞特征减少,这些特征在肿瘤发生和转移中均有明确作用。
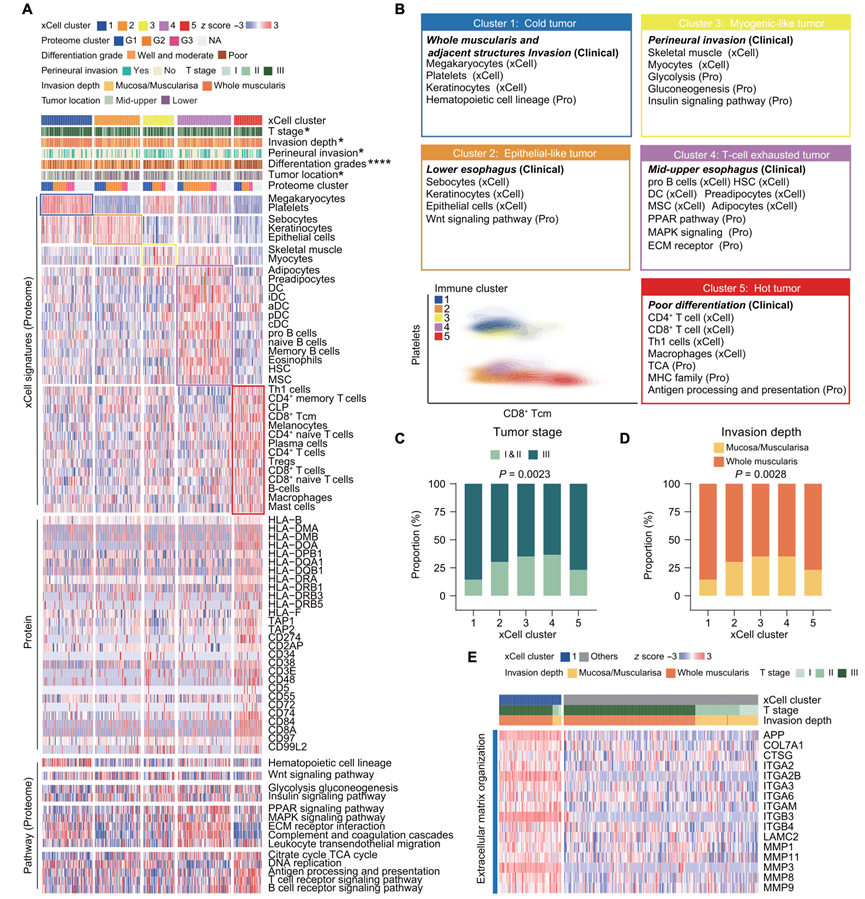
图6. ESCC 中的免疫景观。
(A) 热图显示了 289 名 ESCC 患者在五个蛋白质组学 xCell 聚类中的肿瘤组织的多组学谱。(B) 具有临床和遗传特征的聚类的血小板和 CD8+ Tcm细胞评分的密度图。(C) 直方图显示了五个 xCell 聚类中不同 T 分期的样本比例。(D) 直方图显示了五个 xCell 聚类中侵袭深度的分布。(E) 热图显示了聚类1 和其他四个聚类中 ECM 相关蛋白的表达。
07
LD 形成是 ESCC 治疗的潜在目标
PLIN2 是一种 LD 膜蛋白,参与 LD 结构和脂质储存,已知在维持胚胎干细胞的干性方面发挥作用。在本研究中,PLIN2 在晚期 ESCC 中过度表达,在 G3 组达到峰值,其特征是生存结果较差。在人类样本中,与 NAT 相比,在肿瘤组织中观察到 LD 和高 PLIN2 表达(图 7A-C)。为了验证 PLIN2 在 ESCC 进展中的作用,用 IHC 染色和 H 评分分析了另外 328 个 ESCC 样本,将 PLIN2 表达分为四组(PLIN2 阴性、低、中和高组)。高 PLIN2 含量与较差的 OS 相关。载脂蛋白E (APOE) 是一种参与脂蛋白清除和脂质代谢的载脂蛋白,它促进LD的积累和形成,在胆固醇稳态和细胞分化等细胞过程中发挥作用。本研究中,与NAT相比,APOE在ESCC肿瘤组织中表达过高,且与预后不良相关 (图7 B-C)。
PLIN2 和 APOE 协同调节 LD 的大小和数量,从而增强胆固醇的储存和甘油三酯的分泌。在本研究中,PLIN2和APOE的联合过表达与不良预后相关,表明它们在 ESCC 进展中具有潜在的叠加效应。为了证实 PLIN2 和 APOE 在 ESCC 进展中的潜在联合作用,他们使用人类肿瘤样本、ESCC 细胞系、类器官模型和异种移植模型进行了蛋白质组学分析、代谢组学分析和功能测定,构建了敲低或过表达PLIN2和APOE的 ESCC 细胞(TE1 和 KYSE170)。ESCC细胞系中PLIN2和APOE的过表达(PLIN2 OE、APOEOE和PLIN2OE APOE OE)导致脂质代谢发生改变,脂质相关蛋白增加,特别是参与 FA 和固醇脂质形成的蛋白。敲低任一基因都会抑制 ESCC 细胞增殖、迁移、肿瘤生长和 LD 形成,而其过表达则会促进这些表型,其中双重过表达组表现出最高的 LD 量(图 7D-G)。代谢组学分析显示PLIN2OEAPOE OE组脂质代谢发生特定改变,包括 FA 和固醇脂质含量升高,而它们是 LD 的关键成分。PLIN2和APOE的共同过表达增强了这些脂质种类的积累。
二酰甘油O-酰基转移酶 (DGAT) 是甘油三酯合成和 LD 生物合成中的关键酶。DGAT 抑制剂可以破坏 TG 和 FA 的合成和储存,从而减少 LD 形成。DGAT1/2 活性的抑制会损害 LD 的形成,其证据是 FA 和固醇脂质的数量减少,并且与未接受 DGAT1/2 抑制剂治疗的组相比,ESCC 细胞的增殖和克隆形成能力显著减弱(图 7H)。源自人体组织的类器官模型提供了稳定且灵活的培养物,可以忠实地复制原代组织特性,包括异质性,这使其对于研究癌症治疗非常有价值。为了进一步验证 PLIN2 和 APOE 在 ESCC 中的作用,他们从两例 PLIN2 和 APOE 表达较低的 ESCC 患者身上提取了类器官。PLIN2 、APOE及其组合(PLIN2OE、APOE OE和PLIN2 OE APOE OE)的过表达实验表明,与对照组相比,LD 形成和类器官克隆增殖增加,其中共同过表达组表现出最显著的效果(图7I)。相反,在 PLIN2 和 APOE 高表达的类器官中进行敲低实验(sh-PLIN2和sh-APOE)表明,与对照组相比,LD 形成和克隆数量减少(图 7I)。此外,PLIN2和APOE的联合敲低导致类器官克隆数量进一步减少(图 7I)。
此外,小鼠异种移植实验表明,敲低PLIN2和APOE可导致肿瘤生长减缓,而同时敲低这两种蛋白则进一步阻碍肿瘤进展,凸显了它们在促进 ESCC 恶性肿瘤方面的附加功能(图 7J-K)。顺铂是晚期 ESCC 的主要治疗方法,它会破坏癌细胞 DNA,但也会损害免疫细胞,从而降低免疫浸润和化疗效果。接下来,他们用不同浓度的顺铂或与 DGAT1/2 抑制剂联合处理 ESCC 细胞(TE1 和 KYSE270),以测试在此背景下的 LD 调节。通过 DGAT1/2 抑制剂联合顺铂治疗抑制 LD 形成可显著增强 ESCC 细胞的化学敏感性(图 7L-M)。
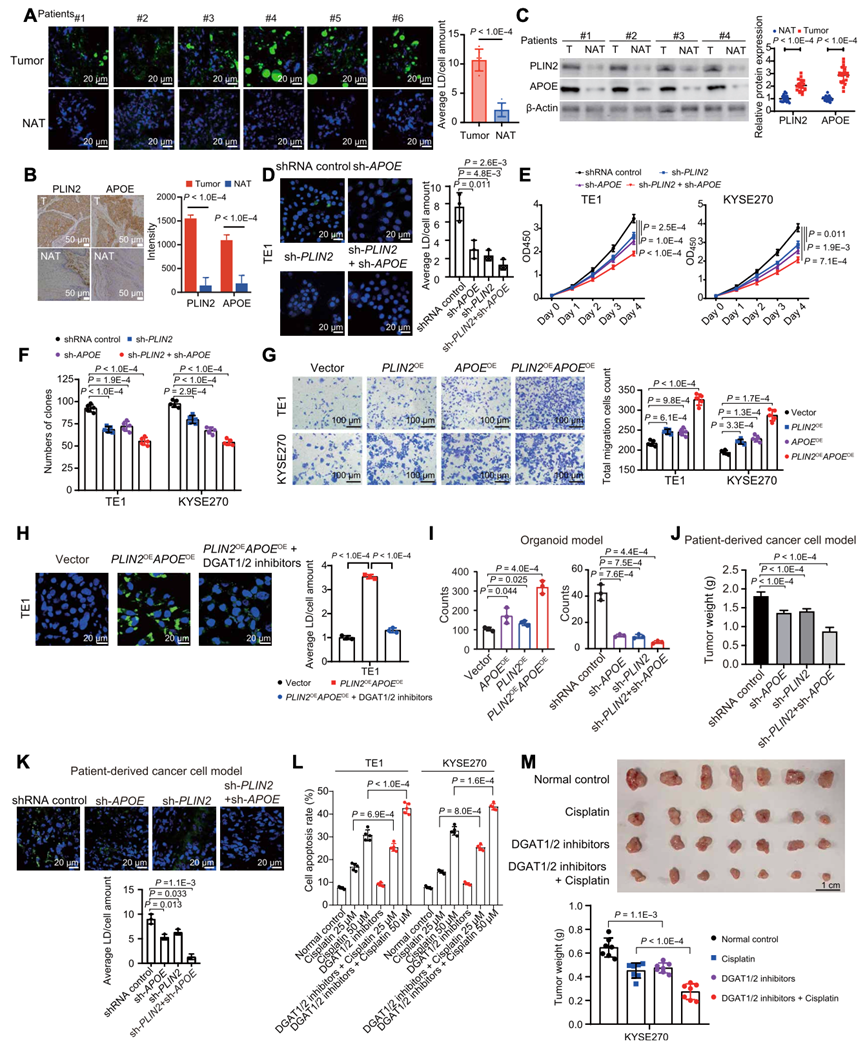
图7. LD 形成是 ESCC 的潜在靶标。
(A) 荧光染色(左)和柱状图(右)显示 ESCC 患者肿瘤组织和匹配 NAT中的 LD 量。(B) IHC 染色(左)和柱状图(右)显示 ESCC 患者的肿瘤组织和匹配 NAT中 PLIN2 和 APOE 的蛋白质表达。(C) Western blot 和箱线图(右)显示 ESCC 患者的 20 对肿瘤和匹配 NAT 中 PLIN2 和 APOE 的蛋白质表达量。(D) 荧光染色(左)和柱状图(右)显示了PLIN2和APOE敲低后 TE1 ESCC 细胞中的 LD 量。(E) 在 OD450(450 nm 处的光密度)波长下进行 CCK-8 分析显示PLIN2和APOE敲低组中的 ESCC 细胞增殖(TE1 和 KYSE270)。(F) 柱状图显示PLIN2和APOE敲低后 ESCC 细胞(TE1 和 KYSE270)中的克隆形成能力。(G) Transwell 实验(左)和柱状图(右)显示PLIN2和APOE过表达组中 ESCC 细胞(TE1 和 KYSE270)的迁移。(H) 荧光染色(左)和柱状图(右)显示PLIN2和APOE过表达后 TE1 细胞中的 LD 量。(I) 类器官克隆形成能力分析。(J) 柱状图显示在PLIN2和APOE敲低后患者来源的癌细胞模型的肿瘤重量。(K) 荧光染色(上)和柱状图(下)显示PLIN2和APOE敲低后患者来源的癌细胞模型中的 LD 量。(L) 柱状图显示顺铂处理后 ESCC 细胞(TE1 和 KYSE270)的凋亡率。(M) 图像(上)和柱状图(下)显示用 DMSO、顺铂、DGAT 抑制剂或顺铂和 DGAT 抑制剂组合处理的 KYSE270 细胞异种移植模型的肿瘤重量
08
PLIN2 或 APOE 表达调节 ESCC 的免疫环境
为了评估 PLIN2 和 APOE 对 T 细胞失活的影响,他们将 Jurkat 细胞与PLIN2和APOE过表达后的 ESCC 细胞系(TE1 和 KYSE270)共培养,并给予或不给予 DAGT1/2 抑制剂处理,这些细胞可分成四个实验组:PLIN2OE、APOEOE、PLIN2OE APOEOE和 DAGT1/2 抑制剂处理。此外,用空载体转染的细胞作为对照(载体组)。结果显示,PLIN2和APOE过表达组的 Jurkat 细胞数量和迁移增强,而 LD 抑制剂可降低这些(图 8A),表明 LD 依赖性 T 细胞募集。流式细胞分析显示,与载体组相比,PLIN2 和 APOE 过表达组的 Jurkat 细胞活化降低。DGAT1/2 抑制剂可减轻这些影响(图 8B)。
TE1 细胞中PLIN2和APOE过表达导致 ECM 相关蛋白(黏着斑和黏着连接)增加,表明食管鳞状细胞癌 (ESCC) 中的基质化增强和免疫抑制。使用 xCell web分析,他们发现 TE1 细胞过表达组中基质浸润显著增强(PLIN2OE、APOE OE和PLIN2 OE APOE OE)(图 8C)。
在本研究中,PLIN2 和 APOE 的表达可以增强 FA 和固醇脂质的表达量,表明它们在 T 细胞抑制中的作用。将 FA 和固醇脂质添加到与PLIN2OE APOE OE ESCC 细胞(TE1 和 KYSE270)共培养的 Jurkat 细胞中。流式细胞分析结果显示,与载体组相比,这些 LD 相关代谢物(FA 和固醇脂质)抑制了 Jurkat 细胞活化,这表现为标志物表达,而这种作用可以由 DGAT1/2 抑制剂逆转(图 8B)。蛋白质组学分析进一步显示,过表达组(PLIN2OE、APOEOE和PLIN2OE APOEOE)的 T 细胞活化标志物减少,而 DGAT1/2 抑制剂也可以逆转这种现象(图 8D)。这些发现表明,PLIN2 和 APOE 增加了 FA 和固醇脂质并促进了 T 细胞募集,但提高了 ESCC 基质化并抑制了 T 细胞活化,这些都与免疫逃避和 ESCC 发展有关。
将PLIN2和APOE过表达的 ESCC 细胞与 Jurkat 细胞共培养可进一步增加 ESCC 细胞数量(图 8E)。此外,与单独过表达PLIN2和APOE 的ESCC 细胞相比,共培养中的 DNA 复制标记表达增加(图 8F)。为了研究 Jurkat 细胞分泌物是否促进 ESCC 增殖,他们对单独和与 Jurkat 细胞共培养的PLIN2和APOE过表达的 ESCC 细胞上清液样本进行了蛋白质组学分析。共培养结果显示生长因子相关蛋白增加,包括胰岛素样生长因子 1 受体 (IGF1R) 和 IGF 结合蛋白 2 (IGFBP2)(图 8G)。为了进一步验证这些生长因子相关蛋白在 ESCC 细胞增殖中的作用,他们用 IGF1 处理PLIN2和APOE过表达的 ESCC 细胞,CCK-8 检测结果显示,IGF1 处理促进了细胞增殖,与共培养结果相当(图 8E-F)。
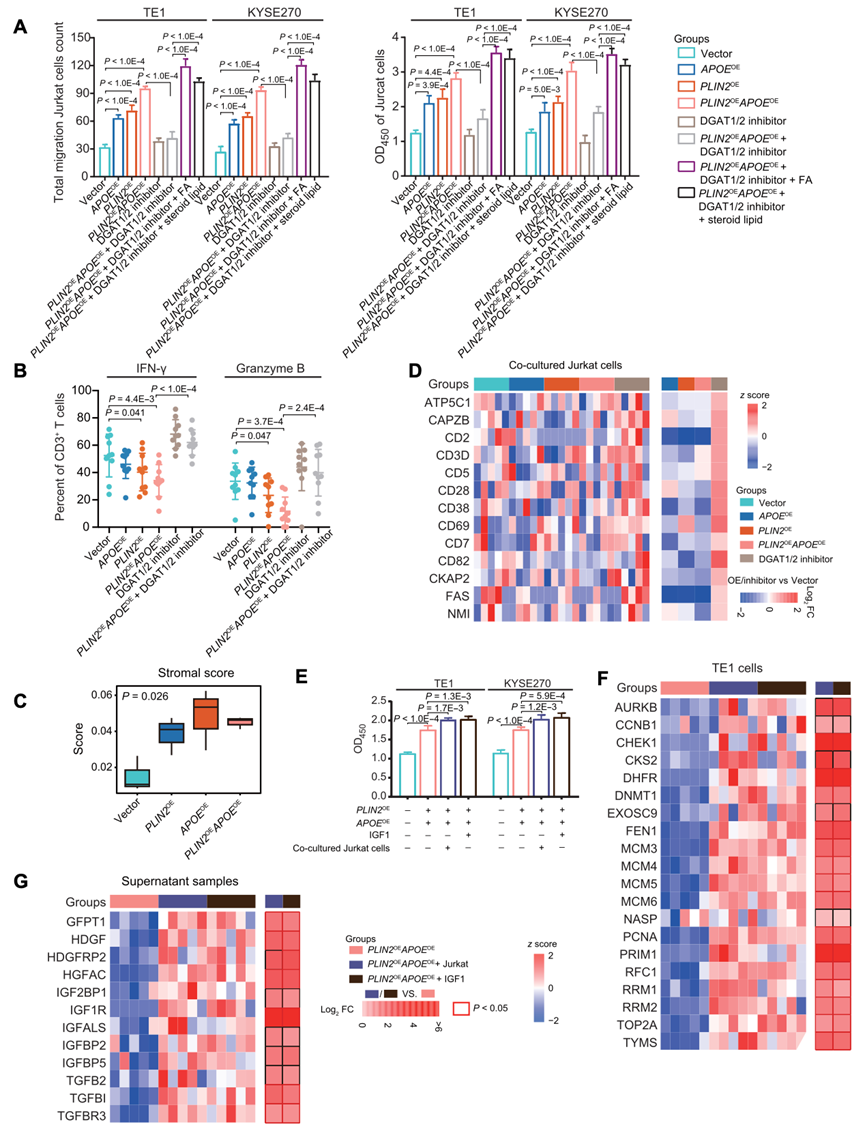
图8. LD形成对免疫浸润的影响。
(A) 柱状图显示迁移的 Jurkat 细胞数量(左)和 OD450波长下 CCK-8 检测的细胞增殖情况(右)。(B) CD3+ T细胞百分比。(C) 箱线图显示PLIN2和APOE过表达后TE1细胞的基质评分。(D) T细胞相关标志物的蛋白表达量。(E) 柱状图显示通过CCK-8检测在OD450波长下对ESCC细胞(TE1和KYSE270)的增殖情况。(F) 热图显示TE1细胞中PLIN2和APOE过表达后。(G) 生长因子相关蛋白的表达量。
+ + + + + + + + + + +
结 论
本研究对293例ESCC患者的遗传学、转录组学、蛋白质组学和磷酸化蛋白质组学特征进行了全面的分析。染色体12q13.13扩增与ESCC组织中Janus激酶信号转导和转录激活因子通路以及角蛋白在蛋白质水平上的上调相关,并与高分化和中分化ESCC肿瘤患者的不良预后相关。低分化ESCC肿瘤患者的肿瘤微环境中存在活化T细胞浸润,提示其可能对免疫疗法有反应。染色体8q扩增与ESCC组织的淋巴结转移相关,其特征是WNT信号从非经典信号向经典信号的转变。蛋白质组学分类显示,预后最差的亚组在ESCC组织中存在染色体2p扩增,且在蛋白质水平上存在脂质代谢上调。围脂滴蛋白脂蛋白2和载脂蛋白E诱导的脂滴形成促进细胞因子分泌,进而募集T细胞并增强基质形成,从而抑制T细胞活化并促进ESCC恶性进展。
+ + + + +



 English
English


