文献解读|Mol Cancer(33.5):定量蛋白质组学分析揭示了VARS1通过调控MAGI1表达在肝细胞癌侵袭性中发挥的关键作用
✦ +
+
论文ID
原名:Quantitative proteomic analysis unveils a critical role of VARS1 in hepatocellular carcinoma aggressiveness through the modulation of MAGI1 expression
译名:定量蛋白质组学分析揭示了VARS1通过调控MAGI1表达在肝细胞癌侵袭性中发挥的关键作用
期刊:Molecular Cancer
影响因子:33.5
发表时间:2025.01.14
DOI号:10.1186/s12943-024-02206-5
背 景
肝细胞癌(HCC)是最常见的肝癌类型。HCC的发生发展主要与潜在的慢性肝病有关,例如乙型肝炎病毒(HBV)或丙型肝炎病毒(HCV)感染、过量饮酒或代谢功能障碍相关性脂肪肝(MASLD)。尽管HBV/HCV相关HCC的发病率最高,但MASLD相关HCC的病例增长速度超过其他病因,预计在未来几年将成为HCC的主要病因。本研究旨在通过对一组特征明确、病因均衡的HCC患者队列的亚细胞分级肝脏样本进行非靶向定量蛋白质组学分析,深入了解HCC的蛋白质组组成和动态变化。
实验设计
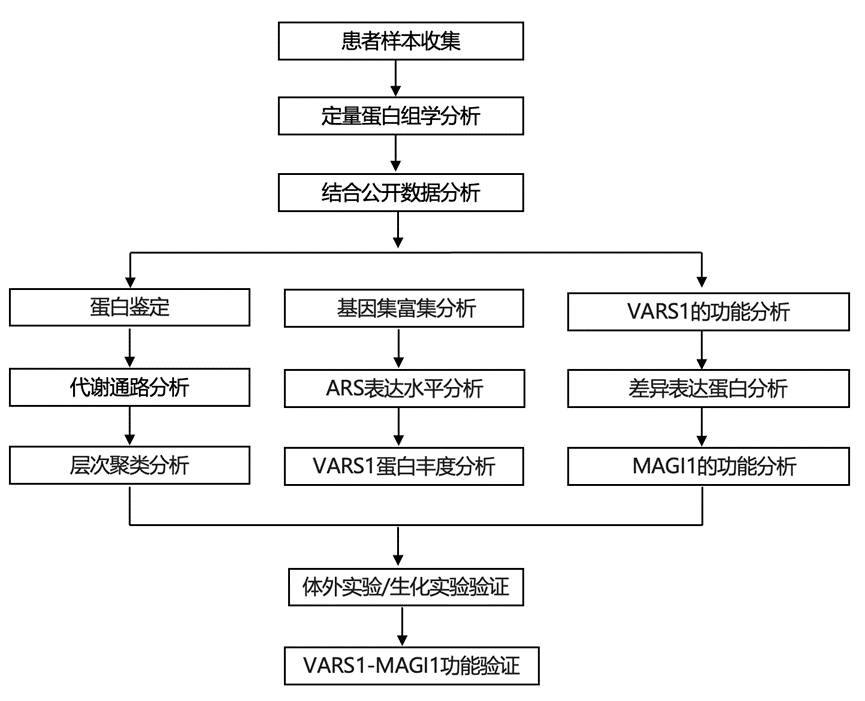
结 果
01
肝细胞癌细胞质和核组分的定量蛋白质组学分析
研究团队对来自 42 例肝细胞癌 (HCC) 患者和 5 例健康肝组织的肿瘤组织 (T) 和癌旁正常组织 (NTAT) 的胞质和核组分进行定量蛋白质组学分析 (SWATH-MS)(图 1A)。结果在胞质组分中鉴定出 1532 种蛋白质,在核中鉴定出 2102 种蛋白质;其中 313 种蛋白质在两个组分中均有表达(图 1B )。通过免疫印迹法,使用组分特异性标记物(NTAT)验证了亚细胞组分分离。通过非监督层次聚类分析,NTAT的蛋白质与健康肝组织的蛋白质相当,因为没有观察到差异聚类,因此表明 NTAT 代表了 NTAT 与肿瘤配对比较的可靠、健康的对照。相比之下,HCC样本的蛋白质组与NTAT样本相比发生了显著改变,其中524种蛋白质(34.2%) 在胞质组分中的丰度 存在显著差异( p < 0.05),1013种蛋白质(48.2%)在核组分中的丰度存在显著差异(图1 B-C)。主成分分析(PCA)进一步证实了HCC蛋白质组的显著失调,基于核蛋白质组,HCC样本与NTAT样本之间存在明显差异,且胞质蛋白质组的变异性更高。
胞质HCC蛋白质组的特征是代谢通路(碳水化合物、脂质和氨基酸代谢)的改变,以及细胞运动(整合素信号通路改变)和mRNA/蛋白质代谢[无义介导衰变(NMD)、蛋白质折叠]的改变(图 1D)。使用IPA软件(该软件可预测细胞通路的激活/抑制)进行的进一步分析证实了LXR/RXR信号通路的激活和外源性物质代谢的普遍失活。核HCC蛋白质组的特征是基因表达过程(RNA聚合酶、转录终止)、RNA代谢(mRNA剪接、tRNA氨酰化)、蛋白质稳态相关细胞功能[未折叠蛋白反应(UPR)、IRE1α和Xbp1信号通路]以及线粒体损伤相关通路的改变(图 1E)。在这种情况下,IPA 分析显示剪接体和 sirtuin 信号传导激活,同时氧化磷酸化和降解过程失活。
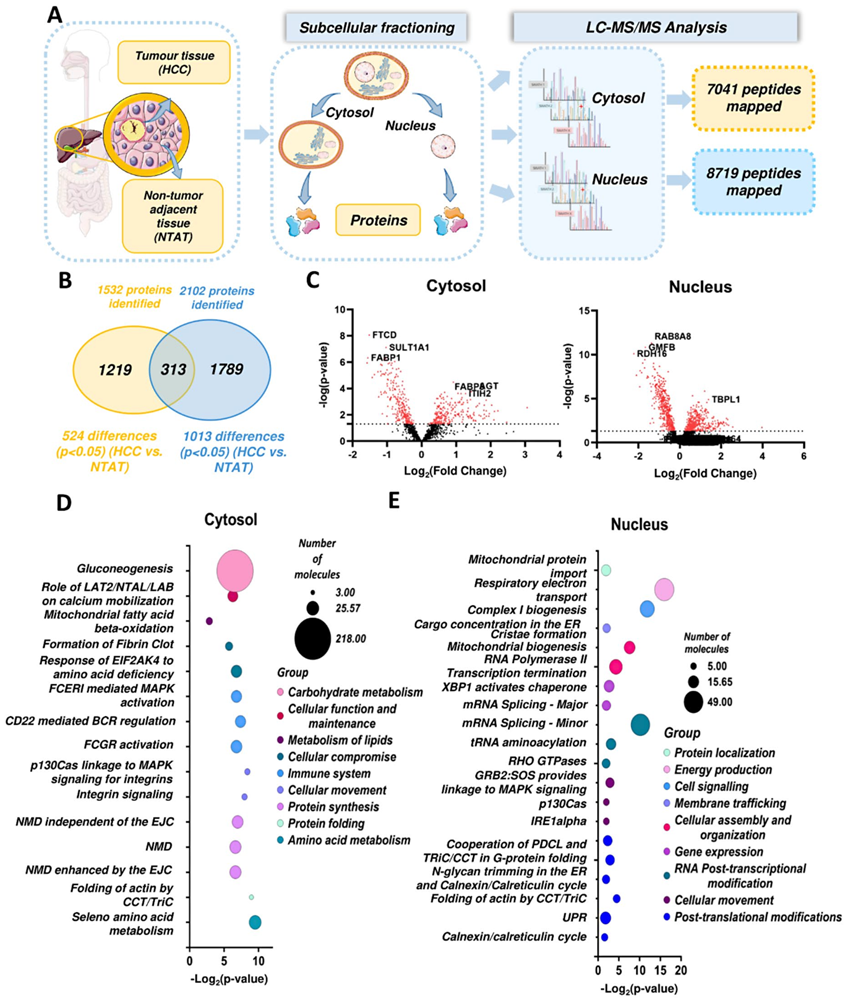
图1. 肝细胞癌(HCC)组织的定量蛋白质组学表征。
(A) 定量蛋白质组学样品制备示意图。(B) Venn 图显示了胞质(黄色)和核(蓝色)组分中鉴定的蛋白质数量,以及每个组分中差异表达蛋白质的数量。(C) 火山图表示 HCC 与 NTAT的差异。(D) 差异表达蛋白的富集分析。
02
胞质和核蛋白质组学特征定义了预后相关的肝细胞癌亚型
为了探究基于胞质或核蛋白质组特征的HCC亚型是否存在,他们对HCC和NTAT样本进行了无监督层次聚类分析。结果显示,胞质和核蛋白质组均定义了两个HCC亚组(PR1和PR2),这两个亚组与NTAT样本明显不同(图 2A-B)。大多数患者在胞质和核蛋白质组特征分析中均归为同一亚组。PR1和PR2亚组具有特定的胞质和核蛋白聚类,并以此进行分子表征。具体而言,PR1样本的胞质蛋白质组富含Cyto3聚类蛋白,核蛋白质组富含Nuc2聚类蛋白,这些蛋白均与急性期反应、LXR和FXR信号通路相关,这与部分保留肝脏特征的亚组相符。另一方面,PR2样本的特征是Cyto4和Nuc4聚类的过表达,这些聚类富集于EIF2、mTOR、剪接体或DNA修复等癌症相关通路,以及其他一些研究较少的通路,例如tRNA氨酰化。PR1和PR2亚组的患者也具有不同的临床特征。PR2亚组的患者预后更差(即肿瘤更大、生存期更短、复发率更高且去分化程度更高)。虽然PR1和PR2之间的病因分布没有统计学差异,但所有MASLD来源的HCC患者均纳入PR2。因此,蛋白质组学上的PR1亚组可能与低侵袭性HCC相关,且肝功能保持良好,而PR2则代表一种高侵袭性/预后不良的HCC亚型。
这些蛋白质组定义的亚类与先前定义的HCC分子亚类相关,基因集富集分析(GSEA)比较了两个亚组的胞质和核蛋白质组,证实了这一点。具体而言,PR2胞质蛋白质组在定义Boyault G12和G3聚类的基因集中富集,而Chiang提出的CTNNB1亚组中下调的基因则获得了负的NES评分。类似地,PR2核蛋白质组在定义Boyault G3和Hoshida S2亚类的基因集中富集,而PR1核蛋白质组在未注释亚类的基因集中富集。因此,PR1与非增殖性HCC亚类具有共同特征,而PR2的分子特征与增殖性亚类相符。
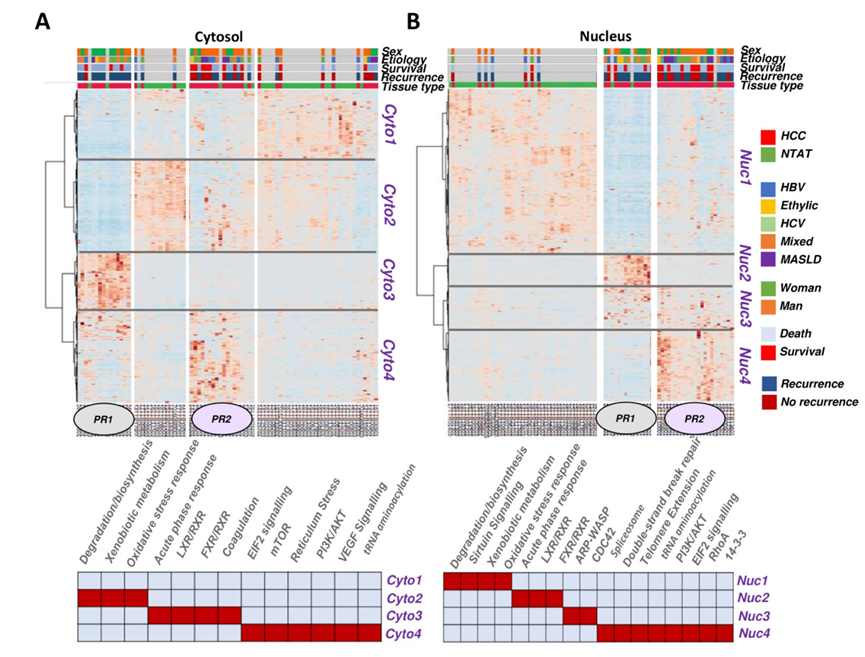
图2. 样本聚类分析识别出两个具有不同分子和临床特征的蛋白质组亚组。
根据(A)胞质和(B)核蛋白质组指纹图谱,对HCC和NTAT进行无监督聚类。
03
氨酰tRNA合成酶(ARS)在肝细胞癌中严重失调
转运RNA(tRNA)氨酰化是由氨酰tRNA合成酶(ARS)催化的关键生物学过程,在HCC中研究较少。与正常组织(NTAT)相比,HCC蛋白质组中tRNA氨酰化是最显著改变的特征之一;与增殖样亚类(PR2)相比,PR2蛋白质组中tRNA氨酰化的特征也最为显著。在检测到的17种ARS中,DARS1、EPRS1、NARS1和VARS1在HCC样本的胞质组分中表达上调。在核组分中,DARS1、FARSA、FARSB、NARS1、VARS1和WARS1表达上调,而EPRS1和RARS1表达下调(图 3A)。胞质组分中的VARS1和NARS1以及核组分中的FARSB在区分HCC和NTAT样本方面具有最高的鉴别能力(图 3A)。在其他已有的计算机模拟HCC队列中,进一步证实了ARS在HCC中的表达失调(图 3B)。在6个mRNA队列中的5个以及蛋白质队列(CPTAC-Zhou)中,VARS1和EPRS1均持续过表达;而NARS1、DARS1和FARSA在超过3个mRNA队列以及CPTAC-Zhou队列中过表达。此外,在4个队列中,VARS1是区分HCC与对照组能力最强的前3个基因之一(图 3C)。
根据ARS家族的表达水平(高、中、低表达),将患者分为三组(胞质和核蛋白质组学队列、TCGA-LIHC(mRNA)队列和CPTAC-Zhou(蛋白质)队列),并评估不同队列的临床特征,结果表明ARS家族的总体失调具有预后价值。胞质ARS丰度高的患者生存率显著降低,复发率显著升高(图 3E)。高ARS表达患者的分子指纹图谱富集Boyault G123基因集,而低ARS表达患者则富集Hoshida S3和Boyault G6亚聚类(图 3F)。核蛋白质组学分析、CPTAC-Zhou 蛋白队列和 TCGA-LIHC 队列也获得了类似的结果。TCGA-LIHC 队列还揭示了高 ARS 亚组与增殖性 HCC 亚类中常见突变基因(例如TP53、ARID1/A、TSC1/2)突变频率较高之间的关联。更深入的分子分析表明,高 ARS 亚组与蛋白质稳态[未折叠蛋白反应 (UPR)]、mRNA 代谢或运动通路改变相关。此外,典型的间质标志物(例如 YWHAZ、YWHAE、ACTN4 等)表达增加,而肝细胞标志物表达下调。在高ARS亚组中检测到了某些标志物(例如ALB、APOB、SERPINA1等)。这些结果证实了ARS家族在侵袭性/增殖性和未分化HCC样本中的上调。
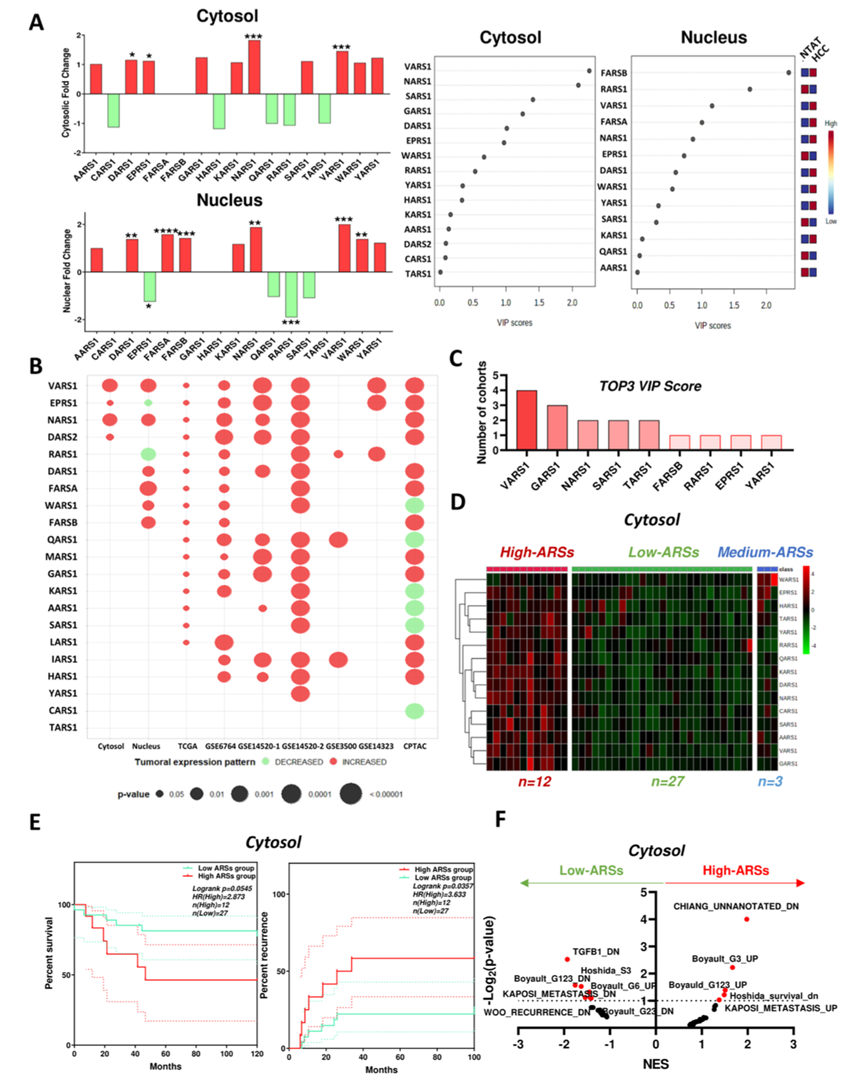
图3. 氨酰tRNA合成酶(ARS)在HCC中表达异常。
(A) 胞质和核蛋白质组学中ARS的丰度。(B) 气泡图显示9个HCC队列中HCC组织和对照组织之间ARS表达/丰度的变化。 (C) 柱状图显示了根据VIP评分结果,每个ARS均位列ARS家族中具有最高区分能力的前3名蛋白的队列数量(共分析了7个队列)。(D) 根据ARS家族的表达模式,对胞质蛋白质组队列进行K均值聚类。(E) 比较高ARS亚组和低ARS亚组之间死亡率和复发率的生存曲线和复发曲线。(F) 胞质蛋白质组队列中差异表达蛋白(高ARS亚组与低ARS亚组)的基因集富集分析(GSEA)结果。
04
缬氨酸-tRNA合成酶(VARS1)表达异常,且与肝细胞癌预后不良相关
基于这些结果,缬氨酸tRNA合成酶(VARS1)在肝细胞癌(HCC)中表现出最显著的改变。事实上,与正常组织相比,HCC样本的胞质和核组分中VARS1蛋白水平均上调,且这种上调在CPTAC蛋白队列和另外5个mRNA队列中得到证实(图 4A)。他们使用回顾性研究2队列(蛋白验证队列)中的部分样本,通过Western Blot实验证实了HCC中VARS1蛋白丰度的增加(图 4B)。值得注意的是,与原发肿瘤相比,HCC来源的肾上腺和肺转移灶中 VARS1的表达水平也更高(图4A)。此外,较高的VARS1胞质蛋白丰度与较大的肿瘤、微浸润和低分化程度显著相关;而较高的VARS1核蛋白丰度与门静脉高压显著相关。最后,在胞质蛋白质组学队列和计算机模拟 TCGA-LIHC 队列中,VARS1 高表达的患者均表现出较低的生存率和较高的复发率(图 4 C-D)。
通过在两种侵袭性不同的HCC细胞系中过表达(质粒)和沉默(两种siRNA)来评估VARS1的功能后果。VARS1过表达对Hep3B和SNU-387细胞的增殖或迁移没有显著影响,而VARS1沉默则轻微但显著地降低了两种细胞系的增殖和迁移。相反,VARS1过表达显著增加了肿瘤球的大小和克隆形成,而VARS1沉默则观察到相反的效果(图 4E),这表明VARS1在间质转化(EMT)和肿瘤形成中发挥着更重要的作用。事实上,VARS1沉默与上皮相关黏附分子(CDH2和ZO-1)的普遍上调以及 RAC-RHO 轴的下调相关,而干性/祖细胞标志物大多未发生改变。与此一致的是,VARS1过表达调节了一些 EMT 和干性/祖细胞标志物的表达,包括 Ras 同源物家族成员 A (RHOA) 和 B (RHOB)、MET 原癌基因以及 Thy-1 细胞表面抗原 (THY1)。
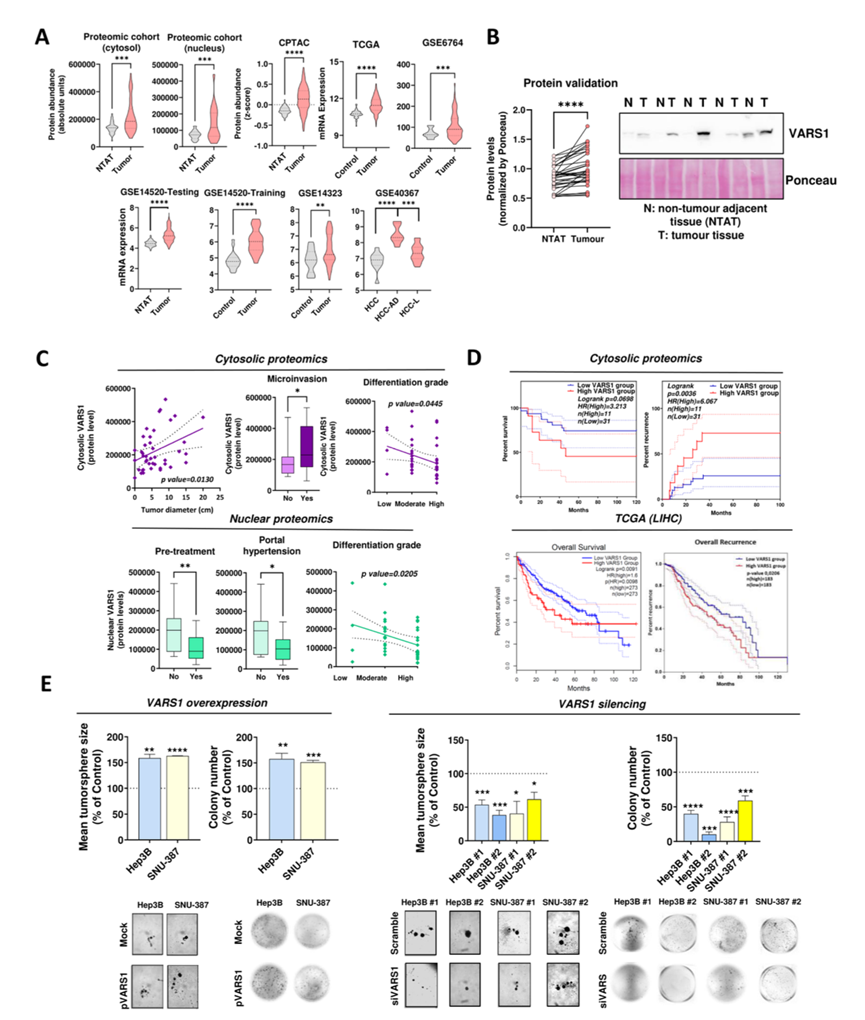
图4. VARS1在HCC中过表达,并与体外干细胞特性和肿瘤形成相关。
(A) 不同HCC队列中VARS1 mRNA/蛋白水平。(B) 蛋白验证队列中VARS1蛋白水平。(C) VARS1胞质(紫色)或核(绿色)水平与临床变量的相关性。(D) 胞质蛋白质组学队列和TCGA-LIHC队列中VARS1高表达组和VARS1低表达组患者(以中位数为界)的生存和复发曲线比较。(E) 在VARS1过表达(左)和VARS1沉默(右)细胞中进行克隆和肿瘤球形成实验。
05
VARS1过表达促进体内肿瘤的形成
VARS1参与肿瘤形成的作用已通过两种体内实验方法得到证实。首先,他们进行了体内极限稀释实验(ELDA),结果表明,在所测试的三种细胞浓度(100万、10万和1万个细胞/侧腹部)下,VARS1过表达细胞形成的皮下肿瘤均大于对照细胞(图 5 A-B)。当皮下注射较低浓度的细胞时,肿瘤体积/重量和肿瘤数量的差异更为显著,而此时对照细胞形成的肿瘤很小或没有肿瘤。其次,使用过表达VARS1和表达荧光素酶的 Hep3B 细胞建立了原位 HCC 模型,证实了在具有挑战性的条件下(注射亚最佳浓度的细胞),过表达VARS1 的细胞更容易启动肿瘤形成并促进肿瘤更快生长(图 5 C-D)。
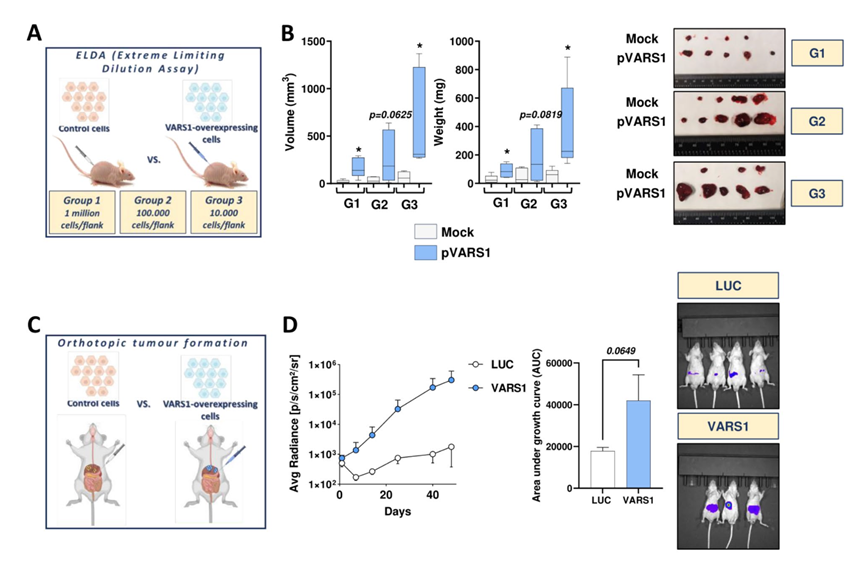
图5. VARS1过表达促进体内肿瘤的形成。
(A) 体内极限稀释法 (ELDA) 的示意图。(B) 使用VARS1过表达的 Hep3B 细胞进行体内 ELDA 实验。(C) 原位HCC模型的示意图。(D) 原位 HCC 模型,图中展示了对照组 (LUC) 和VARS1过表达组 (VARS1) Hep3B 细胞的肿瘤形成能力。
06
VARS1对肝细胞癌蛋白质组具有不依赖于缬氨酸的作用,并调节MAGI1的表达
为了进一步阐明VARS1过表达的分子后果,他们对过表达VARS1的Hep3B和SNU-387细胞系进行了非靶向定量蛋白质组学分析。原始数据见补充数据2C。VARS1过表达改变了Hep3B细胞中257种蛋白质的表达,改变了SNU-387细胞中348种蛋白质的表达(图 6A)。在两种细胞系中,这些变化均与常见的细胞过程相关,例如mRNA代谢、SUMO化和RHO GTP酶循环。有趣的是,还存在其他细胞系特异性改变,包括Hep3B细胞中凋亡调控蛋白的减少以及SNU-387细胞中炎症小体优势的转变(图 6B)。值得注意的是,VARS1过表达在两种细胞系中均诱导了20种共同蛋白质的改变。这些改变的蛋白质中,大多数的缬氨酸含量以中位数为中心,表明不存在对富含缬氨酸蛋白质的偏好。此外,与TCGA-LIHC队列的对照肝组织相比,HCC肿瘤中缬氨酸-tRNA(VARS1的底物)普遍下调,其中30个缬氨酸-tRNA中仅有5个与肿瘤组织中VARS1的表达呈显著负相关。这些数据表明,VARS1的过表达并未伴随将缬氨酸掺入新生蛋白质的tRNA表达的增加,提示VARS1在HCC中具有不依赖于缬氨酸的作用。
在这20种常见的改变蛋白中,MAGI1、EBNA1BP2、IDE和MFSD10在两种细胞系中均表现出一致的改变(表达上调或下调)(图 6C)。其中,MAGI1是HCC中的抑癌基因,其表达水平在三个不同的HCC队列中均与VARS1的表达呈负相关(图 6D)。体外实验表明,VARS1沉默可诱导MAGI1 mRNA和蛋白表达上调,而VARS1过表达则可诱导两种细胞系中MAGI1 mRNA和蛋白表达下调(图 6E-F)。
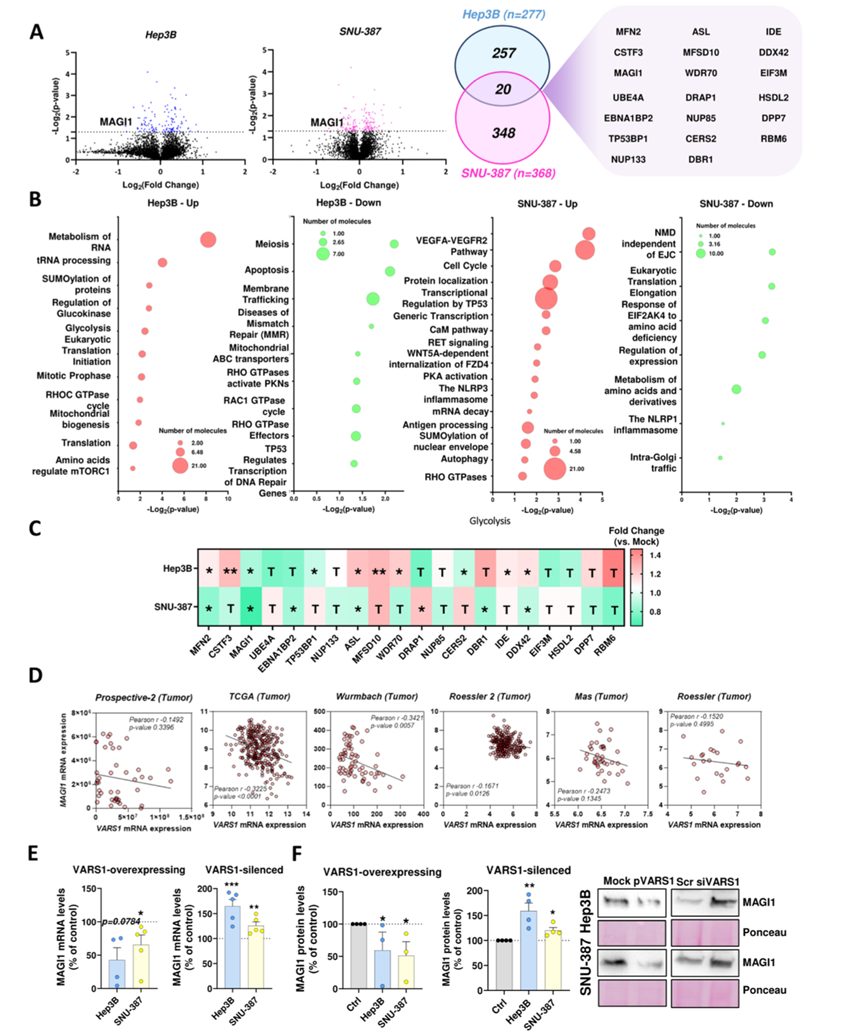
图6. VARS1过表达细胞系的定量蛋白质组学表征。
(A) 火山图表示VARS1过表达组与对照组的比较。(B) 对 Hep3B 和 SNU-387 VARS1过表达细胞中差异上调(红色)和下调(绿色)蛋白进行 Reactome 富集分析。(C) 热图展示了Hep3B(上图)和SNU-387(下图)细胞中20种常见VARS1调控蛋白丰度变化的幅度和显著性。(D) HCC患者中VARS1和MAGI1水平(mRNA)的相关性。(E) VARS1沉默和VARS1过表达细胞中MAGI1 mRNA的水平。 (F) 通过Western Blot检测VARS1沉默和VARS1过表达细胞中MAGI1蛋白的水平。
07
MAGI1在肝细胞癌中发挥抑癌基因的作用,并介导VARS1诱导的侵袭性增强
MAGI1 最初在HCC患者队列中发现,研究证实其在 HCC 样本中的表达显著低于对照组(图 7A)。在细胞系中过表达MAGI1可降低细胞增殖,尤其是在 SNU-387 细胞系中。此外,两种细胞模型中集落和肿瘤球的形成均减少了至少 50%(图 7B),这证实 MAGI1 也参与干细胞特性维持和肿瘤发生,正如 VARS1 所观察到的那样。为了评估MAGI1下调是否是VARS1促进侵袭性所必需的,他们进行了同时过表达VARS1和MAGI1的挽救实验(图 7C)。结果表明,在两种细胞系中, VARS1过表达诱导的克隆形成和肿瘤球形成均受到MAGI1过表达所抑制(图 7D),证实了VARS1过表达在HCC中的作用是通过MAGI1介导的。
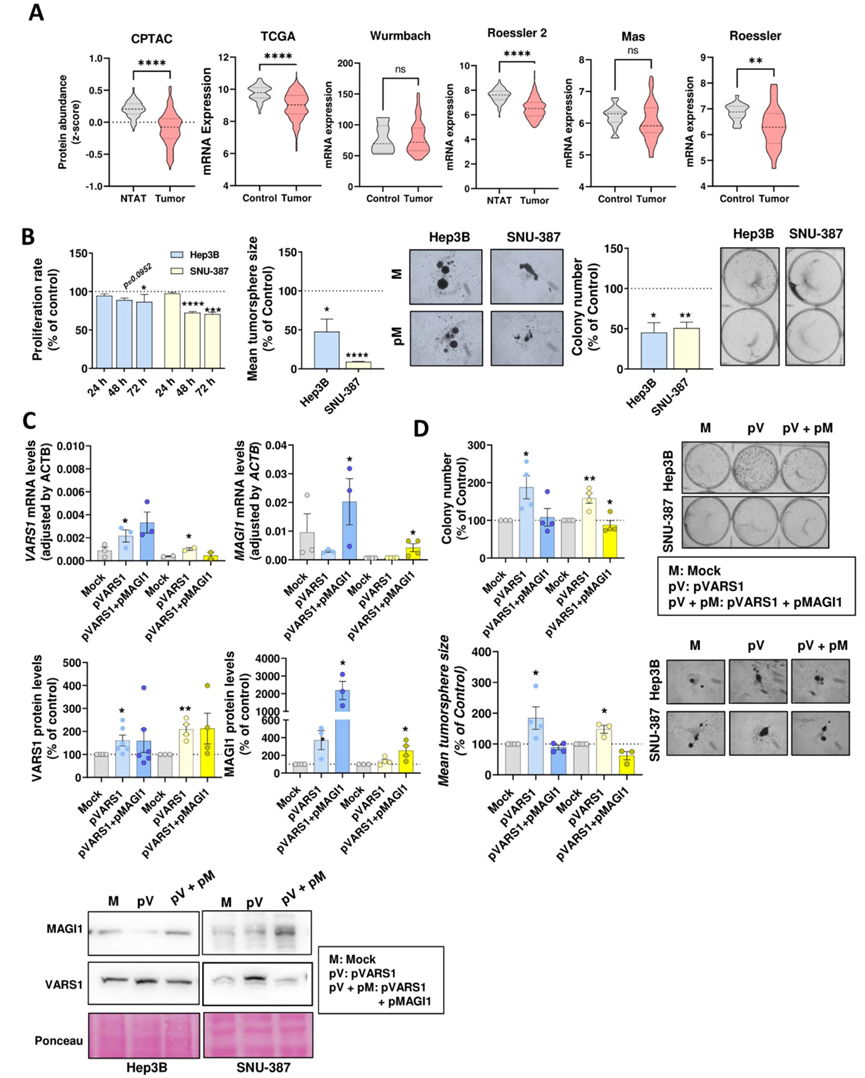
图7. VARS1 调控MAGI1表达以促进干细胞特性和肿瘤形成。
(A) HCC 队列中 MAGI1 的表达(mRNA 和蛋白水平)。(B) MAGI1 过表达后,Hep3B 和 SNU-387 细胞系的增殖、克隆形成和肿瘤球形成实验。(C) 验证 VARS1 单独过表达和 VARS1-MAGI1 同时过表达在细胞系中的表达水平(mRNA 和蛋白水平)。(D) VARS1过表达和VARS1-MAGI1同时过表达的 Hep3B(蓝色)和 SNU-387(黄色)细胞的克隆和肿瘤球形成实验。
+ + + + + + + + + + +
结 论
定量蛋白质组学揭示了HCC中胞质和核蛋白质组的失调,并定义了两个蛋白质组学HCC亚组,其中最具侵袭性的亚组与ARS的失调相关。计算机模拟的HCC队列证实了ARS的失调,且ARS失调与不良预后相关。ARS上调的患者具有增殖性HCC的基因组/转录组特征。VARS1是表达最稳定且与侵袭性相关的ARS。VARS1的调控(沉默/过表达)在体外和/或体内均改变了肿瘤建立相关的参数。对过表达VARS1 的细胞进行定量蛋白质组学分析和拯救实验发现,HCC 中的肿瘤抑制因子MAGI1的下调是 VARS1 功能的介质。
+ + + + +



 English
English


