通过双重免疫调节支架在时空上编程免疫-成骨
项目文章|通过双重免疫调节支架在时空上编程免疫-成骨
级联反应以实现功能性骨再生
2026年4月,《Bioactive Materials》(IF=20.3/Q1)在线发表由山东大学齐鲁第二医院来庆国教授、赵红宇老师完成的重磅研究成果“ Spatiotemporally programming the immune-osteogenic cascade with a dual-immunomodulatory scaffold for functional bone regeneration ”。这项研究为内源性骨修复提供了一种新的多细胞免疫调节策略。
开泰生物为本研究提供了单细胞转录组测序等关键技术服务,项目文章再+1!感谢每一位科研伙伴的信任与协作,开泰将继续努力,提供更优质的服务!


研究背景
临界尺寸骨缺损的功能性修复受到失控的炎症微环境的阻碍,这种环境破坏了内源性再生。传统的骨免疫调节生物材料主要强调直接调节巨噬细胞的表型转化,而忽略了在免疫-成骨级联调节中激活归巢间充质干细胞(MSCs)免疫调节功能的关键作用。在此,本研究提出了一种双重免疫调节骨支架(DIBS),通过时序调节巨噬细胞和MSCs的免疫功能来修复临界尺寸骨缺损,为内源性骨修复提供了一种新的多细胞免疫调节策略。
研究内容及结果
DIBS的制备与表征
为了实现免疫-成骨微环境的原位时序调节,DIBS采用双模块策略设计,具有刚性内层和柔软外层,以实现免疫调节剂和矿化离子的可控释放。DIBS的外层包含一个pH响应性免疫调节水凝胶模块。通过将相邻二醇部分氧化为醛基来合成氧化木葡聚糖(OXG),XG作为一种天然多糖,具有显著的抗炎特性和优异的生物相容性,可以在早期炎症过程中直接调节浸润巨噬细胞的表型和功能,赋予DIBS初始免疫调节能力。为进一步编程募集到缺损部位的MSCs的免疫调节能力,通过采用一步离子/分子组装过程的一锅法合成金属多酚(Sr-PA)纳米颗粒。
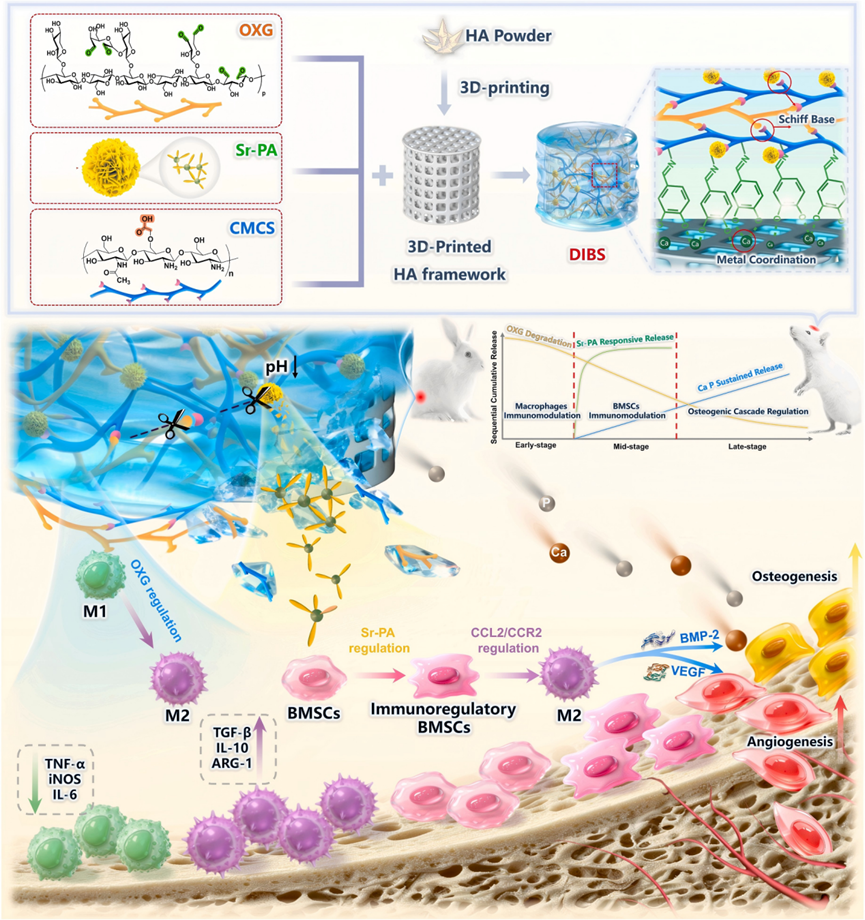
DIBS的设计
DIBS促进细胞募集、粘附和迁移
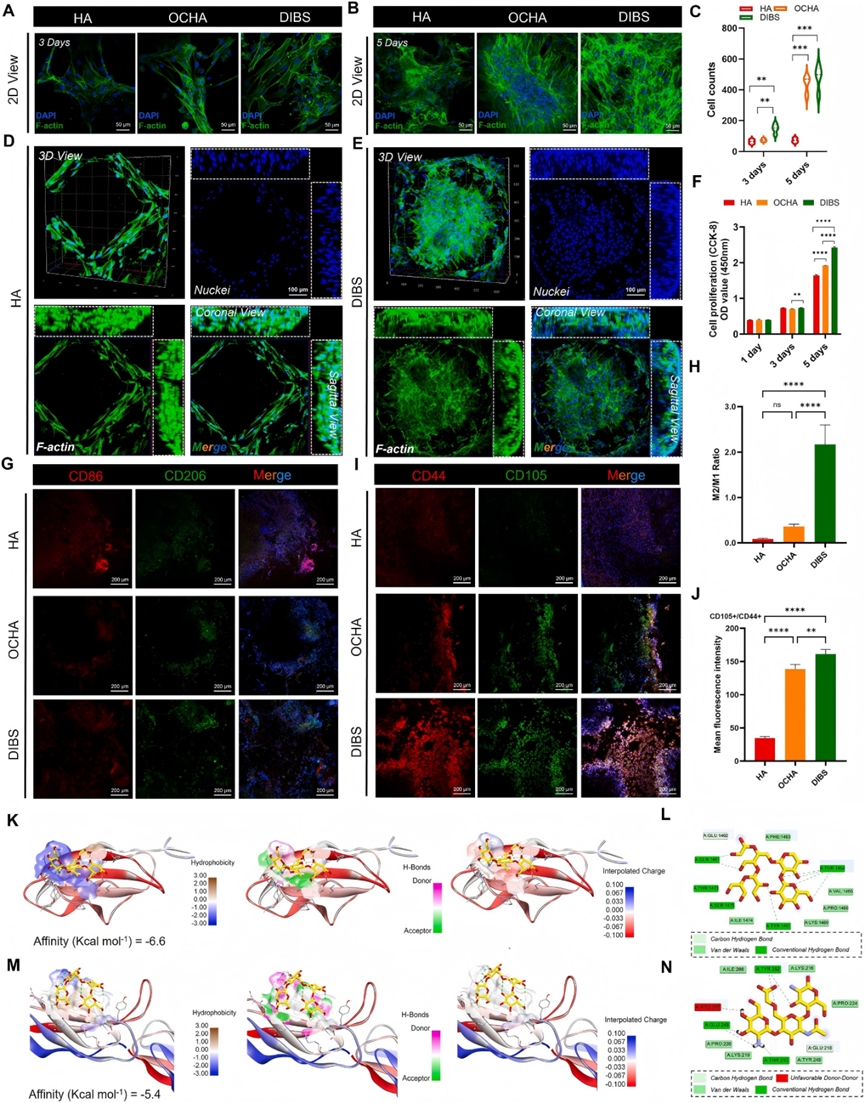
图3. DIBS的生物相容性及细胞反应
作为为微环境量身定制的免疫调节生态位,优异的生物相容性对于促进内源性干细胞/祖细胞的粘附和增殖至关重要。研究人员首先评估了支架对细胞活力和增殖能力的影响。细胞毒性结果显示细胞存活率超过100%,证实所有支架均无毒性。进一步全面评估了不同支架在不同共培养时间内促进BMSCs粘附和迁移到分级微孔结构中的能力。接种1天后,评估与细胞-基质相互作用相关蛋白vinculin的表达,结果显示,DIBS上的BMSCs表现出更集中于中心且拉长的富含vinculin的粘着斑。接种后第3天和第5天,对细胞骨架和细胞核染色的BMSCs的2D视图图像显示它们在所有支架上生长显著。到第3天,BMSCs已发育出纺锤形形态(图3A),与OCHA和HA组相比,DIBS组显示出显著更高的细胞数量(图3C)。5天后,BMSCs表现出更广泛的铺展和更高的细胞长宽比。与HA支架相比,OCHA和DIBS都支持最广泛的BMSCs覆盖面积和存活率(图3B-F)。BMSCs的3D视图显示,在HA支架的大孔内,细胞只能沿着陶瓷壁形成单层,通过细胞间连接向内迁移(图3D)。而在DIBS内部,分级水凝胶网络为细胞粘附和浸润提供了3D空间,细胞利用水凝胶纤维在陶瓷大孔结构中心实现悬浮的3D生长(图3E)。
为进一步评估DIBS的生物相容性及其在体内募集内源性细胞的能力,将无细胞支架植入8 mm大鼠颅骨缺损中。在生物材料初步引入后,会引发免疫反应,巨噬细胞是这一炎症级联反应的中心调节器。理想的骨组织工程支架(BTE)应具有调节巨噬细胞从促炎M1状态向抗炎M2状态转化的能力,从而促进最佳的骨再生。免疫荧光(IF)染色显示,与HA支架相比,植入一周后,OCHA和DIBS均促进了M2型巨噬细胞(CD206⁺细胞)的极化和浸润(图3G和H),显示出优异的免疫调节能力。
此外,在植入后两周也评估了内源性干细胞(ESCs,CD44⁺CD105⁺)的募集效率。IF染色显示,在DIBS内有显著的CD44⁺CD105⁺ ESCs募集。尽管缺乏生物活性PA和Sr²⁺,OCHA的分级物理结构也募集了相当数量的ESCs,而很少有ESCs迁移到HA支架中(图3I和J)。这种显著的募集效应可能归因于结构优势和Sr²⁺诱导的协同组合。有趣的是,体外和体内实验的结果一致表明,陶瓷大孔内的动态多糖水凝胶网络显著增强了MSCs的粘附。
DIBS通过直接调节巨噬细胞极化进行初始免疫调节
炎症调节在DIBS驱动的骨再生的初始阶段起着至关重要的作用,其中巨噬细胞从促炎M1表型及时转变为抗炎M2表型对于创造有利于组织再生的修复性免疫微环境至关重要。本研究中,在炎症早期评估了支架的抗炎特性(图4A)。首先,使用脂多糖(LPS)诱导巨噬细胞向M1表型极化,模拟初始炎症微环境。IF染色显示,与HA相比,DIBS和OCHA早在第3天就显著降低了M1型巨噬细胞(CD86⁺)的比例,并增加了M2型巨噬细胞(CD206⁺)。到第5天和第7天(图4B),M2主导的表型已完全建立。共培养7天后,IF(图4B)、WB和流式细胞术(图4D)分析结果显示DIBS显著诱导巨噬细胞向M2表型极化。而HA组大多数巨噬细胞主要向M1表型极化。在HA组中,巨噬细胞呈现出M1表型特征的圆形或阿米巴样形态,而在DIBS和OCHA组中,细胞呈现出M2巨噬细胞典型的细长、纺锤样形态(图4B)。
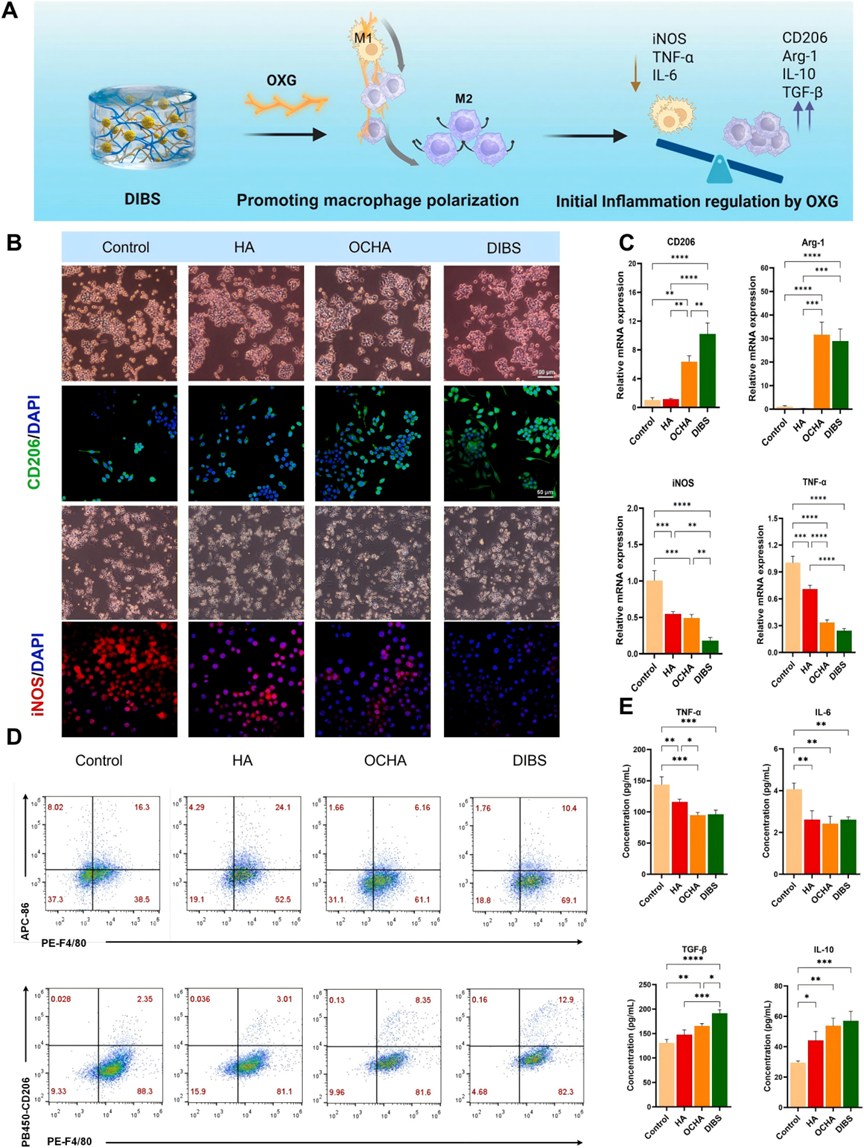
图4. DIBS对巨噬细胞极化的调控
此外,qRT-PCR定量结果证实,与HA组相比,OCHA和DIBS精氨酸酶1(Arg-1)和CD206表达显著上调,诱导型一氧化氮合酶(iNOS)和TNF-α表达下调(图4C)。酶联免疫吸附试验(ELISA)数据进一步证实了这一发现(图4E),显示OCHA和DIBS均减少了促炎细胞因子(TNF-α和IL-6)的分泌,同时增加了抗炎细胞因子(IL-10)和促骨/促血管生成生长因子(TGF-β)的分泌。
DIBS通过调节BMSCs向免疫调节表型重编程进行后续免疫调节
免疫微环境的时序调节对于临界尺寸骨缺损的功能性再生至关重要。初始炎症调节后,内源性MSCs被募集到缺损部位以介导随后的再生修复。鉴于MSCs的免疫调节功能在再生阶段调节巨噬细胞极化和维持免疫稳态中的关键作用,团队进一步研究了DIBS对BMSCs免疫调节功能的影响。
为获得在不同支架微环境中BMSCs的细胞异质性和转录重编程的无偏倚、高分辨率细胞图谱,共培养14天后,从支架中解离BMSCs进行单细胞RNA测序(scRNA-seq)(图5A)。数据处理和细胞质控后,共获得来自HA组的13,758个细胞、来自OCHA组的11,259个细胞和来自DIBS组的12,413个细胞用于进一步分析。通过Seurat流程对数据集进行归一化,并使用t-SNE可视化细胞异质性。无监督图聚类将细胞划分为11个不同的簇,根据标记基因表达和功能被分类为特定细胞类型(图5B-D):1)具有高表达CCL2、CCL7、CXCL1和CXCL3的免疫调节性BMSCs;2)具有高表达ccnpf、Mki67和Top2a的增殖性BMSCs;3)具有高表达Col1a1、Col12a1、Acta2和Sparc的成骨性BMSCs;4)具有高表达Mpg、Fos、Plac8、Spp1和Stc1的成骨祖细胞;5)具有高表达Fosb和Spp1的早期前成骨细胞;6)具有高表达Fosb、VEGFA和Spp1的前成骨细胞,与先前报道一致。与HA组相比,OCHA和DIBS组前成骨细胞比例显著更高(图5C)。这表明在复合支架上培养的BMSCs表现出更高成骨分化潜力的基因表达模式。值得注意的是,具有免疫调节基因表达谱的BMSCs簇主要在OCHA和DIBS组中被识别。该簇的特征是高表达免疫调节基因(Cxcl3、Cxcl6、CCL2、CCL20)。GO功能富集分析表明,该簇的功能主要与间充质细胞分化、干细胞增殖和骨发育、对趋化因子的细胞反应、趋化因子介导的信号通路以及血管生成有关。此外,单细胞轨迹分析进一步揭示,免疫调节性BMSCs位于细胞群体发育起点附近,表明它们可能有助于建立免疫再生微环境(图5E-G)。这些结果表明,在指导性生态位的调节下,BMSCs表现出多能性和异质性,并且免疫调节性BMSCs在免疫调节和干性方面具有更强的可塑性。
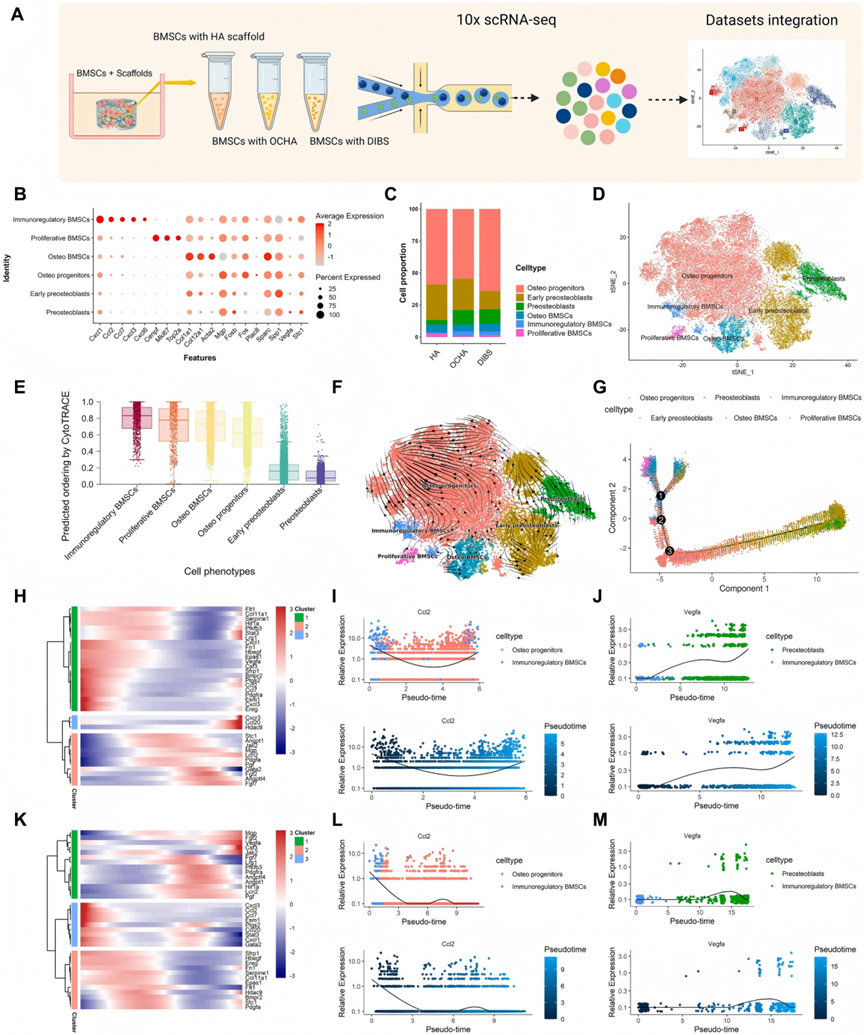
图5. 不同微环境中BMSCs单细胞转录组测序结果
进一步分析DIBS中最丰富的亚群——成骨祖细胞的功能特征。GO分析突出了在生物过程中的显著富集,如炎症反应的正向调节、肿瘤坏死因子产生的调节、过渡金属离子转运和线粒体组织的正向调节。这些过程与免疫调节、细胞代谢和离子运输密切相关,进一步强调了DIBS可以增强干细胞亚群的免疫调节能力和代谢活性。这归因于基于席夫碱键的动态水凝胶模块对酸性炎症微环境作出响应,在成骨分化过程中持续释放PA和Sr²⁺以增强BMSCs的免疫调节能力。接下来,我们分析了在DIBS中,从免疫调节性BMSC亚群向成骨祖细胞(图5H-K)或前成骨细胞亚群发育过程中差异表达基因的拟时序动力学。结果表明,与HA支架相比,大多数免疫调节相关基因(例如,趋化因子CCL2、Stat3)在DIBS中向成骨祖细胞亚群发育过程中表现出更高的表达水平(图5I-L)。这种增强的表达对于募集功能性修复细胞和建立免疫调节再生过程至关重要。相反,在向前成骨细胞亚群分化过程中,免疫调节基因表达下降,同时促血管生成基因(VEGF)表达激增(图5J-M)。这种免疫调节与促血管生成基因程序之间的动态转换可能在恢复临界尺寸骨缺损的级联再生潜力中发挥关键作用。
此外,基于scRNA-seq数据库,通过CellChat分析了HA和DIBS组中不同细胞亚群之间的相互作用。结果显示,DIBS中所有细胞亚群之间的相互作用显著更强(图6A)。值得注意的是,免疫调节性BMSCs与成骨祖细胞和早期前成骨细胞表现出最高数量和强度的配体/受体相互作用,表明具有分级结构的DIBS增强了细胞间通讯,从而促进了级联再生。此外,批量RNA测序结果显示,与HA支架相比,DIBS中的差异表达基因(DEGs)在伤口愈合、免疫调节、血管生成和骨再生方面显著富集。总之,单细胞转录组学揭示了在DIBS内培养的BMSCs中包括一个具有富集免疫调节基因表达谱的亚群。这一观察结果促使我们假设DIBS可能增强MSC介导的免疫调节。
DIBS通过CCR2依赖性方式介导CCL2诱导的巨噬细胞M2极化及成骨与血管生成
团队接下来研究了DIBS如何通过训练BMSCs的免疫调节功能来协调级联骨修复。KEGG通路富集分析进一步为上调的DEGs的功能角色提供了有价值的见解。与HA组相比,DIBS组中上调最显著的前几条富集通路如图6B所示,可分为三个部分:i)细胞能量代谢和分化的正向调节:碳代谢、糖酵解/糖异生和磷脂酰肌醇3-激酶/丝氨酸-苏氨酸激酶(PI3K-Akt)信号通路;ii)免疫相关事件:细胞因子-细胞因子受体相互作用、趋化因子信号通路和IL-17信号通路;以及iii)促进血管化和成骨:缺氧诱导因子-1(HIF-1)信号通路和矿物质吸收。这些上调的通路在免疫调节性BMSCs和成骨祖细胞等亚群中也分别显著富集。多个生物学过程在这些亚群之间协调,在指导性生态位内的再生修复过程中发挥关键作用。选定的关键通路的特定基因-通路相互作用网络和相关基因表达水平显示在图6C和D中。值得注意的是,CCL2作为一个关键的调节性生长因子,参与了包括趋化因子信号通路、细胞因子-细胞因子受体相互作用和IL-17信号通路在内的多个信号通路,似乎是启动通过驯化免疫调节功能进行内源性骨再生的核心介质。
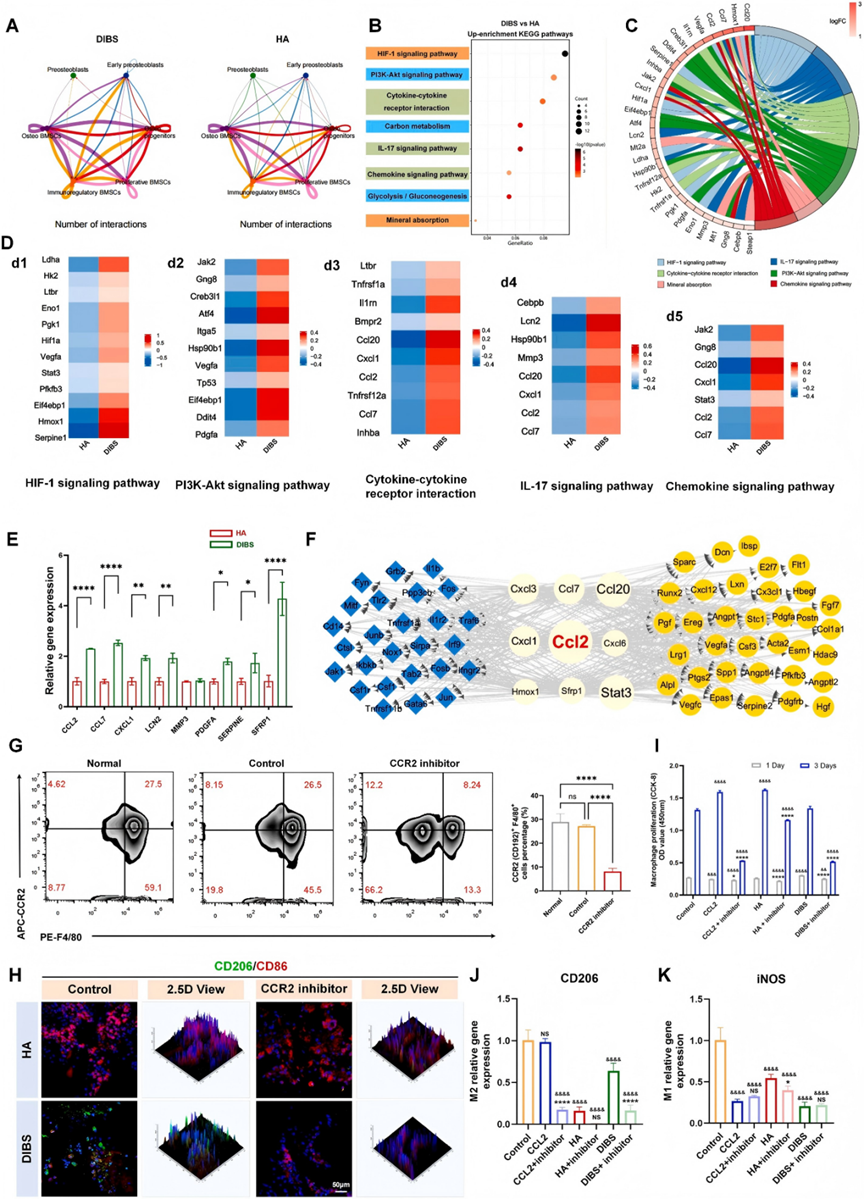
图6. 免疫调节与内源性骨再生机制
qRT-PCR验证参与这些通路的八个关键基因的表达,结果显示七个基因存在显著的组间差异,证实了转录组测序结果(图6E)。相互作用网络分析揭示了DIBS组中代表性免疫调节基因(CCL2、CCL7、Stat3等)与成骨/血管生成和巨噬细胞调节基因集之间存在强烈的相互作用(图6F)。进一步强调了趋化因子,特别是CCL2,是促进再生修复的关键免疫调节因子,而CCR2是CCL2的唯一受体。研究表明,CCL2/CCR2轴参与巨噬细胞增殖和M2表型激活,表明其在免疫调节诱导的内源性组织再生中的关键作用。为了在蛋白质水平上证实转录组学中的发现,研究人员对在不同支架上培养14天的BMSCs进行了CCL2免疫荧光染色。与scRNA-seq数据一致,与在HA或OCHA支架上培养的BMSCs相比,在DIBS上培养的BMSCs显示出显著更高的CCL2蛋白表达。因此,团队假设DIBS可能通过分泌趋化因子并与巨噬细胞串扰来介导随后的骨修复过程。
为进一步阐明ESCs和巨噬细胞之间CCL2/CCR2通路的调节机制,研究人员首先在CCR2抑制小鼠的肌内植入模型中研究了M2巨噬细胞的激活。RS504393是一种高选择性的CCR2趋化因子受体拮抗剂,在植入后的头7天(此后继续)通过每日腹腔注射给药,以抑制CCL2/CCR2信号传导。抑制7天后,外周血中CCR2⁺ F4/80⁺巨噬细胞的比例从27.5%(正常组,无干预)显著下降到8.24%(抑制剂组),显著降低了19.26%(p < 0.0001),证实了CCR2抑制成功(图6G)。肌内植入7天后,与HA组相比,显著更多的M2巨噬细胞浸润到DIBS的分级多孔结构中。然而,CCR2抑制后,M2巨噬细胞浸润急剧减少,表明CCR2信号传导对于DIBS诱导的M2巨噬细胞激活至关重要(图6H)。随后,研究人员采用BMSC-巨噬细胞共培养模型,在CCR2抑制下,研究BMSCs通过CCL2/CCR2通路对巨噬细胞增殖和极化的时空调节。细胞增殖试验显示,DIBS以CCR2依赖性方式促进巨噬细胞增殖。这种促增殖效应在第3天最为显著,并被CCR2抑制显著减弱。在外源性CCL2(40 ng mL⁻¹)或CCL2加抑制剂处理的组中也观察到类似的依赖性(图6I)。类似地,DIBS以CCR2依赖性方式显著上调巨噬细胞中M2表型标志物(CD206)。尽管诱导水平低于外源性CCL2达到的水平(p < 0.0001),但CCR2抑制后这种上调几乎消失(p < 0.0001)(图6J)。此外,DIBS显著下调了促炎标志物(iNOS)的表达,无论CCR2抑制与否,这种效应都持续存在(图6K)。
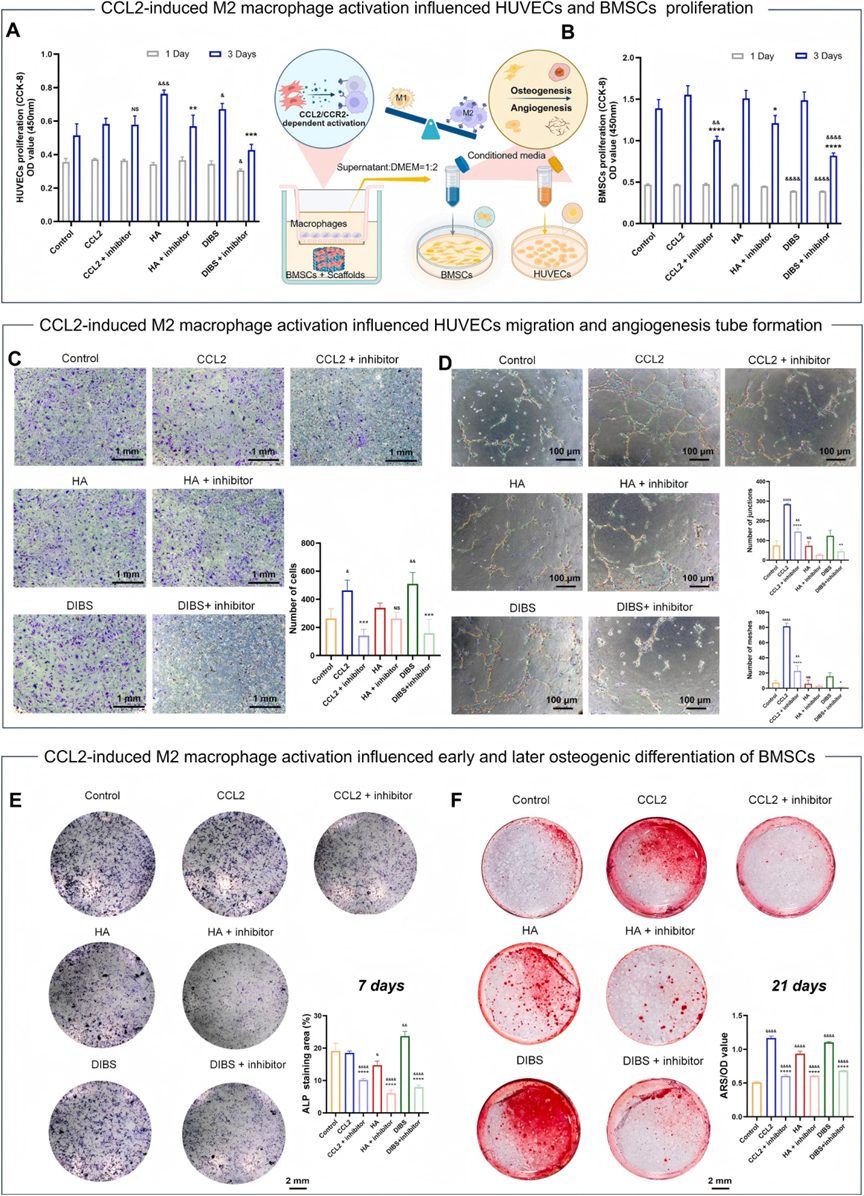
图7. CCL2/CCR2通路激活M2型巨噬细胞增强血管再生和骨形成过程
M2巨噬细胞可以通过分泌多种生长因子促进内皮细胞迁移和干细胞成骨分化。DIBS显著增加了巨噬细胞分泌骨形态发生蛋白-2(BMP2)和血管内皮生长因子(VEGF)。研究人员分析了CCR2依赖性M2巨噬细胞激活介导的免疫-成骨级联调节对成骨分化和血管生成的影响。如图7A所示,实验利用了在不同条件下培养的巨噬细胞和支架-BMSC构建体的条件培养基。与HA组相比,DIBS通过CCL2/CCR2轴诱导的M2巨噬细胞极化显著促进HUVECs和BMSCs的增殖(图7A和B)。功能测定进一步证明,M2巨噬细胞极化显著增强了HUVECs的迁移,增加了管状结构的数量,并改善了细胞连接完整性(图7C和D)。这种促血管生成效应在CCL2/CCR2依赖性激活下更为显著,CCR2抑制导致DIBS诱导的血管化不足。同样,CCL2诱导的M2巨噬细胞有利于BMSCs的成骨分化(图7E和F)。另外,Sr²⁺本身具有直接的成骨和促血管生成效应,可能有助于整体再生,即加入抑制剂后,DIBS仍然保持一定的成骨和血管生成活性。
在早期炎症调节之后,DIBS通过诱导分泌关键的免疫调节因子CCL2来激活M2巨噬细胞表型,从而进一步增强MSCs的免疫功能,进而促进血管生成并增强ESCs的成骨分化。与主要关注初始巨噬细胞反应的传统免疫调节策略相比,DIBS整合了干细胞的免疫调节功能及其与巨噬细胞的串扰,从而在时间序列上实现了多细胞免疫调节,有望促进临界尺寸骨缺损的功能性再生修复。
结论
研究团队开发了一种双重免疫调节骨支架(DIBS),可以在时空上编程免疫-成骨级联反应,用于功能性骨再生。DIBS是通过将含有Sr-PA纳米颗粒的pH响应性OXG/CMCS动态水凝胶与PA修饰的3D打印HA框架整合而构建的。DIBS中动态水凝胶与HA框架之间的多酚和席夫碱键合相互作用形成了具有优化机械性能的分级互连多孔结构,增强了内源性细胞的募集、粘附和迁移。具体来说,DIBS通过以下方式实现免疫-成骨级联的时空编程:i)在植入早期阶段,基于OXG的水凝胶将巨噬细胞从M1重编程为M2表型,从而抑制炎症并建立再生微环境;ii)在骨再生的中期阶段,酸性微环境触发的Sr²⁺和PA的持续释放,通过CCL2/CCR2信号轴训练MSCs获得增强的免疫调节功能,从而诱导M2巨噬细胞极化和HUVECs的血管化;iii)HA框架提供Ca²⁺和磷酸根离子,为新骨形成提供生物矿化来源。体内实验进一步证实,DIBS能有效诱导新骨形成、H型血管生成和功能性胶原排列,从而促进大鼠和兔模型中临界尺寸骨缺损的再生。这项研究首次揭示了一种通过将MSCs作为主动免疫调节单元整合到骨免疫调节材料设计中的新策略,实现了多细胞免疫调节,并在临床前大动物模型中实现了功能性骨再生。DIBS代表了一种有前景的骨免疫调节支架,为未来基于材料的骨再生策略提供启发。
获取原文:https://doi.org/10.1016/j.bioactmat.2026.04.002
关于开泰
亚洲熟妇无码乱子AV电影-日韩av第一区免费-人妻无码综合麻豆-玩弄JAPAN白嫩少妇HD小说-吻胸揉屁股摸腿娇喘视频网站成立于2006年,是集研发、生产、销售、科服为一体的生物高新技术企业;长期致力于为广大客户提供生命科研整体解决方案。
开泰的产品线包括单细胞转录组测序、单细胞多组学测序、空间转录组测序、空间蛋白组测定等单细胞时空组;ATAC-seq、ChIP-seq、m6A(MeRIP seq)、全基因组甲基化等表观组学;Ribo-seq、转录组、基因组和蛋白代谢等科研服务。产品广泛应用于生命科学、医学、农业-分子育种、制药、环境等领域的基础研究。客户遍布大学、研究所、医院、检验所、血站、出入境检验检疫等单位。在中国大陆大部分省市都设有自己的分公司或办事处。
开泰单细胞产品优势
1、千例样本炼就“解离超能力”,被称为“疑难组织克星”!
✅ 胰腺、肝脏、肾脏 ✅ 肠道、卵巢、动脉
✅ 脑组织、心肌、肌肉 ✅ 椎间髓核、颅骨、昆虫
✅ 植物组织及各类疑难组织
2、双平台火力全开,成本直降50%!
双平台:10X Genomics(主流)+ 华大智造DNBelab C(国产性价比之王)。
开泰更是以高难度样本水稻茎-叶鞘的单细胞测序数据通过华大智造的服务商认证,成为DNBelab C系列高通量单细胞RNA文库制备服务商。

3、开泰从样本到发文“全流程护航”!
免费解离测试 → 个性化生信分析 → 顶刊级图表输出
联系我们



 English
English

